微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (8分)已知溶液中:还原性HSO3->I-,氧化性IO3-> I2 > SO42-。在含3 molNa HSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如右图所示。
HSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如右图所示。

试回答下列问题:
(1)写出a点反应的离子方程式_____。
(2)写出b点到c点反应的离子方程式_________。
(3)当溶液中的I-为0.4 mol时,加入的KIO3为_________mol 。
(4)若往100 mL1mol/L的KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式为__________。
参考答案:
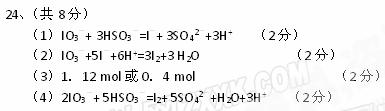
本题解析:略
本题难度:一般
2、选择题 下列说法正确的是(?)
A.SO2和SO3都是酸性氧化物,二者的水溶液都是强酸
B.将铜片放入浓硫酸中,无明显现象是因为铜片发生了钝化
C.硫粉在过量的纯氧中燃烧可以生成大量的SO3
D.富含硫黄的矿物在工业上可用于制造硫酸
参考答案:D
本题解析:SO2溶于水形成亚硫酸,亚硫酸是弱酸,A项错误;常温下铜片和浓硫酸不反应,加热条件下才反应,B项错误;硫粉在过量的纯氧中燃烧生成大量的SO2,C项错误。
本题难度:一般
3、选择题 将H2S、SO2、SO3各0.01mol依次通入1L水中,则该溶液具有(?)
A.中性、漂白性
B.酸性、漂白性
C.只有酸性
D.只有漂白性
参考答案:B
本题解析:略
本题难度:简单
4、推断题 短周期元素形成的常见非金属固体单质A与常见金属单质B,在加热条件下反应生成化合物C,C与水反应生成白色沉淀D和气体E,D既能溶于强酸,也能溶于强碱。E在足量空气中燃烧产生刺激性气体G,G在大气中能导致酸雨的形成。E被足量氢氧化钠溶液吸收得到无色溶液F。溶液F在空气中长期放置发生反应,生成物之一为H。H与过氧化钠的结构和化学性质相似,其溶液显黄色。
请回答下列问题:
(1)组成单质A的元素位于周期表中第______ 周期,第_______ 族。
(2)B与氢氧化钠溶液反应的化学方程式为:___________________________________________ 。
(3)G与氯酸钠在酸性条件下反应可生成消毒杀菌剂二氧化氯。该反应的氧化产物为_____________?,当生成2mol二氧化氯时,转移电子________mol 。
(4)溶液F在空气中长期放置生成H的化学反应方程式为:__________________________________。
(5)H的溶液与稀硫酸反应产生的现象为___________________________________________________________________________ 。
参考答案:(1)三;ⅥA
(2)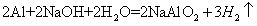
(3)硫酸钠(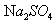 );2
);2
(4)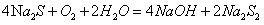
(或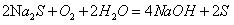 )
)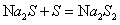
(5)溶液由黄色变为无色,产生浅黄色沉淀和(臭鸡蛋气味的)气体
本题解析:
本题难度:一般
5、选择题 若向含少量水蒸气的容器中通入SO2与H2S共1.00 mol,且知H2S过量,充分反应后,所得的氧化产物比还原产物多8.0 g,则通入的SO2和H2S的物质的量之比可能是
A.1∶1
B.1∶2
C.2∶1
D.1∶3
参考答案:D
本题解析:(差量法)H2S和SO2的反应方程式如下:
2H2S+SO2=3S+2H2O
SO2+2H2S=3S+2H2O ~ S(氧化、还原产物之差)
1 mol 32 g
n(SO2) 8.0 g
n(SO2)=0.25 mol,
n(SO2)∶n(H2S)=0.25 mol∶(1.00 mol-0.25 mol)=1∶3。
本题难度:简单