微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 为测定某镁铝合金样品中铝的含量,进行下列实验:取一定量合金,加入100 mL 0.3 mol?L-1稀硫酸,合金完全溶解,产生的气体在标准状况下体积为560 mL;再加入0.2 mol?L-1 NaOH溶液至沉淀质量恰好不再变化,用去350 mL NaOH溶液。则所取样品中铝的物质的量为
A.0.005 mol
B.0.010 mol
C.0.020 mol
D.0.030 mol
参考答案:B
本题解析:镁铝合金与硫酸反应生成硫酸镁、硫酸铝与氢气,向反应后的溶液中加入0.2 mol?L-1?NaOH溶液至沉淀质量恰好不再变化,铝离子转化为偏铝酸根、镁离子转化为氢氧化镁沉淀,此时溶液中溶质为Na2SO4、NaAlO2,根据硫酸根守恒有n(Na2SO4)=n(H2SO4)=0.1L×0.3mol/L=0.03mol,根据钠离子守恒有n(NaOH)=2n(Na2SO4)+n(NaAlO2),故n(NaAlO2)=0.35L×0.2mol/L-0.03mol×2=0.01mol,根据铝原子守恒n(Al)=n(NaAlO2)=0.01mol,选B。
本题难度:一般
2、选择题 如图是向MgCl2、AlCl3混合液中依次加入M和N时生成沉淀的物质的量与加入的M和N的体积关系图(M、N各表示盐酸或氢氧化钠溶液中的一种),以下结论不正确的是

A.混合溶液中c(AlCl3):c(MgCl2)=1:1
B.混合溶液中c(AlCl3):c(MgCl2)=3:1
C.V之前加NaOH溶液,V之后加盐酸
D.这种盐酸与NaOH溶液中溶质的物质的量浓度相同
参考答案:B
本题解析:根据图像可以得出先加入的氢氧化钠溶液后加入盐酸溶液,先加入氢氧化钠溶液时产生氢氧化镁和氢氧化铝两种沉淀,由于氢氧化铝溶于氢氧化钠所以当沉淀量达到最大时在加入氢氧化钠,氢氧化铝会发生溶解,而氢氧化镁不溶,氢氧化铝溶解完全时在加入盐酸,盐酸与偏铝酸钠反应生成氢氧化铝沉淀,不断加入盐酸,最终盐酸将氢氧化铝和氢氧化镁全部溶解。C正确,不选;根据图像可以知道消耗盐酸的体积与氢氧化钠的体积相同,根据反应方程式的书写,整个过程可以认为是盐酸与氢氧化钠溶液反应,所以二者的物质的溶度相同,D正确;根据沉淀OA和OB段可以确定生成氢氧化铝和氢氧化镁二者的物质的量相同,所以混合溶液中c(AlCl3):c(MgCl2)=1:1,所以答案选B。
本题难度:一般
3、选择题 如图所示,y表示沉淀的质量,x表示加入试剂的体积,能够用该图表示的反应是:
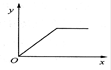
A.向AlCl3溶液中加入浓氨水至过量
B.向Ca(OH) 2溶液中通入CO2至过量
C.向Na[Al(OH)4]溶液中加入盐酸至过量
D.向AlCl3溶液中加入NaOH溶液至过量
参考答案:A
本题解析:氢氧化铝不溶于氨水,A正确。B中先生成碳酸钙沉淀,当CO2过量时,沉淀再溶解生成碳酸氢钙,不正确。C中首先生成氢氧化铝沉淀。当盐酸过量时,沉淀又全部溶解,不正确。D中首先生成氢氧化铝沉淀。当氢氧化钠过量时,沉淀又全部溶解,不正确。所以答案选A。
本题难度:一般
4、选择题 美国“海狼”潜艇上的核反应堆内使用了液体铝钠合金(单质钠和单质铝熔合而成)作载热介质,有关说法不正确的是
A.原子半径:Na<Al
B.铝钠合金若投入一定的水中可得无色溶液,则n(Al)≤n(Na)
C.铝钠合金投入到足量氯化铜溶液中,肯定有氢氧化铜沉淀也可能有铜析出
D.若m g不同组成的铝钠合金投入足量盐酸中,若放出的H2越多,则铝的质量分数越小
参考答案:AD
本题解析:同周期元素原子半径随原子序数的递增而逐渐减小,故A错误;相同质量的Al提供的电子多于相同质量的Na,故D错误。
本题难度:一般
5、选择题 将铁铝硅合金样品分等量两份分别与足量稀盐酸和烧碱充分反应放出氢气质量相同.合金中铁铝硅质量比不可能是( )
A.112:81:28
B.336:27:84
C.324:135:36
D.56:81:56
参考答案:不管是和酸反应还是和碱反应,铝产生的氢气的量是相等的,
所以只要铁和盐酸反应产生的氢气的量与硅和氢氧化钠反应产生的氢气的量相等就行了,
2Fe~2H2
112?4
Si~2H2
28? 4
所以铁与硅的质量比为112:28=4:1,
铝的量任意,
选项中AB符合,CD不符合,
故选CD.
本题解析:
本题难度:一般