微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (16分)“C 1化学”是指以碳单质或分子中含1个碳原子的物质(如CO、CO2、CH4、CH3OH、HCOOH等)为原料合成工业产品的化学工艺,对开发新能源和控制环境污染有重要意义。
(1)一定温度下,在两个容积均为2L的密闭容器中,分别发生反应:
CO2 (g)+3H2(g) CH3OH g)+H2O(g) △H=-49.0kJ/mol。相关数据如下:
CH3OH g)+H2O(g) △H=-49.0kJ/mol。相关数据如下:

请回答:
①a=_______。
②若甲中反应10s时达到平衡,则用CO2来表示甲中反应从开始到平衡过程中的平均反应速率是_________mol・L-1・S-1
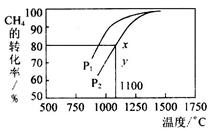
(2)甲烷的一个重要用途是制取H2,其原理为:CO2 (g)+ CH4 (g)  2CO(g)+2H2(g)在密闭容器中通入等物质的量浓度的CH4与CO2在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如下图所示,则压强P1______P2(填“大于”或“小于”);压强为P2时,在y点:
2CO(g)+2H2(g)在密闭容器中通入等物质的量浓度的CH4与CO2在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如下图所示,则压强P1______P2(填“大于”或“小于”);压强为P2时,在y点:
 (正)_________
(正)_________ (逆)(填“大于”、“小于”或“等于”)。
(逆)(填“大于”、“小于”或“等于”)。
(3)一定条件下,治理汽车尾气的反应是 

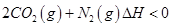 。在恒温恒容的密闭容器中通入
。在恒温恒容的密闭容器中通入 的混合气体,发生上述反应。下列图像正确且能说明反应在进行到
的混合气体,发生上述反应。下列图像正确且能说明反应在进行到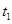 时刻一定达到平衡状态的是__________(选填字母)。
时刻一定达到平衡状态的是__________(选填字母)。

(4)甲酸(HCOOH)是一种弱酸,现用0.1mol・L-1 NaOH溶液分别滴定体积均为20.00mL、浓度均为0.1mol・L-1叫的盐酸和甲酸溶液,滴定曲线如下:

滴定开始前,三种溶液中由水电离出的c(H+)最大的是_________;V1和V2的关系V1_________V2(填“>”、“=”或“<”);M点对应的溶液中,各离子的物质的量浓度由大到小的顺序是_________。
参考答案:(1)①19.6;②0.03;(2)小于大于(3)cd
(4)甲酸溶液,<c(HCOO-)>c(Na+)>c(H+)>c(OH-)。每空2分
本题解析:(1)①甲和乙满足等效平衡的要求,所以放热的绝对值加和等于1摩尔二氧化碳反应时的热量,即a=49.0-29.4=19.6KJ;②根据反应计算二氧化碳的消耗量为29.4/49.0=0.6摩尔,所以二氧化碳的反应速率=0.6/2/10=0.03mol・L-1・S-1;(2)在相同的温度下,P1压强下,甲烷的转化率大,说明平衡正向移动,结合方程式分析P1压强低,所以P1小于P2,在P2压强下的平衡点为x点,所以从y到x需要提高甲烷的转化率,说明反应在向正向进行,所以填大于。(3)a反应在恒温的条件下进行平衡常数始终不变,所以错误;b在t1时刻,一氧化氮和二氧化碳的物质的量相等,但后面仍然在改变,所以反应没有到平衡,错误;c,由于最初加入的一氧化氮和一氧化碳的比例为2:1,反应按1:1进行,当在t1时刻之后一氧化氮和一氧化碳的物质的量比例保持不变,说明反应到达了平衡,正确;d二者的转化率不再变化,说明反应到平衡,正确。所以选cd。(4)等浓度的盐酸和甲酸,由于盐酸是强电解质,完全电离,甲酸是弱电解质,部分电离,所以第一个图为甲酸,第二个图为盐酸。甲酸电离出的氢离子浓度小些,对水的抑制作用小,所以甲酸溶液中水电离出的氢离子浓度大。盐酸完全反应后溶液为中性,但甲酸完全反应后溶液显碱性,所以甲酸溶液中氢氧化钠的加入量要少些才能到中性,所以V1<V2;当加入10毫升氢氧化钠时,溶液中存在等量的甲酸和甲酸钠,溶液显酸性,所以离子浓度关系为:c(HCOO-)>c(Na+)>c(H+)>c(OH-)。
考点:化学平衡计算,条件对化学平衡的影响,强弱电解质的比较
本题难度:困难
2、填空题 在一密闭容器中发生反应N2+3H2 2NH3 , ΔH<0,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:
2NH3 , ΔH<0,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:
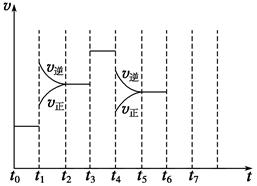
回答下列问题:
(1)处于平衡状态的时间段是__________(填选项)。
A t0~t1 B t1~t2 C.t2~t3
D.t3~t4 E.t4~t5 F.t5~t6
(2)t1、t3、t4时刻分别改变的一个条件是(填选项),t1时刻________; t4时刻________。
A 增大压强 B.减小压强 C.升高温度
D.降低温度 E.加催化剂 F.充入氮气
(3)依据(2)中的结论,下列时间段中,氨的百分含量最高的是__________(填选项)。
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6
(4)一定条件下,合成氨反应达到平衡时,测得混合气体中氨气的体积分数为20%,则反应后与反应前的混合气体体积之比为__________。
参考答案:(1) ACDF (2)C;B。 (3) A (4)5:6
本题解析:(1)当正反应速率等于逆反应速率时,反应达到化学平衡,根据图像可知,t0~t1、t2~t3、t3~t4、t5~t6,正反应速率等于逆反应速率,故答案为:ACDF。
(2)t1时正、逆反应速率都增大,平衡向逆反应方向移动,因为该反应的正反应为放热反应,所以升高温度,正、逆反应速率都增大,平衡向逆反应方向移动,故t1时刻改变的条件是升高温度;t4时刻正、逆反应速率都减小,平衡向逆反应方向移动,因为该反应正反应方向气体系数减小,所以减小压强,正、逆反应速率都减小,平衡向逆反应方向移动,故t4时刻改变的条件是减小压强。
(3)因为t0~t1、t2~t3、t3~t4、t5~t6,处于化学平衡状态,t1~t2、t4~t5,平衡向逆反应方向移动,所以氨的百分含量最高的是t0~t1。
(4)设反应前加入amol N2、bmol H2,达到平衡时生成2xmol NH3,则反应前混合气体总物质的量=(a+b)mol,反应后混合气体总物质的量=(a+b―2x),根据平衡时混合气体中氨气的体积分数为20%,可得:2x÷(a+b―2x)=0.2,解得a+b=12x,所以反应后与反应前的混合气体体积之比=(a+b―2x):(a+b)=(12x―2x):12x=5:6。
考点:本题考查图像的分析、化学平衡的判断、平衡移动的影响因素及应用、化学平衡的计算。
本题难度:一般
3、选择题 2007年国家最高科学技术奖授予石油化工催化剂专家闵恩泽教授,以表彰他在催化剂研究方面做出的突出贡献。下列关于催化剂的说法中正确的是
[? ]
A.使用催化剂可以增大正反应速率,减小逆反应速率
B.使用催化剂可以提高反应物的转化率
C.使用催化剂可以降低反应的活化能
D.使用催化剂可以改变反应的平衡常数
参考答案:C
本题解析:
本题难度:一般
4、选择题 可逆反应mA(g)+nB(s) rC(g)+qD(g)在反应过程中,其他条件不变,D的体积百分 含量和温度T 或压强P关系如图所示,下列叙述中正确的是
rC(g)+qD(g)在反应过程中,其他条件不变,D的体积百分 含量和温度T 或压强P关系如图所示,下列叙述中正确的是

A.温度降低,化学平衡向正反应方向移动
B.使用催化剂,D的物质的量分数增加
C.化学方程式系数m+n = r+q
D.物质B的颗粒越小,反应越快,有利于平衡向正反应方向移动