微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 现有如下两个反应:(A)NaOH + HCl = NaCl + H2O (B)2FeCl3 + Cu = 2FeCl2 + CuCl2
(1)根据两反应本质,判断能否设计成原电池(填“能”或“不能”)
(A)_______________(B)_______________
(2)如果(A或B)不能,说明其原因__________________________
(3)如果(A或B)可以,则写出正、负极材料及其电极反应式,电解质溶液
负极:____________; 正极:____________; 电解质溶液:______________
参考答案:(1)(A)不能;(B)能
(2)(A)的反应是非氧化还原反应,没有电子转移
(3)负极:铜,Cu-2e-=Cu2+;正极:碳棒(或其他),2Fe3++2e-=2Fe2+;电解质溶液:氯化铁溶液
本题解析:
本题难度:一般
2、选择题 关于原电池的叙述中正确的是?
A.构成原电池的电极是两种不同的金属
B.原电池是将化学能转化为电能的装置
C.原电池负极发生的电极反应是还原反应
D.原电池的正极是还原剂,总是溶液中的阳 离子在此被还原
离子在此被还原
参考答案:B
本题解析:略
本题难度:简单
3、选择题 下列说法中,正确的是
A.原电池是利用氧化还原反应将化学能转换为电能的装置
B.由于生铁中含碳,所以比纯铁耐腐蚀
C.在原电池中,电子从正极流向负极
D.在原电池中,负极上发生还原反应,正极上发生氧化反应
参考答案:A
本题解析:
正确答案:A
A.正确;
B.不正确,由于生铁中含碳,易在潮湿的空气中形成原电池,没纯铁耐腐蚀
C.不正确,在原电池中,电子从负极流向正极
D.不正确,在原电池中,负极上发生氧化反应,正极上发生还原反应。
本题难度:一般
4、选择题 下列各变化中属于原电池反应的是( )
A.在空气中金属铝表面迅速氧化形成保护层
B.镀锌铁表面有划损时,仍然能阻止铁被氧化
C.红热的铁丝与冷水接触,表面形成蓝黑色保护层
D.锌与稀硫酸反应时,用锌粉代替锌块可使反应加快
参考答案:A、在空气中金属铝表面迅速氧化形成保护层是发生的化学腐蚀,不是原电池反应,故A不符合;
B、镀锌铁表面破损后形成原电池反应,锌做负极,铁被保护,铁表面有划损时,仍然能阻止铁被氧化,故B符合;
C、红热的铁丝与冷水接触,表面形成蓝黑色保护层是发生的化学反应,故C不符合;
D、锌与稀硫酸反应时,锌粉和稀硫酸接触面积大于锌块的接触面积,用锌粉代替锌块可使反应加快,和原电池反应无关,故D不符合;
故选B.
本题解析:
本题难度:一般
5、选择题 某铅酸蓄电池的工作原理如图所示,其总反应式为Pb+PbO2+2H2SO4=2PbSO4+2H2O。下列判断不正确的是( )
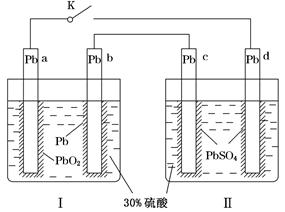
A.闭合K时,d电极的反应式为PbSO4+2H2O-2e-=PbO2+4H++SO42―
B.当电路中转移0.2 mol电子时,Ⅰ中消耗的H2SO4为0.2 mol
C.闭合K时,Ⅱ中SO42―向c电极迁移
D.闭合K一段时间后,Ⅱ可单独作为原电池,d电极为正极
参考答案:C
本题解析:闭合K时,Ⅰ为原电池,Ⅱ为电解池。Pb为负极,PbO2为正极,d为电解池的阳极,c为阴极。阳极上硫酸铅失电子生成的氧化铅附着在d电极上,A正确;根据总反应式可知,每有2 mol硫酸参与反应,则转移2 mol电子,B正确;闭合K时,Ⅱ中硫酸根离子向阳极移动,即向d电极移动,C错误;Ⅱ中电解时在阴极生成铅,阳极生成氧化铅,故电解一段时间后,Ⅱ也可作为原电池,D正确。
本题难度:一般