��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
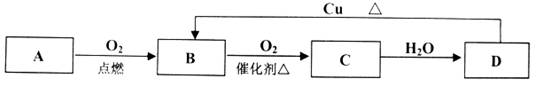
1������� (8��)A��B��C��D��������֮������ͼ��ʾ��ת����ϵ����֪��A��һ�ַǽ������ʣ�Ϊ��ɫ���壻B��C��D��Ϊ�����B���γ��������Ҫ�ɷ�֮һ��
��ش��������⣺
(1)������B��_______(�ѧʽ,��ͬ),������D��___________;
(2)B��C��ѧ��Ӧ��������________��Ӧ(����ϡ������ֽ⡱�����û������ֽ⡱)
(3)��D��ϡ��Һ�еμ�BaCl2��Һ���ܲ�����ɫ������д���÷�Ӧ�����ӷ���ʽ��
__________________________________________________��
�ο��𰸣�(1)SO2?H2SO4?(2)����? (3)Ba2����SO42��=BaSO4��
���������(1)B���γ��������Ҫ�ɷ�֮һ����֪BΪSO2����ǽ�������AΪS��CΪSO3��DΪH2SO4��
(2) SO2��O2��Ӧ����SO3��������������һ�ֻ�������ڻ��Ϸ�Ӧ��
(3)������ϡ��Һ�еμ�BaCl2��Һ���������ᱵ���������ᣬ���ӷ���ʽΪBa2����SO42��=BaSO4��
�ʴ�Ϊ��(1)SO2?H2SO4?(2)����? (3)Ba2����SO42��=BaSO4��
�����Ѷȣ�һ��
2���ƶ��� �ס��ҡ���Ϊ�������ʣ��ҡ�����Ԫ�������ڱ���λ��ͬһ���塣X��A��B��C��D��E��F��G��Ϊ�����Ļ��������A��X��Ħ��������ͬ��A��G����ɫ��ӦΪ��ɫ����һ�������£��������ת����ϵ��ͼ����ش�

��1��д��ѧʽ����________E________
��2��X�ĵ���ʽΪ_____________��
��3��д����Ӧ�Ļ�ѧ��Ӧ����ʽ��________________________��
��4��д��B��G��Һ��Ӧ����F�����ӷ���ʽ��________________________��
��5������ͼ�ķ�Ӧ�У�������������ԭ��Ӧ���ǣ�����ţ�____________________��
��6����8g ������������ȼ�գ���������Dͨ��100mL 3.5mol��L-1��B��Һ�У���ȫ���պ���Һ�е����ʼ������ʵ����ֱ�Ϊ________________����ͬ���������Dͨ��100mL 2.5mol��L-1��B��Һ�У���ȫ���պ���Һ���������ӵ����ʵ���Ũ���ɴ�С��˳��Ϊ________________��
�ο��𰸣���1��O2��SO3
��2��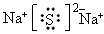
��3��2Na2O2+SO2==Na2SO4
��4��HCO3-+OH-==CO32-+H2O
��5�����
��6��0.15mol NaHSO3��0.1mol Na2SO3 ��c��Na+����c��HSO3-����c��H+����c��SO32-����c��OH-��
���������
�����Ѷȣ�����
3������� ij������Һ�п��ܺ���Na+��SO42-��SO32-��CO32-��Cl-��NO3-��HCO3-�����ӣ�����������ʵ�飮������BaCl2��H2SO4��HNO3��Ca��OH��2��������
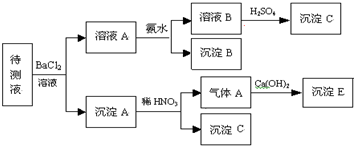
��1���жϴ���Һ������SO42-��SO32-����˵�����ɣ�______��
��2��д������B�Ļ�ѧʽ��______��
��3������C������ʲô���ʣ�______��
��4��д����������B�����ӷ���ʽ��______��
�ο��𰸣�����Һ���Ȼ�����Ӧ���ɳ���A��˵������Һ�к���SO42-��SO32-��CO32-�е�һ�֡����ֻ����֣�������м�ϡ������������ܽ��������壬˵������Һ�к���̼������ӣ������ᱵ�ܱ����������������ᱵ�����Դ�ʵ��֤������Һ�к���SO42-��SO32-�е�һ�ֻ����֣�������̼���������Ʒ�Ӧ����̼��ư�ɫ����E��
��ҺA�мӰ�ˮ���ɳ�������ˮ��̼��������ӷ�Ӧ����̼������ӣ�̼������Ӻͱ����ӷ�Ӧ����̼�ᱵ������˵������Һ�к���̼��������ӣ�������Ȼ����ǹ����ģ������Ӻ���������ӷ�Ӧ�������ᱵ�������ٸ���Ԫ�ػ���������ʷ������
��1��ͨ�����Ϸ���֪������Һ�к���SO42-��SO32-�е�һ�ֻ����֣���Ϊ����Һ����BaCl2��Һ��ϡHNO3������BaSO4������BaSO4�����ɿ�������SO42-��SO32-�е�һ�ֻ����֣�
�ʴ�Ϊ������SO42-��SO32-�е�һ�ֻ����֣���Ϊ����Һ����BaCl2��Һ��ϡHNO3������BaSO4������BaSO4�����ɿ�������SO42-��SO32-�е�һ�ֻ����֣�
��2��ͨ�����Ϸ���֪������B��BaCO3���ʴ�Ϊ��BaCO3��
��3��ͨ�����Ϸ���֪������C��BaSO4���ʴ�Ϊ��BaSO4��
��4����ˮ��̼��������ӡ������ӷ�Ӧ����̼�ᱵ������笠����ӡ�ˮ�����ӷ���ʽΪHCO3-+NH3?H2O+Ba2+=BaCO3��+NH4++H2O��
�ʴ�Ϊ��HCO3-+NH3?H2O+Ba2+=BaCO3��+NH4++H2O��
���������
�����Ѷȣ�һ��
4��ѡ���� ��֪A��B��C��D֮���ת����ϵA + B �� C + D������˵������ȷ���ǣ�?��
A����AΪFe��DΪ��������B�������ᣬҲ������ˮ
B����A��DΪ�����BΪˮ����C���������嵥�ʣ�Ҳ�����ǻ�����
C����A��B��C��D��Ϊ������÷�Ӧһ�����ڸ��ֽⷴӦ
D����A��B��C��D��Ϊ10����������C�ǿ�ʹʪ��ĺ�ɫʯ����ֽ���������壬��D
������һ����Һ̬
�ο��𰸣�C
���������A����ȷ��B����ȷ��C����Ӧ����Ϊ3NO2��H2O=2HNO3��NO���÷�ӦΪ������ԭ��Ӧ�������� D����ȷ��
�����Ѷȣ�һ��
5���ƶ��� ��12�֣�A��B��C��D��E���ֶ�����Ԫ�أ����ǵ�ԭ��������������AԪ�ص�ԭ�Ӱ뾶��С��BԪ�ص�����������Ӧˮ���������⻯����������M��D��Aͬ���壬����Eͬ���ڣ�EԪ��ԭ�ӵ������������ȴ�����������2��A��B��D��E������Ԫ�أ�ÿһ����CԪ�ض����γ�ԭ�Ӹ����Ȳ���ͬ�������ֻ������ش�
��1�� C��E����Ԫ����Ƚϣ�ԭ�ӵõ���������ǿ��Ԫ�������ڱ��е�λ��Ϊ?����������˵���У�������֤C��E�õ�������ǿ�����ǣ���д��ţ�?��
a���Ƚ�������Ԫ�صij������ʵķе�
b�������γɵĻ������У�CԪ�ص�ԭ���Ը���
c���Ƚ�������Ԫ�ص���̬�⻯����ȶ���
��2����M�к��еĻ�ѧ��������?��
��3��A��B��C��E���γ�������ʽ�Σ������и�����Ԫ�أ�����������ʽ����ˮ��Һ�����Ӧ�����ӷ���ʽΪ?��
��4��B2A4��һ�ֿ�ȼ��Һ�壬B2A4������ȼ�ϵ����һ�ּ���ȼ�ϵ�أ�B2A4����������ΪB2�����ϵĵ缫��ӦʽΪ?��
��5����֪1molD��ˮ��Ӧ�ų�283.5kJ����������д��D��ˮ��Ӧ���Ȼ�ѧ��Ӧ����ʽ?��
�ο��𰸣���1���ڶ����ڢ�A��? bc?��2�����Ӽ������ۼ�
��3��HSO3����H�� = H2O��SO2�� ����HSO3����HSO4�� = H2O ��SO2����SO42����
��4��N2H4+ 4OH����4e��= 4H2O��N2
��5��2Na(s)+2H2O(l)=2NaOH(aq)+H2(g)? ��H = �C567kJ/mol
���������A��ԭ�Ӱ뾶��С����AΪH��BԪ�ص�����������Ӧˮ���������⻯����������M����BΪN��MΪNH4NO3��EԪ��ԭ�ӵ������������ȴ�����������2����EΪS��D��Aͬ���壬����Eͬ���ڣ���DΪNa��ÿһ����CԪ�ض����γ�ԭ�Ӹ����Ȳ���ͬ�������ֻ������CΪO��
��1��O��Sͬ�壬O�ĵõ�������ǿ��O�����ڱ��е�λ��Ϊ�ڶ����ڢ�A�塣���ʵķе��ɷ��Ӽ�������������a������Ԫ���γɻ�����ʱ���õ�������ǿ���Ը��ۣ�b��ȷ����̬�⻯����ȶ�����ǽ������йأ��ǽ�����ǿ���⻯���ȶ���c��ȷ������ѡbc��
��2��NH4NO3�к������Ӽ����ۼ���
��3��H��O��Na��S�γɵ�������ΪNaHSO3��NaHSO4�����Է�Ӧ�����ӷ���ʽΪHSO3��+H��=H2O+SO2����
��4��N2H4������ȼ�ϵ�صĸ�����ӦΪN2H4+ 4OH����4e��= 4H2O��N2��
��5��Na��ˮ��Ӧ���Ȼ�ѧ����ʽΪ��2Na(s)+2H2O(l)=2NaOH(aq)+H2(g)?��H = �C567kJ/mol��
�����������ۺ���ǿ�������֪ʶ��ȫ�棬�Ǹ߿����ȵ�ϰ�⡣
�����Ѷȣ�һ��