��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��֪NH4CuSO3��������2mol/L������Һ����ȣ��������������к�ɫ��������?�ڲ����̼�����ζ������?����Һ������ɫ���ݴ��ж�����˵����ȷ���ǣ�������
A��NH4CuSO3����Ԫ�ر�����
B���÷�Ӧ��ʾ�����������
C���̼�����ζ�������ǰ���
D���÷�Ӧ��������������
2��ѡ���� ��һ�������£�RO3n-��I-�ɷ������·�Ӧ��RO3n-+6I-+6H+ = R-+ 3I2 +3H2O����RO3n-��RԪ�صĻ��ϼ�Ϊ
[? ]
A����1
B����3
C����5
D����7
3������� ������أ�K2FeO4�����м��ߵ������ԣ��Ի�������Ӱ�죬�����dz�Ϊ����ɫ��ѧ���Լ���ijУ��ѧ��ȤС��Ը�����ؽ���������̽����
I����������Ʊ���
����һ���¶��£�������ͨ��KOH��Һ���Ƶô��������Һ�����ھ��ҽ��������£���Fe��NO3��3?����������������Һ�У����Ʒ�Ӧ�¶ȣ����������طֽ⣻�ۼ�?KOH�����ͣ�ʹK2FeO4?����������پ������ò�Ʒ��
��1���¶ȹ��ᵼ�´�����طֽ��������ֻ��������֮һ������أ�KClO3�����˷�Ӧ��ѧ����ʽ��______��
��2���Ʊ����̵�����ӦΪ��a��b��c��d��e��fΪ��ѧ����ϵ������aFe?��OH��?3+b?ClO-+cOH-=d?FeO42-+e?Cl-+f?H2O����a��f=______��
II��̽��������ص�ij�����ʣ�
ʵ��1��������K2FeO4�ֱ��ܽ���pH?Ϊ?4.74��7.00��11.50?��ˮ��Һ�У����FeO42-Ũ��Ϊ?1.0mmol?L-1��1mmol?L-1=10-3mol?L-1�������������ã����첻ͬ��ʼ?pH?��ˮ��Һ��K2FeO4ij�����ʵ�Ӱ�죬�����ͼ1��ע��800min��������Һ�и�����ص�Ũ�Ȳ��ٸı䣩��
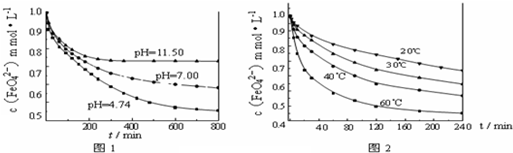
ʵ��2��������?K2FeO4?�ܽ���pH=4.74?��ˮ��Һ�У����Ƴ�FeO42-Ũ��Ϊ?1.0mmol?L-1?���������������ֱ�����?20�桢30�桢40���?60��ĺ���ˮԡ�У����첻ͬ�¶ȶ�K2FeO4ij�����ʵ�Ӱ�죬�����ͼ2��
��3��ʵ��1��Ŀ����______��
��4��ʵ��2�ɵó��Ľ�����______��
��5�����������ˮ�еķ�ӦΪ4FeO42-+10H2O?4Fe��OH��3+8OH-+3O2����
��ͼ1��֪��800minʱ��pH=11.50����Һ�и����������Ũ�ȱ�pH=4.74����Һ�иߣ���Ҫԭ����______��
���ø�����������ܵ�صĵ缫���ϣ�
Al-K2FeO4�����һ�ָ��ܵ�أ�����������Ϊ�������Һ�����õ�طŵ�ʱ������Ӧʽ�ǣ�______��
4��ѡ���� ��һ�������·������·�Ӧ��2KClO3+I2�T2KIO3+Cl2���������ƶϲ���ȷ���ǣ�������
A���÷�Ӧ�����û���Ӧ
B���÷�Ӧ��������ΪKClO3
C���÷�Ӧ�л�ԭ��ΪI2
D���÷�Ӧ��KClO3������ΪCl2��I2Ϊ����ԭKIO3
5������� ��1����������ԭ��Ӧ�У�������______?���ӣ������ķ�Ӧ��______��Ӧ����ԭ��______���ӣ������ķ�Ӧ��______��Ӧ������������Ӧ�ķ���ʽΪ2Fe+3Cl2=2FeCl3��������������______�ۣ���1mol����Ӧʱ����Ӧ��ת�Ƶĵ���______mol��������������ӷ�Ӧ����ʽΪ______��
��2��������������Ԫ����Fe2+��Fe3+����ʽ���ڣ��������������ױ����գ���ƶѪ�߲�����ʱ��Ӧ���躬Fe2+�������Σ�����������������ά����C����ʹʳ���е�Fe3+��ԭ��Fe2+���������������գ����������н��Т�Fe2+��Fe3+��ת��ʱ��Fe2+��______��������______��Ӧ��
��Fe3+��Fe2+��ת��ʱ��Fe3+��______��������______��Ӧ��