微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 有关如图所示原电池的叙述不正确的是

[? ]
A.电子沿导线由Cu片流向Ag片
B.正极的电极反应是Ag++e-=Ag
C.盐桥中的K+移向AgNO3溶液
D.用该电池电解饱和食盐水,有3.2 g Cu溶解时理论上生成1.12 LCl2
参考答案:D
本题解析:
本题难度:一般
2、填空题 (6分)用铜、银与硝酸银设计一个原电池,此电池的负极是: ,
负极的电极反应式是: ,
总反应方程式为 。
参考答案:负极是 Cu ,负极的电极反应式 Cu - 2e- ="=" Cu2+;总反应式 Cu + 2Ag+ ="= " 2Ag + Cu2+。
本题解析:略
本题难度:简单
3、填空题 将Zn棒和Cu棒用导线连接后,放入某电解质溶液中,构成如下图所示装置。试回答下列问题:
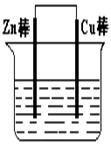
(1)若电解质溶液为稀硫酸,则Zn棒为原电池的 极,可观察到Cu棒的所产生现象是 ,写出该电极反应式: 。
(2)若电解质为硫酸铜溶液,则Cu棒上发生 反应,Zn棒上发生反应的电极反应式为: 。
参考答案:(10分)(1)负极(2分)有气泡生成(或有气体放出)(2分);2H++2e-=H2↑(2分)
(2)还原 (2分) Zn-2e-=Zn2+ (2分)
本题解析:(1)原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。锌比铜活泼,所以锌失去电子,做负极。铜是正极,溶液中的氢离子在正极得到电子,生成氢气,电极反应式是2H++2e-=H2↑,所以实验现象是有气泡生成(或有气体放出)。
(2)若电解质为硫酸铜溶液,则溶液中的铜离子在正极得到电子,发生还原反应。而锌仍然是负极,失去电子,电极反应式是Zn-2e-=Zn2+。
考点:考查原电池的有关判断以及电极反应式的书写
点评:该题是中等难度的试题,也是高考中的常见题型,属于基础性试题的考查。试题贴近教材,基础性强,有利于激发学生的学习兴趣和学习积极性。该题的关键是明确原电池的工作原理,然后结合题意灵活运用即可。有利于培养学生的逻辑推理能力和规范的答题能力。
本题难度:一般
4、选择题 铜片和锌片用导线连接后插入稀硫酸中构成原电池,下列说法正确的是
A.铜片做负极
B.铜片做正极
C.电子从铜片流向锌片
D.锌片上有气体产生
参考答案:B
本题解析:
本题难度:简单
5、选择题 铜锌原电池(如图所示)工作时,下列叙述正确的是:
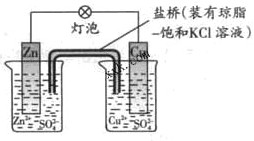
A.正极反应是:Zn