微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 Ⅰ. 在水溶液中橙红色的Cr2O72-与黄色的CrO42-有下列平衡关系:
Cr2O72-+H2O  2CrO42-+2H+,把K2Cr2O7溶于水配成稀溶液是橙色。
2CrO42-+2H+,把K2Cr2O7溶于水配成稀溶液是橙色。
(1)向上述溶液中加入NaOH溶液后,溶液呈?色,因为?。
(2)向已加入NaOH溶液的(1)中再加入过量稀H2SO4后,则溶液呈?色,因为?。
(3)向原溶液中加入Ba(NO3)2溶液(已知BaCrO4为黄色沉淀)则平衡向?方向移动,溶液颜色将?。(填“变深”、“变浅”或“不变”)
Ⅱ.实验室有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:
1.配制100mL 0.10mol/L NaOH标准溶液。
2.取20.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的标准NaOH溶液进行滴定。
3.重复上述滴定操作2~3次,记录数据如下。
实验编号
| NaOH溶液的浓度
(mol/L)
| 滴定完成时,NaOH溶液滴入的体积(mL)
| 待测盐酸溶液的体积
(mL)
|
1
| 0.10
| 22.62
| 20.00
|
2
| 0.10
| 22.58
| 20.00
|
3
| 0.10
| 22.60
| 20.00
|
?
(1)滴定达到终点的现象是?,此时锥形瓶内溶液的pH范围为?。
(2)根据上述数据,可计算出该盐酸的浓度约为?。
(3)排去碱式滴定管中气泡的方法应采用下图?的操作,然后挤压玻璃球使尖嘴部分充满碱液。
 ?
? ?
?
甲?乙?丙
(4)在上述实验中,下列操作(其它操作正确)会造成测定结果偏高的有?(多选扣分)。
A.滴定终点读数时俯视读数
B.酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
C.锥形瓶水洗后未干燥
D.配制NaOH标准溶液时,没有等溶解液降至室温就转移至容量瓶中
E.配制NaOH标准溶液时,定容时仰视容量瓶的刻度线
F.碱式滴定管尖嘴部分有气泡,滴定后消失
2、选择题 NH3氧化制硝酸时,在吸收塔里发生如下反应:3NO2+3H2O 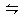 2HNO3+NO △H<0,为了提高HNO3的产量,在理论上应该采取的措施是(?)
2HNO3+NO △H<0,为了提高HNO3的产量,在理论上应该采取的措施是(?)
A.降温
B.升温
C.减压
D.增压
3、实验题 为证明化学反应有一定的限度,进行如下探究活动:
I.取5mL 0.1mol/L的KI溶液,滴加5―6滴FeCl3稀溶液;?
Ⅱ.继续加入2mL CCl4,盖好玻璃塞,振荡静置。
Ⅲ.取少量分液后得到的上层清液,滴加KSCN溶液。
Ⅳ.移取25.00mLFeCl3稀溶液至锥形瓶中,加入KSCN溶液用作指示剂,再用c mol/LKI标准溶液滴定,达到滴定终点。重复滴定三次,平均耗用c mol/LKI标准溶液VmL。
(1)探究活动I中发生反应的离子方程式为?。
请将探究活动Ⅱ中“振荡静置”后得到下层液体的操作补充完整:将分液漏斗放在铁架台上,静置。
?。
(2)探究活动Ⅲ的意图是通过生成红色的溶液(假设溶质全部为Fe(SCN)3),验证有Fe3+残留,从而证明化学反应有一定的限度,但在实验中却未见溶液呈红色。对此同学们提出了下列两种猜想:
猜想一:Fe3+全部转化为Fe2+?猜想二:生成的Fe(SCN)3浓度极小,其颜色肉眼无法观察。
为了验证猜想,查阅资料获得下列信息:
信息一:乙醚微溶于水,密度为0.71g/mL,Fe(SCN)3在乙醚中的溶解度比在水中大;
信息二:Fe3+可与[Fe(CN)6]4―反应生成暗蓝色沉淀,用K4[Fe(CN)6](亚铁氰化钾)溶液检验Fe3+的灵敏度比用KSCN溶液更高。
结合新信息,现设计以下实验方案验证猜想:
①请完成下表
实验操作
| 现象和结论
|
步骤一:
| 若产生暗蓝色沉淀,则?。
|
步骤二:
| 若乙醚层呈红色,则?。
|
?
②写出实验操作“步骤一”中的反应离子方程式:?。
(3)根据探究活动Ⅳ,FeCl3稀溶液物质的量浓度为?mol/L。
4、填空题 工业上可利用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下所示:
化学反应
| 平衡
常数
| 温度/℃
|
500
| 700
| 800
|
①2H2(g)+CO(g) CH3OH(g) CH3OH(g)
| K1
| 2.5
| 0.34
| 0.15
|
②H2(g)+CO2(g) H2O(g)+CO(g) H2O(g)+CO(g)
| K2
| 1.0
| 1.70
| 2.52
|
③3H2(g)+CO2(g) CH3OH(g)+H2O(g) CH3OH(g)+H2O(g)
| K3
| ?
| ?
| ?
|
?
请回答下列问题:
(1)反应②是________(填“吸热”或“放热”)反应。
(2)据反应①与②可推导出K1、K2与K3之间的关系,则K3=__________(用K1、K2表示)。
(3)500 ℃时测得反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol・L-1)分别为0.8、0.1、0.3、0.15,则此时v正________v逆(填“>”、“=”或“<”)。
(4)反应①按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如下图所示。下列说法正确的是__________(填序号)。

A.温度:T1>T2>T3
B.正反应速率:v(a)>v(c),v(b)>v(d)
C.平衡常数:K(a)>K(c),K(b)=K(d)
D.平均摩尔质量:M(a)>M(c),M(b)>M(d)
5、选择题 I2在KI溶液中存在下列平衡:I2(aq) + I一(aq) 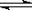 I3一(aq)。测得不同温度下该反应的平衡常数值如下表:
I3一(aq)。测得不同温度下该反应的平衡常数值如下表:
t/℃
| 5
| 15
| 25
| 35
| 50
|
K
| 1100
| 841
| 680
| 533
| 409
|
下列说法正确的是
A.反应I2(aq)+I一(aq) 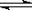 I3-(aq)的△H>0
I3-(aq)的△H>0
B.利用该反应可以除去硫粉中少量的碘单质
C.在上述体系中加入苯,平衡不移动
D.25℃时,向溶液中加入少量KI固体,平衡常数K小于680