��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� .A��B��C��Ϊ������Ԫ�أ����������ڱ��е�λ����ͼ��ʾ.��֪B��C��Ԫ��ԭ������֮��ΪAԪ��ԭ��������4������A��B��C�����ǣ�?��
A.C��Al��P? B.N��Si��S? C.O��P��Cl? D.F��S��Ar
�ο��𰸣�C
�����������A��ԭ������Ϊa������������aΪ8
�����Ѷȣ�һ��
2��ѡ���� Ԫ��R����ۺ�����Ļ�ѧʽΪHnRO2n��2?��������̬�⻯����RԪ�صĻ��ϼ�Ϊ��?��
A��12��3n
B��3n��12
C��3n��10
D��6��3n
�ο��𰸣�B
�����������̬�⻯����Ԫ��һ��Ϊ��ͼ�̬�����ݻ������л��ϼ۵Ĵ�����Ϊ0��RԪ�ص���ۺ�������R�Ļ��ϼ�Ϊ��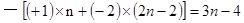 ����ͼ۵ľ���ֵ�����̬�ĺ�Ϊ8������R����ͼ�̬��Ϊ��ֵ��Ϊ
����ͼ۵ľ���ֵ�����̬�ĺ�Ϊ8������R����ͼ�̬��Ϊ��ֵ��Ϊ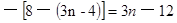 ����ѡB��
����ѡB��
�����Ѷȣ���
3������� A��B��C��D��E��F���ֶ���������Ԫ�أ�ԭ��������������AԪ�ص�һ�ֺ���������������������ֵ����ȣ�B��Eͬ���壬�Һ˵����֮��Ϊ1�U2��C�ĵ���������ˮ���ҷ�Ӧ������ǿ������Һ�к������ֵ�������ͬ�����������ӣ�D���������������ڲ����������һ�롣�Իش��������⣺
��1��Fλ�����ڱ��е�________����________�塣
��2������ʱ��39 g B��C��ԭ�Ӹ�����1�Ul�γɵĻ�����X������CO2��Ӧ�ų�Q kJ��������д���÷�Ӧ���Ȼ�ѧ����ʽ?��
д������X��FeCl2��Һ��Ӧ�����ӷ���ʽ_______________________________________��
��3��B��C��F��ɵĻ�����Y�Ǽ�������������Ҫ�ɷ֣�Y����Һ�ʼ��ԣ������ӷ���ʽ������ԭ��______________________________�����������õ�������ʽΪ_________��
��4����ԭ�ӷ���Z��C�ĵ��ʺ�ˮ��Ӧ���õ������ӵ�������ȣ�Z�ķ��ӿռ乹��Ϊ___________�ͣ�������_________���ӣ�����ԡ��Ǽ��ԡ�������Ƚ�Z��DA3�ķе�ߵͲ����Խ���_____________________________________________________��
��5��Ŀǰ���������о�����һ�ָ��ܵ�أ����������ڵ�C��E����Ϊ��������C��
�ӵ������-Al2O3�մ����������ʣ���ӦʽΪ��2C+xE  ?C2Ex����д����طŵ�ʱ�������ĵ缫��Ӧʽ��������Ӧʽ��_______________________���øõ������Դ���е�⺬��0.2 mol CuSO4��0.2 mol NaCl�Ļ����Һ500 mLʱ�����˵�ع���һ��ʱ�������23 g C���ʡ������������������Ϊ��________L����״���£���������Һ��ˮϡ����2 L ����Һ��pHΪ��________��
?C2Ex����д����طŵ�ʱ�������ĵ缫��Ӧʽ��������Ӧʽ��_______________________���øõ������Դ���е�⺬��0.2 mol CuSO4��0.2 mol NaCl�Ļ����Һ500 mLʱ�����˵�ع���һ��ʱ�������23 g C���ʡ������������������Ϊ��________L����״���£���������Һ��ˮϡ����2 L ����Һ��pHΪ��________��
�ο��𰸣���1����?��A ����1�֣�?
��2��2Na2O2(s) + 2CO2(g) = 2Na2CO3(s) + O2(g)����H= -4Q kJ/mol
3Na2O2 + 6Fe2+ + 6H2O = 6Na+ + 4Fe(OH)3��+ 2Fe3+����2�֣�
��3��ClO-+ H2O  HClO + OH-
HClO + OH- ?����2�֣�
?����2�֣�
��4��������1�֣����ԣ�1�֣�NH3�ķе����PH3����ΪNH3���Ӽ���������2�֣�
��5��xS��2e��=Sx2��?6.72 L?1����2�֣�
���������AԪ�ص�һ�ֺ���������������������ֵ�����,˵��A��H��B��Eͬ���壬�Һ˵����֮��Ϊ1�U2��B��O��E��S��C�ĵ���������ˮ���ҷ�Ӧ������ǿ������Һ�к������ֵ�������ͬ�����������ӣ�C��Na,Na����OH�D��������ͬ��D���������������ڲ����������һ�룬D��P����A�DH��B�DO��C�DNa��D�DP��E�DS��F�DCl��
��1����?��A?
��2��39 gNa2O2��Ӧ�ų�QkJ��������2molNa2O2��CO2��Ӧ�ų�4QkJ�����������ԣ�
2Na2O2(s) + 2CO2(g) = 2Na2CO3(s) + O2(g)����H= -4Q kJ/mol
3Na2O2 + 6Fe2+ + 6H2O = 6Na+ + 4Fe(OH)3��+ 2Fe3+
��3��ClO-+ H2O  HClO + OH-?
HClO + OH-? ?
?
��4��������1�֣����ԣ�1�֣�NH3�ķе����PH3����ΪNH3���Ӽ���������2�֣�
��5��xS��2e��=Sx2��? ;�Ⱥ�������2����Ӧ��
CuCl2 Cu��Cl2��,? 2e�D?
Cu��Cl2��,? 2e�D?
0.1mol? 0.1mol? 0.2mol?
2CuSO4��2H2O 2 Cu?��O2���� H2SO4 ?4e�D
2 Cu?��O2���� H2SO4 ?4e�D
0.1mol? 0.05mol? 0.1mol? 0.2mol
2H2O 2H2����O2��? 4e�D
2H2����O2��? 4e�D
0.15mol? 0.6mol
����������0.1mol+ 0.05mol+ 0.05mol="0.3mol," ��6.72 L���壻������0.1molH2SO4, ��ˮϡ����2 L�������ӵ�Ũ��Ϊ��0.1mol��2/2L=0.1mol/L��PH= 1 ��
�����Ѷȣ�һ��
4������� �ǽ���Ԫ��R���䵥��4.8g�������г��ȼ������RO29.6g����Rԭ���У�������������������������R��Ԫ������Ϊ?�������Ϊ?������������Ԫ�رȽϣ�R���⻯���?�ȶ���R������������ˮ�������Ա�?����
�ο��𰸣���+6��PH3,HClO4
������������ݻ�ѧ��Ӧ�������غ㶨�ɣ�O2������Ϊ9.6g-4.8g=4.8g������RO2��R��O2��������ȣ���R��Ħ��������O2��Ħ��������ȣ�RΪSԪ�أ����Ϊ+6�ۣ��ǽ����ԣ�Cl>S>P����R���⻯���PH3�ȶ���R������������ˮ�������Ա�HClO4����
���������⿼����ǻ�ѧ����ʽ�ļ����Ԫ�������ɵ�֪ʶ����Ŀ�ѶȲ�����ѧ���Ի���֪ʶ�����ճ̶ȼ�����������
�����Ѷȣ�һ��
5��ѡ���� ���и����ʻ������ʵıȽ�����ȷ����
A���е㣺H2O��H2S��H2Se
B�����ȶ��ԣ�H2CO3��NaHCO3��Na2CO3
C���뾶��Cl��Cl����S2��
D�����ԣ�H2CO3��HNO3��H3PO4
�ο��𰸣�C
�����������
�����Ѷȣ���