微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列溶液中有关物质的量浓度关系正确的是?
[? ]
A.在0.1mol/L的Na2S溶液中:c(OH-)= c(H+)+ c(HS-)+ c(H2S)
B.pH相等的CH3COONa、NaOH和Na2CO3:c(NaOH)<c(CH3COONa)<c(Na2CO3)
C.物质的量浓度相等CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-) +2c(OH-)=2c(H+) + c(CH3COOH)
D.0.1mol・L-1NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-)
2、选择题 关于浓度均为0.1mol・L-1的三种溶液:①氨水 ②盐酸 ③氯化铵溶液,下列说法不正确的是
[? ]
A.溶液的pH:①>③>②
B.水电离出的(H+):③>②>①
C.①和②等体积混合后的溶液:c(H+) =c(OH-)+c(NH3・H2O)
D.①和③等体积混合后的溶液呈碱性:c(NH4+) >c(Cl-) >c(OH-) > c(H+)
3、填空题 常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表
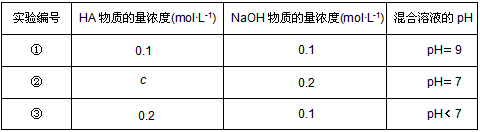
请回答:
(1)从①组情况分析, HA是___________(填“强酸”或“弱酸”)。
(2)②组情况表明,c___________0.2 (填“大于”、“小于”或 “等于”)。混合液中离子浓度
c(A-)与 c(Na+)的大小关系是___________。
(3)分析第③组实验结果,说明HX的电离程度________NaX的水解程度(填“大于”或“小于”)。该混合溶液中离子浓度由大到小的顺序是___________。
(4)①组实验所得混合溶液中由水电离出的c(OH-)=___________mol・L-1。
(5)写出该混合溶液中下列算式的精确结果(不能作近似计算:)。
c(Na+)-c(A-)=___________mol・L-1;c(OH-)-c(HA)=___________mol・L-1。
4、填空题 按要求写离子方程式,并回答有关问题。
(1)氢硫酸的电离:___________,溶液中c(H+)、c(HS-)、c(S2-)的大小关系__________。
(2)碳酸钠的水解:___________。
(3)某学生做如下实验,将盛有滴加酚酞的0.1 mol/L NaHCO3溶液的试管微热,观察到此溶液的浅红色加深,若冷却至室温时则又变回原来的颜色,为什么?(用方程式说明) 答:_____________________________。
5、选择题 下列有关电解质溶液中微粒的物质的量浓度关系正确的是
[? ]
A. 在0.1 mol/L NaHCO3溶液中:c(Na+)?> c(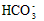 )> c(
)> c( )?> c(H2CO3)
)?> c(H2CO3)
B. 在0.1 mol/L Na2CO3溶液中:c(OH-) - c(H+)?= c(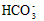 ) + c(H2CO3)
) + c(H2CO3)
C. 向0.2 mol/L NaHCO3溶液中加入等体积0.1 mol/L NaOH溶液:c( )?>c(
)?>c( )?>c(OH-)?>c(H+)
)?>c(OH-)?>c(H+)
D. 向 0.1 mol/L的CH3COONa溶液中加入等体积0.1 mol/L CH3COOH溶液:2c(H+) - c(CH3COO-) =2c(OH-) - c(CH3COOH)