微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列事实不能用勒夏特列原理解释的是
[? ]
A.开启啤酒瓶后,瓶中立刻泛起大量泡沫
B.SO2催化氧化成SO3的反应,往往需要使用催化剂
C.向氯水中加CaCO3后,溶液漂白性增强
D.棕红色NO2加压后颜色先变深后变浅
参考答案:B
本题解析:
本题难度:一般
2、简答题 我国有丰富的天然气资源.以天然气为原料合成尿素的主要步骤如图所示(图中某些转化步骤及生成物未列出):
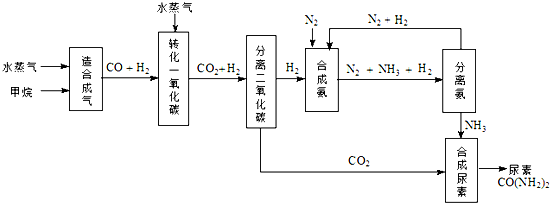
(1)“造合成气”发生的热化学方程式是CH4(g)+H2O(g)?CO(g)+3H2(g);△H>0
在恒温恒容的条件下,欲提高CH4的反应速率和转化率,下列措施可行的是______.
A、增大压强?B、升高温度?C、充入He气?D、增大水蒸气浓度
(2)“转化一氧化碳”发生的方程式是H2O(g)+CO(g)?H2(g)+CO2(g),该反应平衡常数随温度的变化如下:
提高氢碳比[n(H2O)/n(CO)],K值______(填“增大”、“不变”或“减小”);若该反应在400℃时进行,起始通入等物质的量的H2O和CO,反应进行到某一时刻时CO和CO2的浓度比为1:3,此时v(正)______v(逆)(填“>”、“=”或“<”).
(3)有关合成氨工业的说法中正确的是______.
A、该反应属于人工固氮
B、合成氨工业中使用催化剂能提高反应物的利用率
C、合成氨反应温度控制在500℃左右,目的是使化学平衡向正反应方向移动
D、合成氨工业采用循环操作的主要原因是为了加快反应速率
(4)生产尿素过程中,理论上n(NH3):n(CO2)的最佳配比为______,而实际生产过程中,往往使n(NH3):n(CO2)≥3,这是因为______.
(5)当甲烷合成氨气的转化率为60%时,以3.0×108L甲烷为原料能够合成______L?氨气.(假设体积均在标准状况下测定)
参考答案:(1)A、增大压强,反应速率加快,平衡向逆反应方向移动,甲烷的转化率降低,故A错误;
B、升高温度,反应速率加快,平衡向正反应方向移动,甲烷的转化率增大,故B正确;
C、充入He气,反应混合物的浓度不变,反应速率不变,平衡不移动,甲烷的转化率不变,故C错误;
D、增大水蒸气浓度,反应速率加快,平衡向逆反应方向移动,甲烷的转化率增大,故D正确;
故答案为:BD;
(2)平衡常数只受温度影响,与反应物的浓度无关,提高氢碳比[n(H2O)/n(CO)],K值不变;
令开始H2O和CO的物质的量都是1mol,某一时刻时CO和CO2的浓度比为1:3,设此时参加反应CO为xmol,则(1-x):x=1:3,解得x=0.75,则:
? H2O(g)+CO(g)?H2(g)+CO2(g),
?开始(mol):1? 1? 0? 0
?变化(mol):0.75? 0.75? 0.75? 0.75
某时刻(mol):0.25? 0.25? 0.75? 0.75
故产生浓度商Qc=0.75×0.750.25×0.25=9<9.94,反应向正反应进行,故v(正)>v(逆),
故答案为:不变;>;
(3)A.固氮指由游离态的氮转化为化合态的氮,合成氨属于人工固氮,故A正确;
B.催化剂加快反应速率,不能影响平衡移动,不能提高反应物的利用率,故B错误;
C.该反应正反应是放热反应,高温不利用氨气的合成,合成氨反应温度控制在500℃左右,在该温度下反应速率较快、催化剂活性较高,故C错误;
D.合成氨工业采用循环操作,目的是提高原料的利用率,故D错误;
故答案为:A;
(4)根据尿素的化学式CO(NH2)2,C、N原子完全利用最后,由C、N原子守恒可知生产尿素过程中,理论上n(NH3):n(CO2)的最佳配比为2:1;
往往使n(NH3):n(CO2)≥3,这是由于:有利于提高CO2的转化率,且NH3极易溶于水,便于分离、回收利用;
故答案为:2:1;有利于提高CO2的转化率,且NH3极易溶于水,便于分离、回收利用;
(5)由CH4(g)+H2O(g)?CO(g)+3H2(g),N2(g)+3H2(g)?2NH3(g),可得CH4(g)~3H2(g)~2NH3(g),设能够合成氨气的体积为VL,则:
? CH4(g)~3H2(g)~2NH3(g),
? 1? 2
3.0×108L×60%? VL
故V=3.0×108L×60%×2=3.6×108L
合成气的反应中:CH4~~~~~~~~~CO~~~~~~~~~~3H2,
? 3.0×108L×60%?3.0×108L×60%?3.0×108L×60%×3
分离二氧化碳过程生成的H2体积:CO~~~~~~~~~~H2,
?3.0×108L×60%? 3.0×108L×60%?
所以产生的氢气的总体积为3.0×108L×60%×3+3.0×108L×60%=12×108L×60%
令产生氨气的体积为V,则:
? 3H2~~~~~~~~~2NH3
? 3? ? 2
? 12×108L×60%? ?V
故V=12×108L×60%×23=4.8×108L?
故答案为:4.8×108.
本题解析:
本题难度:一般
3、选择题 体积不变的密闭容器中发生反应2SO2(g)+O2(g)?2SO3(g),从开始到平衡过程中保持不变的是( ? )
A.气体的总物质的量
B.气体的总质量
C.气体压强
D.气体的平均式量
参考答案:B
本题解析:
本题难度:一般
4、选择题 下列事实不能用勒夏特列原理来解释的是( )
A.加压有利于SO2与O2反应生成SO3
B.温度过高对合成氨反应不利
C.高温及加入催化剂都能使合成氨的反应速率加快
D.用过量空气煅烧硫铁矿可以提高原料的利用率
参考答案:C
本题解析:
本题难度:一般
5、选择题 下列事实不能用勒夏特列原理解释的是
[? ]
A.温度控制在500℃有利于合成氨反应
B.用排饱和食盐水法收集Cl2
C.打开碳酸饮料会有大量气泡冒出
D.工业制取金属钾Na(l)+KCl(l) NaCl(l)+K(g)选取适宜的温度,使钾成蒸气从反应混合物中分离出来
NaCl(l)+K(g)选取适宜的温度,使钾成蒸气从反应混合物中分离出来
参考答案:A
本题解析:
本题难度:一般