微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 如图I所示,甲、乙之间的隔板K和活塞F都可以左右移动,F受压力恒定.甲中充入2mol?A和1mol?B,乙中充入2mol?C和1mol?He,此时K停在0处.在一定条件下发生可逆反应:2A(g)+B(g)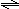 2C(g),反应达到平衡后,再恢复至原温度,则下列说法正确的是(? )
2C(g),反应达到平衡后,再恢复至原温度,则下列说法正确的是(? )
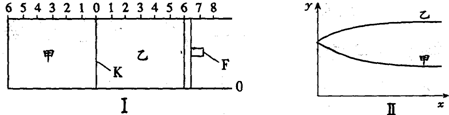
A.达到平衡时,隔板K最终停留在0刻度左侧的2到4之间
B.若达到平衡时,隔板K最终停留在左侧1处,则乙中C的转化率小于50%
C.若达到平衡时,隔板K最终停留在左侧靠近2处,则乙中F最终停留在右侧的刻度大于4
D.如图II所示,若x轴表示时间,则y轴可表示甲、乙两容器中气体的总物质的量或A的物质的量
2、简答题 硝酸工业的基础是氨的催化氧化,在催化剂作用下发生如下反应:
①4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-905kJ/mol?①主反应
②4NH3(g)+3O2(g)?2N2(g)+6H2O(g)△H=-1268kJ/mol?②副反应
有关物质产率与温度的关系如甲图.
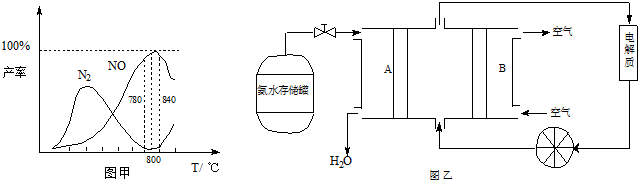
(1)由反应①②可知反应③N2(g)+O2(g)?2NO(g)的反应热△H=______
(2)由图甲可知工业上氨催化氧化生成?NO时,反应温度最好控制在______
(3)用Fe3O4制备Fe(NO3)3溶液时,需加过量的稀硝酸,原因一:将Fe4O3中的Fe2+全部转化为Fe3+,原因二:______(用文字和离子方程式说明).
(4)将NH3通入NaClO溶液中,可生成N2H4,则反应的离子方程式为______.
(5)依据反应②可以设计成直接供氨式碱性燃料电池(如乙图所示),则图中A为______(填“正极”或“负极”),电极方程式为______.
3、选择题 恒温下,容积均为2L的密闭容器M、N中,分别有以下列两种起始投料建立的可逆反应 3A(g)+2B(g)?2C(g)+xD(s)?的化学平衡状态,相关数据如下:M:3molA?2molB;?2min达到平衡,生成D1.2mol,测得从反应开始到平衡C的速率为0.3mol/Lmin.N:2molC?ymolD;?达到平衡时c(A)=0.6mol/L.下列推断的结论中不正确的是( )
A.x=2
B.平衡时M中c(A)=0.6mol/L
C.y>0.8
D.y=2
4、选择题 在体积为VL的恒容密闭容器中盛有一定量H2,通入Br2(g)发生反应:
H2(g)+Br2(g)

2HBr(g);△H<0.当温度分别为T1、T2平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示.
下列说法正确的是( )
A.由图可知:T2>T1
B.两点的反应速率:a>b
C.T1时,随着Br2(g)加入,平衡时HBr的体积分数不断增加
D.a点比b点体系的颜色深