| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点讲解《物质的量》高频考点特训(2017年练习版)(八)
参考答案:B 本题解析:同质量时,气体的摩尔质量越大,则体积越小,因M(Cl2)>M(CO2)>M(N2)>M(H2),则体积最大的为氮气,故答案选B. 本题难度:一般 4、选择题 将VLHCl气体(?标准状况)溶于水制得1000mL盐酸溶液,则该盐酸的物质的量浓度为( )
B.
C.
D.
参考答案:标准状况下,VLHCl气体的物质的量为n=VL22.4L/mol=V22.4mol, 本题解析: 本题难度:简单 5、选择题 用NA表示阿伏加德罗常数的值,下列叙述正确的是( ) |
参考答案:C
本题解析:
试题解析:溶液体积未知,无法计算Na+离子数,故A错误;浓硫酸随反应进行,浓度减小为稀硫酸不与铜发生反应,生成SO2分子数目小于0.46NA,故B错误;C、标准状况下,22.4 L气体的物质的量为1mol,且氢气和氯气都是双原子分子,故原子总数为2NA,C正确;依据化学方程式定量关系计算,3Fe+4H2O=Fe3O4+4H2,0.10mol Fe粉与足量水蒸气反应生成的H2分子数为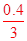 NA,故D错误。
NA,故D错误。
考点:阿伏加德罗常数
本题难度:一般
|
||
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | ||
| 下一篇:高中化学知识点讲解《物质的量浓.. | ||