微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列有关说法正确的是
[? ]
A.两种元素组成的分子中一定只有极性键
B.离子化合物的熔点一定比共价化合物高
C.非金属元素组成的化合物一定是共价化合物
D.含有阴离子的化合物一定含有阳离子
参考答案:D
本题解析:
本题难度:简单
2、选择题 下列含有非极性键的共价化合物是
[? ]
A.Cl2
B.Na2O2
C.C2H2
D.CO2
参考答案:C
本题解析:
本题难度:简单
3、填空题 如表是元素周期表的一部分,根据①~⑩在周期表中的位置,用元素符号或化学式回答下列问题:

(1)金属性最强的元素是______,最容易与H2反应单质是______.
(2)⑤位于周期表中第______周期,______族;其原子结构示意图为______.
(3)最高价氧化物所对应的水化物酸性最强的是______(填化学式).
(4)②与⑧形成的化合物属于______(填“离子化合物”或“共价化合物”).
(5)最高价氧化物既能与酸反应又能与碱反应的是______(填化学式).
(6)③和⑦对应的氢化物较稳定的是______(填化学式).
(7)⑤和⑥的原子半径较大是______,⑤和⑥的最高价氧化物对应水化物的碱性较强的是______(填化学式).
(8)用电子式表示⑤和⑨元素形成的化合物的形成过程______.
参考答案:由元素在周期表中的位置可知①为H元素,②为C元素,③为N元素,④为F元素,⑤为Na元素,⑥为Al元素,⑦为P元素,⑧为S元素,⑨为Cl元素,⑩为Ar元素,(1)同周期元素从左到右元素的金属性逐渐减弱,非金属性逐渐增强,同主族元素从上到下,元素的金属性逐渐增强,非金属性逐渐减弱,则金属性最强的为Na,非金属性最强的为F,元素的非金属性越强,对应的单质越易与氢气发生反应,则最容易与H2反应单质是F2,
故答案为:Na;F2;
(2)⑤位于周期表中第三周期,ⅠA族,原子核外有3个电子层,最外层电子数为1,则原子结构示意图为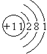 ,
,
故答案为:三;ⅠA; ;
;
(3)最高价氧化物所对应的水化物酸性最强的是HClO4,故答案为:HClO4;
(4)②与⑧形成的化合物为CS2,为共价化合物,故答案为:共价化合物;
(5)最高价氧化物既能与酸反应又能与碱反应的是Al2O3,故答案为:Al2O3;
(6)非金属性N>P,元素的非金属性越强,对应的氢化物越稳定,故答案为:NH3;
(7)同周期元素从左到右元素的原子半径逐渐减小,则原子半径较大的为Na,金属性Na>Al,元素的金属性越强,对应的最高价氧化物的水化物的碱性越强,则碱性较强的为NaOH,
故答案为:Na;NaOH;
(8)⑤和⑨元素形成的化合物为NaCl,用电子表示形成过程为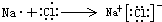 ,故答案为:
,故答案为: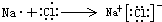 .
.
本题解析:
本题难度 :一般
4、选择题 下列化合物中既含有离子键又含有极性共价键的是
[? ]
A.KBr
B.NaOH
C.HBr
D.N2
参考答案:B
本题解析:
本题难度:简单
5、填空题 已知:①A的简单阴离子核外有2个电子,B元素原子最外层电子数是内层电子数的3倍,E原子基态3p原子轨道上有2个未成对电子,其单质晶体类型属于分子晶体,F元素原子序数为26。
②X、Y和Z为第三周期元素,其原子的第一至第四电离能如下表:
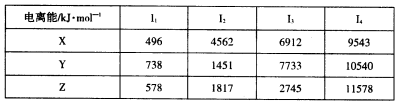
回答下列问题:
(1)B元素原子核外已成对电子数是未成对电子数的____倍。
(2)X、Y、Z的电负性从大到小的顺序为____(用元素符号表示)。
(3)分子式为A2B、A2E的两种物质中?__更稳定(用化学式表示),原因是____。
(4)X的氯化物的熔点比Y的氯化物的熔点____,原因是____。
(5)F的氯化物FCl3与KSCN溶液反应显红色,该反应的离子方程式为____。等电子体指的是原子总数相同.价电子总数相同的分子.离子或基团,据此定义写出离子SCN―的一种等电子体____。
(6)F的一种常见配合物F(CO)3常温下呈液态,熔点为- 20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断F(CO)5的晶体类型为?。F元素的单质晶体在不同温度下有两种堆积方式,晶胞分别如
图所示。在面心立方晶胞中F原子的配位数为____,体心立方晶胞的密度可表示为____。(F的原子半径为r)
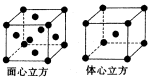
参考答案:

本题解析:依题意可知:A为H,B为O,E为S,F为Fe,X的第一电离能小容易失去一个电子,所以为Na,Y的第三电离能突然增大,表明Y为Mg,同事Z为Al。
(6)小题中的物质溶沸点低,易溶于有机溶剂,所以为分子晶体。
由分摊法计算: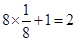 ;该晶胞的质量m=
;该晶胞的质量m=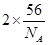 ,设该晶胞的边长为a:则有:
,设该晶胞的边长为a:则有:
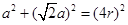 ?解之得:
?解之得: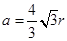
该晶胞的体积: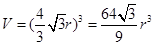
晶胞的密度为: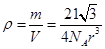
本题难度:一般