| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
�߿���ѧ֪ʶ����ɡ�ԭ���ԭ��������ǿ����ϰ��2017��Ѻ��棩(��)
�ο��𰸣� ��������� �����Ѷȣ�һ�� 3������� ��10�֣���ͼ�е缫a��b�ֱ�ΪAg�缫��P �ο��𰸣���10�֣���1��������2�֣���2��4OH�D�D��e�D ����������� �����Ѷȣ�һ�� 4������� ��4�֣�Ϊ������ɫ��������̼�������Ƽ��������Ϻ��������Ѿ���ʼʹ���й��Լ�������ȼ�ϵ���������ó��������Ϳ����е�����Ϊȼ�ϣ�KOHΪ�������Һ������ʵ���ˡ����ŷš����õ�صĸ�����ӦʽΪ?���������Ƕȷ�����������ȼ�ϵ����ֱ��ȼ�������Ҫ�ŵ���?�� �ο��𰸣���4�֣� H2-2e-+2OH-=2H2O?ȼ�ϵ�ص�����ת��Ч�ʸ� ����������� �����Ѷȣ��� 5��ѡ���� �����й������仯���̵�˵����ȷ���� |
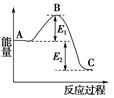
�ο��𰸣�C
���������A���������绹�dz�ϫ���磬���ǽ���е��ת��Ϊ���ܣ�
B����ϡ��Һ������ǿ���ǿ������кͷ�Ӧ�ķ�Ӧ����ֵ����ȣ�Ϊ57.3kj/mol��
D��ʹ�ô��������Խ��ͻ�ܣ�E1���С��������������ϵ���¶ȣ����E1��Ȼ���ֲ��䡣
���������黯ѧ������ʶ����������֪ʶ��
�����Ѷȣ���
|
||
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | ||
| ��һƪ�����л�ѧ֪ʶ���ȫ������������.. | ||
| �����Ŀ |