��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���й���ʵ���������������ȷ���ǣ�������
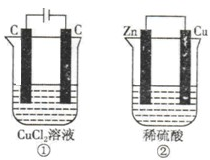
A����ͭƬ����Ƭ������һ�����ϡ�����У�ͭƬ�����������
B������Ƭ����������Ƭ�������������������Һ����Ƭ�������һ����
C����ͭƬ�������Ȼ�����Һ�У���ͭƬ�������һ����
D����п������ʢ��������Թ��У����뼸���Ȼ�ͭ��Һ�����ݷų����ʼӿ�
�ο��𰸣�A��ͭΪ�����������������ӵõ��ӱ���ԭ������������ͭƬ����������ݣ���A��ȷ��
B��Ϊ���װ�ã�����������������ԭ����������B��ȷ��
C��ͭ���Ȼ�������������ԭ��Ӧ�����Ȼ�ͭ���Ȼ������������û���������C����
D��п�û���ͭ���γ�ԭ��ط�Ӧ���绯ѧ��Ӧ�ϻ�ѧ��Ӧ�죬��D��ȷ��
��ѡ��C��
���������
�����Ѷȣ�һ��
2�������� ����ͭ����пƬ��200mlϡ�������ԭ��أ�����ѧ��ת��Ϊ���ܣ���ͭ���Ϲ�����3.36L����״��������ʱ������ǡ��ȫ�������ġ���ش��������⣺
��1����ԭ��ص�������ӦʽΪ��
��2������ԭϡ��������ʵ���Ũ�ȡ�
��3������ͭ��������Ƭ���������ʽ����������ܷ����ԭ����أ� ����ܡ����ܡ����������ԭ��أ���ԭ��صĸ�����Ӧʽ��
�ο��𰸣���1��2H+ + 2e- = H2�� ��2�֣� ��2��0.75mol/L ��3�֣�
��3���ܣ�1�֣���Zn �� 2e- = Zn2+��2�֣�
�����������1����ԭ����нϻ��õĽ�����������ʧȥ���ӣ�����������Ӧ�����Ӿ����ߴ��ݵ������ϣ�������Һ�е��������������ƶ������������ƶ��������õ����ӣ�������ԭ��Ӧ��п��ͭ���ã�п�Ǹ�����ͭ����������Һ�е��������������õ����ӣ���ӦʽΪ2H+ + 2e- = H2����
��2�������������3.36L�����ʵ�����3.36L��22.4L/mol��0.15mol��������ԭ���غ���жϣ���������ʵ���Ҳ��0.15mol����Ũ����0.15mol��0.2L��0.75mol/L ��
��3�����Ļ�����Ҳ����п�ģ������ܹ���ԭ��أ�п���Ǹ������������������и�����ӦʽΪZn �� 2e- = Zn2+��
�����Ѷȣ�һ��
3��ѡ���� ��ͼ��ʾ������ʵ��װ�ã���Һ�������Ϊ200mL����ʼʱ�������Һ��Ũ�Ⱦ�Ϊ0.1mol/L������һ��ʱ���õ����о�ͨ��0.02mol���ӣ����������ε�ˮ�����Һ������仯��������������ȷ���ǣ�������
A�����������������٣���
B����Һ��pH�仯���ټ�С��������
C���缫���������ʵ���������=��
D���缫��Ӧʽ����������2Cl--2e-�TCl2�������и���2H++2e-�TH2��