微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 64.维生素C的结构简式是 ,它的分子式是______________。由于它能防治坏血病,又称为_________________。在维生素C溶液中滴入紫色石蕊
,它的分子式是______________。由于它能防治坏血病,又称为_________________。在维生素C溶液中滴入紫色石蕊 试液,溶液颜色变红,说明维生素C溶液具有__________性;在维生素C溶液中滴入少量蓝色的含有淀粉的碘水,可观察到的现象是______________,说明维生素C具有_______________性。
试液,溶液颜色变红,说明维生素C溶液具有__________性;在维生素C溶液中滴入少量蓝色的含有淀粉的碘水,可观察到的现象是______________,说明维生素C具有_______________性。
参考答案: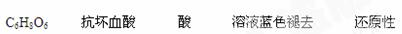
本题解析:略
本题难度:简单
2、选择题 下列说法正确的是
[? ]
A.绿色食品就是指颜色为绿色的食品
B.白色污染是指白色的废弃物的污染
C.有机食品是指含有有机物的食品
D.食盐加碘实质是在食盐中加入KIO3
参考答案:D
本题解析:
本题难度:简单
3、选择题 下列说法中正确是
A.蔗糖和葡萄糖互为同分异构体
B.淀粉、纤维素都是天然高分子化合物
C.在常温下,淀粉遇碘离子变蓝
D.检验蔗糖在稀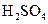 作用下水解的产物,可在水解后的混合溶液中直接加新制
作用下水解的产物,可在水解后的混合溶液中直接加新制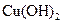 ,加热观察有无砖红色沉淀
,加热观察有无砖红色沉淀
参考答案:B
本题解析:略
本题难度:简单
4、选择题 将Cu片放入0.1mol?L-1FeCl3溶液中,反应一定时间后取出Cu片,溶液中c(Fe3+):c(Fe2+)=2:3,则Cu2+与Fe3+的物质的量之比为
A.3:2
B.3:5
C.3:4
D.4:3
参考答案:C
本题解析:分析:先利用假设法求出二价铁离子、三价铁离子的物质的量,再根据离子方程式中铜离子和二价铁离子的关系求出铜离子的物质的量.
解答:将Cu片放入FeCl3溶液中.发生反应:Cu+2Fe3+=Cu2++2Fe2+,假设溶液中n(Fe2+)=3mol,则溶液中n(Fe3+)=2mol,
由离子方程式可知,n(Cu2+)= n(Fe2+)=
n(Fe2+)= ×3mol=1.5mol,所以n(Cu2+):n(Fe3+)=1.5mol:2mol=3:4,
×3mol=1.5mol,所以n(Cu2+):n(Fe3+)=1.5mol:2mol=3:4,
故选C.
点评:本题考查的是铜的化学性质、离子方程式的有关计算,巧妙利用假设法是解本题的关键.
本题难度:困难
5、选择题 将某种金属卤化物和浓硫酸在烧瓶中加热后,可得无色卤化氢气体(无其他杂质气体),则该金属卤化物为.
A.氟化物
B.氯化物
C.溴化物
D.碘化物
参考答案:B
本题解析:由于采用了浓硫酸,则不可能制取HBr和HI,HBr和HI会被浓硫酸氧化,否则卤化氢中必定混有杂质.反应在玻璃器皿(烧瓶)中制取,不可能是制取HF,因为HF易腐蚀玻璃.
本题难度:简单