微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (11分)已知A、B、C、D、E是短周期中的五种非金属元素,它们的原子序数依次增大。A元素原子形成的离子核外电子数为零,C、D在元素周期表中处于相邻的位置,B原子的最外层电子数是内层电子数的2倍。E元素与D元素同主族;E的单质为黄色固体,易溶于二硫化碳。
(1)请写出元素符号: B___________、D___________。
(2)画出E的阴离子的结构示意图 ______________________。
(3)A的单质和C的单质在一定条件下反应生成化合物X,用电子式表示化合物X的形成过程:____________________________? _______。向X的水溶液中滴入酚酞溶液,会观察到什么现象:_________________________。
参考答案:(1)C? O?(2)? ?
?
(3)略?显红色
本题解析:略
本题难度:简单
2、填空题 下列A~G均是中学常见化合物,它们之间有如图的转化关系(部分反应物或生成物略去),已知B为一种气体,E、F、G三种化合物中均含有同一种元素M,且价态互不相同。请回答下列问题。
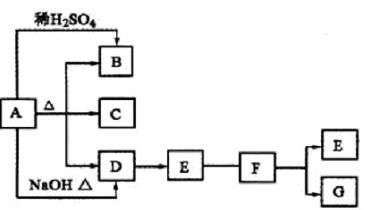
(1)M元素为____________。
(2)B是_________或_________,写出两种鉴别它们的方法________;____________。
(3)若A与G反应也能制B,且反应中n(A):n(G)=1:2,则此时该反应的离子方程式是________________________。
(4)若B与F在一定条件下反应生成一种化合物和一种单质,该反应的化学方程式为________________________。
参考答案:
(1)N或氮(3分)
(2)SO2; CO2(每空1分,共2分);将B通入品红溶液,如溶液退色,则为SO2,如不褪色,则为CO2;将B通入酸性KMnO4溶液中,如褪色,则为SO2,如不褪色,则为CO2;(每空2分,共4分)(其他合理答案也给分)
(3)2H++CO2-3 =CO2↑+H2O(3分,答出生成SO2的反应不得分)
(4)2NO2+4SO2=N2+4SO3(3分)
本题解析:略
本题难度:一般
3、选择题 下列物质不能使品红溶液褪色的是?(?)
A.氯气
B.硫化氢
C.二氧化硫
D.过氧化钠
参考答案:B
本题解析:略
本题难度:简单
4、简答题 A、B、C、D、E、F六种物质的相互转化关系如右图所示(反应条件及部分产物未列出).
(1)若A是常见金属单质,与B的水溶液反应生成C和D.D、F是气体单质,D在F中燃烧时发出苍白色火焰.则反应②(在水溶液中进行)的离子方程式为______.
(2)若A、D为短周期元素组成的固体单质,一种为金属,另一种为非金属.且③④两个反应都有红棕色气体生成,则反应④的化学方程式为______.
(3)若A是黑色固体,D是有臭鸡蛋气味的气体,E溶液中滴加KSCN溶液呈血红色.则D的电子式是______;工业上生产B的第一个生产阶段是煅烧与A含相同元素的矿石,其化学方程式是______,使用的设备是______.
(4)若B是由地壳中含量最高的两种元素组成,A的一种同素异形体与B、D属同一种类型的晶体,则反应①的化学方程式是______,B与烧碱溶液反应的化学方程式是______.
参考答案:(1)D、F是气体单质,D在F中燃烧时发出苍白色火焰,应是在中的燃烧反应,则D、F应分别为H2、Cl2,B为HCl,A应为Fe,C为FeCl2,E为FeCl3,反应②为FeCl2被氧化生成FeCl3的反应,离子方程式为2Fe2++Cl2=2Fe3++2Cl-,
故答案为:2Fe2++Cl2=2Fe3++2Cl-;
(2)A+B=C+D是置换反应,若A、D为短周期元素单质,且A为固体金属单质,D为固体非金属单质,③和④两个反应中都有红棕色气体生成,非金属单质D为C,F为浓硝酸,金属置换非金属单质的反应应为镁和二氧化碳反应生成氧化镁和碳的反应,判断A为Mg;B为CO2;C为MgO;D为C;E为Mg(NO3)2;F为NHO3,
浓HNO3与C反应的化学方程式为C+4HNO3(浓)?△?.?CO2↑+4NO2↑+2H2O,
故答案为:C+4HNO3(浓)?△?.?CO2↑+4NO2↑+2H2O;
(3)若A是黑色固体,D是有臭鸡蛋气味的气体,应为H2S,电子式为

,E溶液中滴加KSCN溶液呈血红色,说明来源:91考试网 www.91eXam.orgE溶液中含有Fe3+,A应为FeS2,F应为氧化性酸,可为HNO3,则B为H2SO4,FeS2与O2的反应为工业制备硫酸的重要反应,在沸腾炉中进行,反应的方程式为4FeS2+11O2?△?.?2Fe2O3+8SO2,
故答案为:

;?4FeS2+11O2?△?.?2Fe2O3+8SO2;沸腾炉;
(4)B是由地壳中含量最高的两种元素组成,应为SiO2,为原子晶体,则A应为C,D为Si,C为CO,F为O2,E为CO2,
反应①的化学方程式是2C+SiO2?△?.?Si+2CO↑,SiO2可与烧碱反应,方程式为SiO2+2NaOH=Na2SiO3+H2O,
故答案为:2C+SiO2?△?.?Si+2CO↑;?SiO2+2NaOH=Na2SiO3+H2O.
本题解析:
本题难度:一般
5、实验题 10已知A、B、D、E均为中学化学常见单质及化合物,它们之间的转化关系如图所示(部分产物略去)

(1)若A和E均为单质且B物质为极性键形成的非极性分子。B的结构式为____。
(2)若A为可溶性强碱(MOH),E为同主族元素形成的常见非金属化合物,且该化合物中两种元素的质量比为1:1,试写出A到B的化学方程式______。
(3)若取B的溶液装于试管,向溶液中滴加KSCN溶液,无明显现象,再滴加稀盐酸,产生红色溶液,则用化学方程式表示工业制备E化学原理______;D的溶液中含有少量B,用离子方程式表示除杂方法_______。
参考答案:(1)O="C=O" (2分)? (2) MOH+SO2==MHSO3(2分)
高温
本题解析:略
本题难度:一般