微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法中正确的是
A.氧化还原反应中一定有化合价的升降
B.有氧元素参加的反应一定是氧化还原反应
C.氧化剂在反应中失去电子
D.还原剂在反应中化合价升高,被还原
参考答案:A
本题解析:本题考查同学们对基本概念的掌握情况,A项可根据氧化还原反应的特征:有化合价的升降加以判断,为正确选项.B项明显不符合“氧化还原反应中有电子转移”的观点,错误.C项中,氧化剂在反应中应得到电子而被还原,故也不正确.D项中,还原剂在反应中化合价确实升高,但发生的是氧化反应,被氧化.故D项也错误,故选A项.
本题难度:困难
2、选择题 将Cu片放入0.1mol・L-1FeCl3溶液中,反应一定时间后取出Cu片,溶液中c(Fe3+):c (Fe2+)=2:3,则Cu2+与Fe3+的物质的量之比为
[? ]
A.3:2
B.3:5
C.3:4
D.4:3
参考答案:C
本题解析:
本题难度:简单
3、选择题 用0.1 mal/L的Na2SO3溶液30 mL,恰好将2×10-3mol的XO4-还原,则元素X在还原产物中的化合价
[? ]
A.+1
B.+2
C.+3
D.+4
参考答案:D
本题解析:
本题难度:简单
4、填空题 在Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O反应中
(1)______元素被氧化,______是氧化剂.
(2)用双线桥标出该反应电子转移的方向和数目.Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O
(3)若有2.4mol的H2SO4参与反应,则被还原的H2SO4为______g.
参考答案:(1)Cu+2H2SO4(浓)△.CuSO4+SO2↑+2H2O中,铜元素的化合价由0价→+2价,失电子被氧化,硫元素的化合价由+6价→+4价,所以硫酸得电子作氧化剂,故答案为:铜;硫酸;
(2)铜失电子数=1(2-0)=2,硫酸得电子数=1(6-4)=2,该反应中转移电子数是2,用用双线桥标出该反应电子转移的方向和数目为: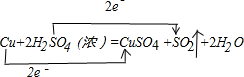 ,故答案为:
,故答案为: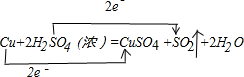 ;
;
(3)该反应中有一半的硫酸是氧化剂,一半的硫酸起酸的作用,所以若有2.4mol的H2SO4参与反应,则被还原的H2SO4的物质的量是1.2mol,其质量=1.2mol×98g/mol=117.6g,
故答案为:117.6.
本题解析:
本题难度:一般
5、选择题 24?mL0.05?mol・L-1的Na2SO3溶液恰好与40?mL?0.02?mol・L-1的K2RO4酸性溶液反应生成硫酸钠,则元素R在还原产物中的价态是
A.+6
B.+3
C.+2
D.0
参考答案:B
本题解析:二者的物质的量之比为3:2,其中S元素化合价自+4升至+6,而R在K2RO4中的化合价为+6价,根据化合价升降相等可求得R在还原产物中的价态是+3
本题难度:困难