��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� wg���ۺ����۵Ļ���������?NaOH��Ӧ��Ȼ����ˣ���������ȫ�ռ����������м��ȣ�ֱ�������ȵ������������ٱ仯��ȡ���������е����ʳ�����Ϊwg����ԭ����������۵����������ǣ�������
A��30%
B��50%
C��70%
D��90%
�ο��𰸣�wg���ۺ����۵Ļ���������NaOH��Ӧ��Ȼ����ˣ�����ΪFe��
��������������ȫ���պ�����Ӧ����Fe2O3��
ȡ���������е����ʳ�����Ϊwg��
�����۵���������Fe2O3��OԪ�ص�������
����ԭ����������۵���������Ϊ��3��163��16+2��56��100%=30%��
��ѡA��
���������
�����Ѷȣ���
2��ѡ���� ijͬѧ��һ��������ɰֽ��ϸ��ĥ����ȥ����ı���Ĥ��������ǯ��ס���ھƾ��ƻ����ϼ������ۻ��������ۻ������������䣬���Ǻ�����һ��Ĥ���š�������˵��������ǣ�������?
A������Һ������Ĥ��������
B����ʵ��˵�������������۵���������۵�
C��������������е�������Ӧ�ڱ����γ������ﱣ��Ĥ
D�����Ļ�ѧ���ʽ��ȶ�����ʹ���ȵ��ۻ�Ҳ��������е�������Ӧ
�ο��𰸣�D
��������� ��������������Ӧ���ڱ������γ������������۵���������۵㣬�ʼ���ʱ���ۻ�����������䡣
�������������仯��������Ҫ�����������߿����ص㡣�����ڱ���������Ӧע����۸����ʵ����ʼ���Ҫ�Ļ�ѧ��Ӧ��
�����Ѷȣ���
��Դ:91������ 91Exam.org 3��ѡ���� ��14�֣������������Ի������Һ�о�����NO3������������ԭ��Ӧ��ת����ϵ����ͼ��ʾ��
 ��
��
���У�����D��F��Ӧ�������Σ�����D��A��Һ��Ӧ���ɰ�ɫ������
��ش��������⣺��
��1����Al��ϡ���ᷴӦʱ��ϡ������ֵ���������������������������
A��ֻ����ǿ������?
B��ֻ��������
C��ͬʱ����ǿ�����Լ�����
D��������ǿ�����Ի������˻�ԭ��
��2�����������ӷ���ʽ�ĺ�������д����Ļ�ѧʽ������Ҫ��ƽ��
������Al + NO3��+ OH��+ H2O��������������+����������
��3������D��ˮ��Һ��A��Һ��Ӧ�����ӷ���ʽ����������?��������
��4��D����C��Ӧ�Ļ�ѧ����ʽ��?
��5��C��E��������л���ɴ�����Ⱦ���ڴ��������£�D���Խ�C��Eת��Ϊ������̬���ʣ��õ�������������������
��6����ȥC�е�E�������ʿ��õĻ�ѧ�����ǣ����û�ѧ����ʽ��ʾ��?
��7��Al��NO3�������������·�Ӧ��Al�뱻��ԭ��NO3�������ʵ���֮��������?��������
�ο��𰸣�(16�֣�ÿС��2��)
��1����C��
��2����AlO2����+����NH3 ��
��3����3NH3��H2O��+ Al3+ ="=" Al(OH)3��+3 NH4+?��
��4��? 4 NH3 +5O2 ="=" 4NO + 6 H2O
��5����N2����
��6��? 3NO2 + H2O ="=" 2HNO3 + NO?
��7��? 1:1
���������
�����������Ի������Һ�о�����NO3������������ԭ��Ӧ������ͼʾ��Ϣ��֪�������Ի����£���Ӧ�������κ�һ�����������Ի���������ƫ�����κͰ�����������������������һ��������ˮ��һ���������Ժ�������Ӧ���ɶ�����������AΪ��������BΪƫ�����Σ�CΪNO��DΪ������EΪ����������FΪ���ᣮ
��1��Al��4HNO3=Al(NO3)3��NO����2H2O,HNO3�еĵ����ֱ�ۣ�ͬʱ����ǿ�����Լ����ԣ�ѡC���ʴ�Ϊ��C��
��2����ԭ���غ�͵�ʧ�����غ�ã���������������AlO2�D��ʽ���ڣ�������������������һ��������ˮ���ʴ�Ϊ����AlO2����+����NH3 ��
�ǹ����İ�ˮ�����ܽ�Al(OH)3����3NH3��H2O��+ Al3+ ="=" Al(OH)3��+3 NH4+������Ӧ��������������ɫ�������ʴ�Ϊ����3NH3��H2O��+ Al3+ ="=" Al(OH)3��+3 NH4+
��4��D����C��Ӧ�Ļ�ѧ����ʽ����������������һ��������ˮ4 NH3 +5O2 ="=" 4NO + 6 H2O�ʴ�Ϊ��4 NH3 +5O2 ="=" 4NO + 6 H2O
��5��6NO��4NH3=5N2��6H2O,8NH3��6NO2=5N2��12H2O��������ΪN2, �ʴ�Ϊ����N2��
�ʿ�����ˮϴ����3NO2 + H2O ="=" 2HNO3 + NO���ʴ�Ϊ��3NO2 + H2O ="=" 2HNO3 + NO
��Al��NO3�������������·�Ӧ��������������Ϊ���۵������ӣ�ʧȥ����3mol�����������ԭΪһ���������õ�����Ҳ��3mol�����ݵ����غ㣬Al�뱻��ԭ��NO3�������ʵ���֮����1��1���ʴ�Ϊ��1��1��
�����Ѷȣ�һ��
4�������� ��12�֣���ʽ̼����þ[MgaAlb(OH)c(CO3)d��x?H2O]������������ȼ����
��1����ʽ̼����þ������ȼ���ã������������ȷֽ������մ���������?��
��2��MgaAlb(OH)c(CO3)d��x?H2O��a��b��c��d�Ĵ�����ϵʽΪ?��
��3��Ϊȷ����ʽ̼����þ����ɣ���������ʵ�飺
��ȷ��ȡ3.390g��Ʒ������ϡ�����ַ�Ӧ������CO20.560L���ѻ���ɱ�״���£�������ȡһ������Ʒ�ڿ����м��ȣ���Ʒ�Ĺ�������ʣ�������Ʒ��ʣ������/������Ʒ����ʼ������100%�����¶ȵı仯����ͼ��ʾ����Ʒ��2700Cʱ����ȫʧȥ�ᾧˮ��6000C���ϲ�������Ϊ����������Ļ�����
��������ʵ�����ݼ����ʽ̼����þ��Ʒ�е�n(OH��): n(CO32��)��д��������̣���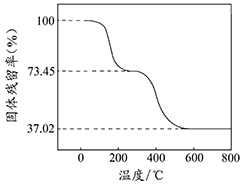
�ο��𰸣�
��ֹȼ��
2a+3b=c+2d
��3��

���������(1�����ȷֽ�Ϊ���۵������þ�������������ڿ�ȼ����棬��ֹȼ�գ���2�������и�Ԫ�صĺϼ۴�����Ϊ0��2a+3b=c+2d����3�����ݷֽ�ͼ�����֪��Ϣ���ó���һ����ʧȥ�ᾧˮ���ڶ����Ƿֽ�Ϊ�����Ӧ���ݺ�һ�μ���OH-��CO32-�Ĺ�ϵ������ʱǰ������ˮ���������ɶ�����̼�����ߵĺͿ��Ը���ͼ�е����ݻ��㣬�ٸ��ݶ�����̼�����������ˮ�������������õ�OH-��CO32-�����ʵ�����
�����Ѷȣ�һ��
5�������� ��þ�ۺ�̼��þ�Ļ�����������������գ�ֱ���������ٸı�Ϊֹ�����ⶨ�����պ����ù���������ԭ�����������ͬ����ԭ�������þ�ۺ�̼��þ�������ȡ�
�ο��𰸣�11��14
���������������Ŀȫ������������û��һ���ɹ�ֱ�����õľ������ݡ���ϸ�������⣬ץס�ؼ�����������պ����ù���������ԭ�����������ͬ��ת��Ϊ��������Ϊ��¶����Mg���յ�O2��������MgCO3�ֽ�ų���CO2��������������2Mg��O2��MgCO3��CO2������44Mg��16MgCO3����һ��ϵʽ��������ԭ�������þ����̼��þ����������44��24��16��84��11��14��
�����Ѷȣ���