��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����������ȷ����(? )
A��ͬһԪ�ز����ܼȱ��ֽ����ԣ��ֱ��ַǽ�����
B���Ȼ�������ˮ�ܵ��磬��Һ̬�Ȼ��ⲻ�ܵ���
C��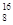 O��
O�� O��
O��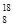 O��Ϊͬλ�أ���������Ԫ�أ���������ȫ��ͬ
O��Ϊͬλ�أ���������Ԫ�أ���������ȫ��ͬ
D��������ǿ����Һ�������ƶ���������Ŀһ���ȵ�����������Һ�������ƶ���������Ŀ��
�ο��𰸣�B
���������A����Ԫ�ؾͼȱ��ֽ����ԣ��ֱ��ַǽ�����
B:��ȷ
C��ͬλ�ص��������ʲ�ͬ
D����Һ����������Һ��Ũ�ȡ����ʵĵ���̶ȡ��ƶ�����������ɶ��پ��й�
��ΪB
�����Ѷȣ���
2��ѡ���� ʵ�ʴ��ڵ�11H��12H��13H ��H+��H2��������
A���������ͬλ��
B����Ԫ�ص����ֲ�ͬ��
C��������ֺ���
D��������Ԫ��
�ο��𰸣�B
���������A��11H��12H��13H��ͬλ�أ������ֲ��ǣ�����B�����ֺ��ء����Ӻͷ��ӣ����ֲ�ͬ������ȷ��C������D����������Ԫ����ɣ�����
�����Ѷȣ�һ��
3������� ��8�֣���A��B��C��D��E 5��Ԫ�أ����ǵĺ˵�������������Ҷ�С��20������C��E�ǽ���Ԫ�أ�A��E��ͬһ�壬����ԭ�ӵ����������Ų�Ϊns1��B��DҲ��ͬһ�壬����ԭ��������p�ܼ���������s�ܼ���������������Cԭ��������ϵ���������Dԭ��������ϵ�������һ�롣��ش��������⣺
��1����������Ԫ����ɵ�һ�ֻ������ǣ�д��ѧʽ��__________________��
��2��д��CԪ�ػ�̬ԭ�ӵĵ����Ų�ʽ______________________________ ��
��3���õ����Ų�ʽ����ʽ��ʾBԪ��ԭ�ӵļ۵��ӹ���_______________��
��4��Ԫ��B��D�ĵ縺�ԵĴ�С��ϵ��___________��C��E�ĵ�һ�����ܵĴ�С��ϵ��________________������Ԫ�ط��ź͡�������ʾ��
��5��DB2����?�����ɵ�?������ԡ��Ǽ��ԡ� �����ӣ�
���ӿռ乹����?��
�ο��𰸣���1��KAl(SO4)2?12H2O��1�֣�?��2��1s22s22p63s23p1 ��1�֣�?��3��2s22p4 ?��1�֣�
��4��O��S? Al��K ��2�֣�?��5�����ԣ����ԣ� V�ͣ�3�֣�
�������������Ԫ�صĽṹ���й����ʿ�֪��A��B��C��D��E 5��Ԫ�طֱ���H��O��Al��S��K��
��1����������Ԫ����ɵ�һ�ֻ�����Ӧ������������ѧʽΪKAl(SO4)2?12H2O��
��2�����ݹ���ԭ����֪��AlԪ�ػ�̬ԭ�ӵĵ����Ų�ʽΪ1s22s22p63s23p1 ��
��3�����ݹ���ԭ����֪����Ԫ��ԭ�ӵļ۵��ӹ�����2s22p4��
��4���ǽ�����Խǿ���縺��Խ����Ԫ�صķǽ�����������Ԫ�صģ�������Ԫ�صĵ縺�Դ�����Ԫ�صġ�������Խǿ����һ������ԽС�����Ľ���������K�ģ����Ե�һ��������Al��K��
��5�����ݼ۲���ӶԻ������ۿ�֪��SO2��Sԭ�ӵŶԵ��Ӷ����ǣ�6��2��2����2��1������SO2�Ǻ��м��Լ��ļ��Է��ӣ��ռ乹����V�͡�
�����Ѷȣ�һ��
4��ѡ���� X��Y��Z���ֶ�����Ԫ�������ڱ��е�λ����ͼ��ʾ��Yԭ�ӵ������������Ǵ�����������3��������˵����ȷ����

A����̬�⻯��ķе㣺Z��Y
B��ZԪ�ص��������Ӧ��ˮ����һ����һ��ǿ��
C������Ԫ��ԭ�Ӱ뾶�Ĵ�С˳��Ϊ�� X��Y��Z
D��Z������Fe��Ӧ���ɵĻ������У���Ԫ����+3��
�ο��𰸣�A
������������ݶ�����Ԫ�������ڱ��е����λ�ÿ�֪��Y��XӦ���ǵڶ�����Ԫ�ء�Yԭ�ӵ������������Ǵ�����������3����ʵ��YӦ������Ԫ�أ���X�ǵ�Ԫ�أ�Z��SԪ�ء�A������ˮ���Ӽ�������������ˮ�ķе����H2S�ķе㣬A��ȷ��B��������ǿ�ᣬ�������������ᣬB����ȷ��C��ͬ������������ԭ�Ӱ뾶��С��ͬ�������϶���ԭ�Ӱ뾶��������������Ԫ�ص�ԭ�Ӱ뾶��С˳����Z��X��Y��C����ȷ��D���������������ɵ����Ȼ�����FeS���ò�����3������D����ȷ����ѡA��
�����Ѷȣ�һ��
5��ѡ���� ������Ϊ���ڵ�IA�����Ԫ��Ҳ���Է������������У������й�˵������ȷ����
A��������Ԫ���ٵ�һ�������γ��ȶ��ṹ���Է��ڵڢ�A��
B��������Ԫ�ؿ�������Ԫ���γ����ӻ�����NaH�����Է��ڢ�A��
C����Ԫ��Ӧ���ڷ�Ԫ�ص��ϱ�
D��������Ԫ���������������۵ľ���ֵ��ȿ��Է��ڢ�A��
�ο��𰸣�C
���������±��Ԫ������������Ϊ7���õ�һ����Ϊ�ȶ��ṹ���γɸ�һ�������ӣ�����Ԫ��ԭ�������ֻ��һ�����Ӳ㣬һ�����ӣ��õ�һ������Ҳ�γ�����ȶ��ṹ����NaH��±��Ԫ�ش��ϵ��·ǽ���������������Ԫ�طǽ�����ǿ�����ԣ���Ԫ�طǽ����Խ������������ڷ�Ԫ���Ϸ���C����
�����Ѷȣ�һ��