|
高中化学必备知识点《原电池原理》答题技巧(2017年最新版)(四)
2017-07-10 17:43:59
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列叙述正确的是( )
A.K与N连接时,X为硫酸,一段时间后溶液的pH增大
B.K与N连接时,X为氯化钠,石墨电极反应:2H++2e-=H2↑
C.K与M连接时,X为硫酸,一段时间后溶液的pH增大
D.K与M连接时,X为氯化钠,石墨电极反应:4OH--4e-=2H2O+O2↑
| 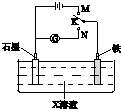
参考答案:A.K与N连接时,X为硫酸,该装置是原电池,铁作负极,石墨作正极,负极上铁失电子生成亚铁离子,正极上氢离子放电生成氢气,导致溶液中氢离子浓度降低,所以一段时间后溶液的pH增大,故A正确;
B.K与N连接时,X为氯化钠,该装置是原电池,铁作负极,石墨作正极,石墨上氧气得电子发生还原反应,电极反应式为:2H2O+O2+4e-=4OH-,故B错误;
C.K与M连接时,X为硫酸,该装置是电解池,石墨作阳极,铁作阴极,阳极上氢氧根放电,阴极上氢离子放电,实际上电解的是水,硫酸的物质的量不变,所以硫酸浓度增大,溶液的pH减小,故C错误;
D.K与M连接时,X为氯化钠,该装置是电解池,石墨作阳极,铁作阴极,阳极上氯离子放电,所以阳极上的电极反应式为:2Cl--2e-=Cl2↑,故D错误;
故选A.
本题解析:
本题难度:简单
2、填空题 (18分)能源的开发和利用是当前科学研究的重要课题。
(1)利用二氧化铈(CeO2)在太阳能作用下前实现如下变废为宝的过程:
mCeO2 (m-x)CeO2 (m-x)CeO2 xCe+xO2 xCe+xO2
(m-x)CeO2 xCe+xH2O+xCO2 xCe+xH2O+xCO2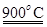 mCeO2+xH2+xCO mCeO2+xH2+xCO
上述过程的总反应是 ,该反应将太阳能转化为 。
(2)CO、O2和KOH溶液构成的燃料电池的负极电极反应式为 。该电池反应可获得K2CO3溶液,某温度下0.5mol L-1 K2CO3溶液的pH=12,若忽略CO32-的第二级水解,则CO32- +H2O L-1 K2CO3溶液的pH=12,若忽略CO32-的第二级水解,则CO32- +H2O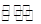 HCO3-+OH-的平衡常熟Kh= 。 HCO3-+OH-的平衡常熟Kh= 。
(3)氯碱工业是高耗能产业,下列将电解池与燃料电池相组合的工艺可以节能30%以上。
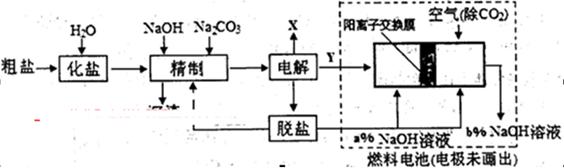
①电解过程中发生反应的离子方程式是 ,阴极附近溶液PH (填“不变”、“升高”或“下降”)。
②如果粗盐中SO42-含量较高,精制过程需添加钡试剂除去SO42-,该钡试剂可选用下列试剂中的 。
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
现代工艺中更多使用BaCO3除SO42-,请写出发生反应的离子方程式 。
③图中氢氧化钠溶液的质量分数a% b%(填“>”、‘‘=”或“<”),,燃料电池中负极上发生的电极反应为 。
参考答案:(18分)
(1)H2O + CO2 =H2 + CO + O2(2分) 化学能(1分)
(2)CO
本题解析:
本题难度:一般
3、填空题 (5分)21世纪最富有挑战性的课题之一是使汽油氧化直接产生电流,新研制的某汽油燃料电池的一个电极通入空气,另一个电极通入汽油蒸气,填写下列空格。
(1)汽油燃料电池的能量转换形式是将________能直接转化为______能。
(2)通入空气的那个电极是燃料电池_________极(选填“正”或“负” )该电极上若有
32g O2参加反应,则反应过程中转移了_________mol e-
参考答案:(共5分)
(1)化学能 电能 (2)正极 4 (2分,其余各1分)
本题解析:略
本题难度:一般
4、选择题 下列有关化学电源电极的叙述不正确的是( )
A.锌锰碱性电池的负极材料为锌
B.铅蓄电池的负极材料为铅
C.镍镉电池的负极材料为镍
D.锂电池的负极材料为锂
参考答案:A.锌锰碱性电池中,锌易失电子作负极,电极反应式为Zn-2e-=Zn 2+,故A正确;
B.铅蓄电池放电时,铅易失电子作负极,电极反应式为:Pb(s)+SO42-(aq)-2e-=PbSO4(s),故B正确;
C.放电时的反应方程式:Cd+2NiO(OH)+2H2O=2Ni(OH)2+Cd(OH)2,Cd失电子而作负极,故C错误;
D.锂电池中,锂易失电子而作负极,电极反应式为:4Li-4e-=4Li+,故D正确,
故选C.
本题解析:
本题难度:一般
5、填空题 原电池是一种___________?_____________装置。电子表所用的某种钮扣电池的电极材料为Zn和Ag2O,电解质溶液为KOH,其电极反应式为:
Zn+2OH--2e-=ZnO+H2O ? Ag2O+H2O+2e-=2Ag+2OH-
电池的负极是_____?_______,正极发生的是_______?_____反应(填反应类型),总反应式为_______________?____________________。
参考答案:将化学能转化成电能的? Zn?还原反应? Zn+Ag2O=2Ag+ZnO
本题解析:考查原电池的概念以及电极反应式的书写。原电池是一种把化学能转化为电能的装置,在原电池较活泼的金属作负极,失去电子,发生氧化反应。正极得到电子,发生还原反应。所以根据电极反应式可判断,锌是负极,氧化银是正极。正负极电极反应式想叠加,就是总反应式,所以总反应式为Zn+Ag2O=2Ag+ZnO。
本题难度:一般
| 