|
|
|
高考化学知识点整理《水的电离平衡》高频试题巩固(2017年最新版)(十)
2017-07-10 17:45:26
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 室温时,柠檬水溶液的pH是3,其中的c(OH-)是
A.0.1 mol/L
B.1×10-11 mol/L
C.1×10-7 mol/L
D.1×10-3 mol/L
|
参考答案:B
本题解析:柠檬水溶液的pH是3,则氢离子浓度是0.001mol/L,则根据水的离子积常数可知,溶液中c(OH-)=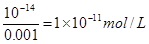 ,答案选B。 ,答案选B。
考点:考查溶液中离子浓度的有关计算
点评:在计算溶液中OH-浓度时,应该充分利用好水的离子积常数和pH的定义式。
本题难度:一般
2、填空题 (16分)雾霾含有大量的污染物SO2、NO。工业上变“废”为宝,吸收工业尾气SO2和NO,可获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素):

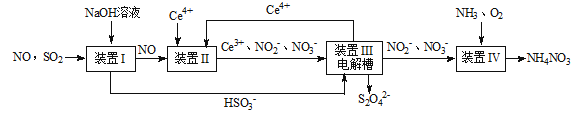
(1)装置Ⅰ中的主要离子方程式为 。
(2)含硫各微粒(H2SO3、HSO3-和SO32-)存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数X(i)与溶液pH的关系如图所示。

①若是0.1molNaOH反应后的溶液,测得溶液的pH=8时,溶液中各离子浓度由大到小的顺序是 。
②向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因: 。
(3)写出装置Ⅱ中,酸性条件下反应的离子方程 式 , 。
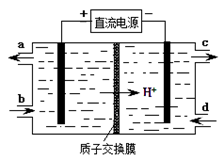
(4)装置Ⅲ还可以使Ce4+再生,其原理如图所示。①生成Ce4+从电解槽的 (填字母序号)口流出。②写出阴极的反应式 。
(5)已知进入装置Ⅳ的溶液中,NO2-的浓度为a g・L-1,要使1 m3该溶液中的NO2-完全转化为NH4NO3,需至少向装置Ⅳ中通入标准状况下的O2 L。(用含a代数式表示,计算结果保留整数)
参考答案:(1)SO2+OH-=HSO3-
(2)①c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)>c(H+);②因为亚硫酸氢根离子存在电离平衡HSO3- H++ SO32-,加入氯化钙后,Ca2++ SO32-= CaSO3↓,使平衡正向移动,氢离子浓度增大,pH减小; H++ SO32-,加入氯化钙后,Ca2++ SO32-= CaSO3↓,使平衡正向移动,氢离子浓度增大,pH减小;
(3)NO+3Ce4++2H2O=NO3-+ 3Ce3++4 H+, NO+Ce4++H2O=NO2-+ Ce3++2 H+;
(4)a;2HSO3-+2e-+2H+= S2O42-+2H2O;
(5)243a或5600a/23
本题解析:(1)根据流程图可知,二氧化硫与NO的混合气体与氢氧化钠溶液反应主要生成亚硫酸氢钠,所以装置Ⅰ中的主要离子方程式为SO2+OH-=HSO3-;
(2)①由图可知,pH=8时溶液中主要的阴离子是亚硫酸根离子,说明二氧化硫与氢氧化钠溶液反应主要生成亚硫酸钠,其次还有少量的亚硫酸氢钠,则溶液中离子浓度的大小关系是c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)>c(H+);
②向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中出现浑浊,pH降为2,溶液的酸性增强,因为亚硫酸氢根离子存在电离平衡HSO3- H++ SO32-,钙离子与亚硫酸根离子结合为亚硫酸钙沉淀,促进亚硫酸氢根离子的电离,氢离子浓度增大,pH减小; H++ SO32-,钙离子与亚硫酸根离子结合为亚硫酸钙沉淀,促进亚硫酸氢根离子的电离,氢离子浓度增大,pH减小;
(3)装置II是Ce4+与NO的反应,将NO氧化为硝酸根离子和亚硝酸根离子,自身被还原为Ce3+,离子方程式是NO+3Ce4++2H2O=NO3-+ 3Ce3++4 H+, NO+Ce4++H2O=NO2-+ Ce3++2 H+;
(4)装置Ⅲ还可以使Ce4+再生,则Ce3+被氧化为Ce4+,阳极发生氧化反应,所以Ce4+从电解槽的a口流出;阴极发生还原反应,根据流程图可知,HSO3-得到电子生成S2O42-,则电极反应式是2HSO3-+2e-+2H+= S2O42-+2H2O;
(5)NO2-与氨气、氧气反应生成硝酸铵,则N元素被氧化,化合价从+3价升高到+5价,1m3的溶液中的NO2-的物质的量是1000L×ag/L/46g/mol=1000a/46mol,失去电子的物质的量是1000a/46×2mol=,根据得失电子守恒,则需要氧气在标准状况下的体积是1000a/23mol/4×22.4L/mol=5600a/23L。
考点:考查电解质溶液中离子浓度的关系,对流程的分析,氧化还原反应的分析判断
本题难度:困难
3、选择题 水是一种极弱的电解质,在室温下水的电离常数为1.8×10-16,若平均每n个水分子只有一个水分子能电离,则n是
[? ]
A.1×10-4
B.55.6×107
C.1×107
D.6.02×1021
参考答案:B
本题解析:
本题难度:一般
4、选择题 下列溶液,按 由小到大顺序排列的是 由小到大顺序排列的是
① 溶液 ② 溶液 ② 溶液 溶液
③ 溶液 ④ 溶液 ④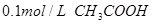 溶液 溶液
A.①②④③
B.②①④③
C.③④①②
D.④③②①
|
参考答案:B
本题解析:酸中C(H+)越大,溶液的pH就越小。①是一元强酸,②是二元强酸,④是一元弱酸,③是一元强碱。当酸的浓度相等时,二元强酸的氢离子的浓度大于一元强酸的,一元强酸的大于一元弱酸的,碱中的氢离子浓度最小,因此C(H+)由大到小的顺序是②①④③ ,所以pH由小到大顺序排列②① ④ ③,选项是B。
考点:考查溶液中的pH 的大小排列顺序的知识。
本题难度:一般
5、选择题 用0.10 mol・L-1的盐酸滴定0.10 mol・L-1的氨水,滴定过程中不可能出现的结果是
A.c(NH4+) > c(Cl-),c(OH-) > c(H+)
B.c(Cl-) > c(NH4+),c(OH-) > c(H+)
C.c(NH4+) = c(Cl-),c(OH-) = c(H+)
D.c(Cl-) > c(NH4+),c(H+) > c(OH-)
参考答案:B
本题解析:用0.10 mol・L-1的盐酸滴定0.10 mol・L-1的氨水,当滴入盐酸量小于氨水时,c(NH4+) > c(Cl-),c(OH-) > c(H+);当滴入盐酸量等于氨水时c(NH4+) = c(Cl-),c(OH-) = c(H+);当滴入盐酸量大于氨水时,c(Cl-) > c(NH4+),c(H+) > c(OH-),故B错误。
考点:中和滴定
本题难度:一般