��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� һ���¶��£����ܱ������г���1.0molN2��3.0molH2����Ӧ�ﵽƽ��ʱ���NH3�����ʵ���Ϊ0.6mol�����ڸ������п�ʼʱ����2.0 molN2��6.0molH2����ƽ��ʱNH3�����ʵ���Ϊ?
�١���Ϊ����������n(NH3)=1.2mol? �ڡ���Ϊ����������n(NH3)>1.2mol
�ۡ���Ϊ��ѹ������n(NH3)=1.2mol? �ܡ���Ϊ��ѹ������n(NH3)<1.2mol
A��ֻ�Тڢ�
B��ֻ�Т٢�
C��ֻ�Т٢�
D��ֻ�Тڢ�
�ο��𰸣�A
�����������Ϊ����������������൱������ǰ�ߵĻ���������ѹǿ��ƽ��������Ӧ�����ƶ������������ʵ�������1.2mol����Ϊ��ѹ������������ƽ���ǵ�Ч�ģ���˰��������ʵ�����1.2mol����ѡA��
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣��Ҫ�ǿ���ѧ���Ե�Чƽ�����Ϥ���ճ̶ȣ��Լ�������õ�Чƽ��֪ʶ���ʵ�����������������������ѧ���������������ͳ���˼ά������
�����Ѷȣ���
2��ѡ���� ��ӦA��g��+3B��g���T2C��g��+2D��g�������ֲ�ͬ����µķ�Ӧ���ʷֱ�Ϊ��
��v��A��=0.45mol?L-1?min-1��v��B��=0.6mol?L-1?s-1
��v��C��=0.4mol?L-1?s-1��v��D��=0.45mol?L-1?s-1
�����йط�Ӧ���ʵıȽ�����ȷ���ǣ�������
A���ܣ���=�ڣ���
B����=�ڣ��ܣ���
C���٣��ڣ��ۣ���
D���ܣ��ۣ��ڣ���
�ο��𰸣�A
���������
�����Ѷȣ���
3������� Ϊ��������ЧӦ�����˼���CO2���ŷš�ֲ�����֡���Һ̬CO2ע����ȴ�ʩ�⣬����һ��˼·�ǽ�
CO2ת����������ȼ���ʡ��繤ҵ����ʵ��CO2��H2��Ӧ���ɼ״���ת������֪��
��һ���¡������ܱ������г���1mol CO2��3mol H2��һ�������·�����Ӧ��
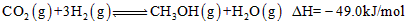 �����CO2��CH3OH(g)��Ũ����ʱ��仯����ͼ��ʾ��
�����CO2��CH3OH(g)��Ũ����ʱ��仯����ͼ��ʾ��

��ش�
(1)���ܱ������������_____L��?
(2)�ﵽƽ���ʱ����_____min(�3����10��)����ǰ10min�ڣ���CO2Ũ�ȵı仯��ʾ�ķ�Ӧ����(CO2)=
_____ mol/(L��min)��
(3)���жϸ÷�Ӧ�ﵽ��ѧƽ��״̬��������__________��
a������ѹǿ���� b�����������c(CO2)���� c��(CH3OH)=(H2O) d��c(CH3OH)=c(H2O)
(4)Ϊ�����H2��ת���ʣ��ɲ�ȡ_____(�����С��)CO2Ũ�ȵĴ�ʩ����ƽ���H2��ת������__________��ƽ�ⳣ��K=__________��(����������һλС��)
(5)��ʵ������ͼ�в������÷�Ӧ��c(H2)��ʱ��ı仯����ͼ��

�ο��𰸣�(1)1
(2)10��0.075
(3)ab
(4)����75����5.3 (5)
���������
�����Ѷȣ�����
4�������� ��7�֣���1 mol CO��1 mol H2O����ij�̶��ݻ��������У���ij�����´ﵽƽ�⣺CO��g��+H2O��g�� CO2��g��+H2��g������ʱ��
CO2��g��+H2��g������ʱ�� ��COת��ΪCO2������ƽ��״̬�»��������CO2�����������
��COת��ΪCO2������ƽ��״̬�»��������CO2�����������
�ο��𰸣�33.3%
������������ڸ÷�Ӧ�����������Ŀ����ķ�Ӧ��������������干��2 mol�������ɵ�CO2�� ?mol������ƽ��ʱCO2���������Ϊ��
?mol������ƽ��ʱCO2���������Ϊ�� ?mol��
?mol�� ��100%=33.3%��
��100%=33.3%��
�����Ѷȣ�һ��
5��ѡ���� ��15 gA������10.5 gB����ǡ����ȫ��Ӧ������9 gC��������0.3 molD���ʣ���D��������Ħ��������
A.55 g
B.55 g/mol
C.111 g/mol
D.27.5 g/mol
�ο��𰸣�B
���������
�����Ѷȣ���