微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某氯化镁溶液的密度为d?g/cm3,其中镁离子的质量分数为w,a?mL该溶液中Cl-的物质的量为
A.mol
B.mol
C.mol
D.mol
参考答案:D
本题解析:分析:根据c=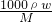 计算镁离子的浓度,再结合MgCl2可知,c(Cl-)=2c(Mg2+),以此来解答.
计算镁离子的浓度,再结合MgCl2可知,c(Cl-)=2c(Mg2+),以此来解答.
解答:氯化镁溶液的密度为d?g/cm3,其中镁离子的质量分数为w,
则c(Mg2+)=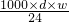 mol/L,
mol/L,
所以c(Cl-)=2c(Mg2+)=2×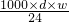 mol/L=
mol/L=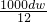 mol/L,
mol/L,
则a?mL该溶液中Cl-的物质的量为a×10-3L×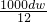 mol/L=
mol/L=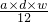 mol,
mol,
故选D.
点评:本题考查物质的量浓度的有关计算,熟悉质量分数与物质的量浓度的关系即可解答,题目难度不大.
本题难度:简单
2、填空题 (10分)照相用的废定影液中含有Na+、[Ag(S2O3)2]3-、Br-等离子.某研究性学习小组拟通过下列实验程序,对某照相公司的废定影液进行实验处理,回收其中的银和溴.
(已知:4H++2 [Ag(S2O3)2]3- = Ag2S↓+3S↓+3SO2↑+SO42-+2H2O)
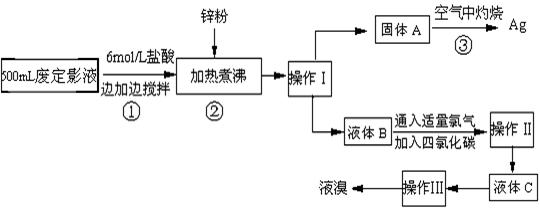
(1)操作Ⅲ的名称是?;操作Ⅱ需要的主要玻璃仪器有? ?.
?.
(2)加入锌粉的目的是将少量溴化银中的银还原出来,该反应的离子反应方程式为?.
(3)液体B中除含有Br-,还有SO42-,检验溶液中存在SO42-的操作是?
?.
(4)步骤③实验操作时,也常采用加入适量硝酸钾加盖后再灼热的方法,推测加硝酸钾的目的可能是?.
(5)上述回收银的流程中,从绿色化学的要求看,存在的不足是?.
参考答案:⑴蒸馏(1分)?分液漏斗、烧杯(2分)
(2)2AgBr + Zn =" 2Ag" + Zn2+ + 2Br―? (2分 )
)
(3)取少量液体B于小试管中,滴加BaCl2溶液,有白色沉淀说明有SO42―(2分)
(4)提供氧,使Ag2S充分反应(2分)
(5)在空气中灼烧产生的SO2有毒,污染空气(1分)
本题解析:略
本题难度:一般
3、选择题 下列说法错误的是(?)
A.一些国家常利用蒸馏法大规模地将海水淡化为可饮用的水
B.煎熬中药时,用水在煮沸条件下,提取中药的有效成分是利用化学上的萃取原理
C.物质的分离是指把混合物中各物质经过物理(或化学)变化,将其彼此分开的过程,分开后各物质要恢复到原来的状态
D.物质中所含的杂质都是无用的有害的
参考答案:D
本题解析:略
本题难度:简单
4、选择题 向碘水中加入适量CCl4并振荡,静置后观察到的现象是
[? ]
A.形成均匀的无色溶液
B.形成均匀的紫红色溶液
C.液体分层,下层呈紫红色
D.液体分层,上下层均呈无色
参考答案:C
本题解析:
本题难度:简单
5、填空题 除去Na2CO3粉末中混有的NaHCO3杂质用______方法;用______检验酒精中是否含有水.
参考答案:NaHCO3不稳定,加热易分解,除去Na2CO3粉末中混有的NaHCO3杂质用加热的方法,加热时发生
2NaHCO3?加热?.?Na2CO3+CO2↑+H2O,检验是否有水生成,可用无水硫酸铜或CuSO4,生成CuSO4?5H2O蓝色晶体.
故答案为:加热;无水硫酸铜(或CuSO4).
本题解析:
本题难度:一般