��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��MgSO4��Al2(SO4)3�Ļ����Һ�У���μ���NaOH��Һ������ͼ���У�����ȷ��ʾ������Ӧ����(�������ʾ����NaOH��Һ��������������ʾ��Ӧ���ɳ���������)
[? ]
A.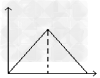
B.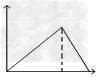
C.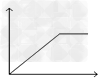
D.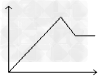
�ο��𰸣�D
���������
�����Ѷȣ�һ��
2������� ��6�֣�A��B��C��D���ֿ������Σ������ӷֱ������Ba2����Na����Ag����Cu2���е�ijһ�֣������ӷֱ������NO3����SO42����Cl����CO32���е�ijһ�֡���������ѧϰ��֪ʶ�ش��������⣺�ٰ������ηֱ�����ʢ������ˮ���Թ��У�ֻ��C�ε���Һ����ɫ������ٵ���֧�Թ��зֱ�������ᣬB���г������ɣ�D������ɫ��ζ���������
��1�������εĻ�ѧʽ�ֱ�Ϊ��A��_______��B��___________��C��__________��D��________��
��2��д��A��B��A��C��Ӧ�����ӷ���ʽ��
A+B��??��A+C��?
�ο��𰸣���ÿ��һ�֣���6�֣�
��1��A��BaCl2?B��AgNO3? C��CuSO4? D��Na2CO3
��2��A+B��Ag++Cl-==AgCl��? A+C:? Ba2++SO42-==BaSO4��
�����������Ϊ������ֻ�ܺ�NO3����ϣ�����һ������������ͬ��������֪��Ba2����ֻ�ܺ������ӽ�ϣ�����һ�����Ȼ�����C�ε���Һ����ɫ��˵��C�к���ͭ���ӡ�����ͭ���Ӳ��ܺ�CO32���������棬����C������ͭ��B�����ᷴӦ���ɰ�ɫ����������B����������D�����ᷴӦ�������壬����D��ֻ����̼���ƣ����A���Ȼ�����
�������������ʵļ���ʱ��Ҫ�������ʵ��������ʺ�������Ӧ��ѡ���ʵ����Լ��ͷ�����ȷ�۲췴Ӧ�е�������������ɫ�ı仯�����������ɺ��ܽ⡢����IJ�������ζ���������ɫ�ȣ������жϡ���������֤���ɡ�
�����Ѷȣ�һ��
3��ѡ���� ��ϡ��Һ���ܴ������棬����NaOH��Һ���г�������������������������ݳ���һ��������
A.Na+��S��Cu2+��Cl-
B.Na+��Ca2+��Cl-��HC
C.K+��Na+��N��C
D.Ca2+��K+��S��C
�ο��𰸣�B
�����������������������֮���ܽ������ˮ�����塢�����ȣ������Ӳ��ܹ��棬����ϼ���NaOH��Һ���ɳ����ͼ��������������������
���A����������֮�䲻��Ӧ���ܹ��棬��NaOH����������ͭ�������������Ӧ����A��ѡ��
B����������֮�䲻��Ӧ���ܹ��棬��NaOH����̼��Ƴ��������������ɶ�����̼���壬��Bѡ��
C����������֮�䲻��Ӧ���ܹ��棬��NaOH����Ӧ����C��ѡ��
D��Ca2+�ֱ���CO32-��SO42-������ɳ��������ܹ��棬��D��ѡ��
��ѡB��
���������⿼�����ӵĹ������⣬��Ϥ����֮��ķ�Ӧ�ǽ����Ĺؼ�����Ŀ�ѶȲ���ע����Ϣ���ۺ�Ӧ�������
�����Ѷȣ���
4��ѡ���� ���з�Ӧ����H++OH-��H2O��ʾ����
A.HCl+NH3��H2O
B.HCl+Ba(OH)2
C.H2SO4+Fe(OH)3
D.CH3COOH+NaOH
�ο��𰸣�B
���������A��NH3��H2OΪ���C��Fe(OH)3���ܣ�D��CH3COOHΪ���ᣮ
�����Ѷȣ���
5��ѡ���� ��100mLCuSO4����Һ�У���ʯī���缫���һ��ʱ�䣬�������յ�2.24L���壨��״��������ԭ��Һ�У�Cu2+�����ʵ���Ũ��Ϊ
A.1mol?L�D1
B.2mol?L�D1
C.3 mol?L�D1
D.4 mol?L�D1
�ο��𰸣�A
���������������ص��йؼ���͵缫������жϡ����Ե缫�������ͭ��Һ������ʧȥ���ӣ�OH-�ŵ磬����������Ӧ�����������缫��ӦʽΪ4OH--4e-=2H2O+O2��������ͭ���ӷŵ磬������ԭ��Ӧ��������ͭ���缫��ӦʽΪ2Cu2+��4e-=2Cu��Ӧ���������ռ������壬˵��ͭ���Ӳ��㣬��ͭ���ӷŵ����֮�ͣ���Һ�е������ӿ�ʼ�������ŵ磬�缫��ӦʽΪ4H++4e-=2H2�������������������ʵ�������0.1mol�����Ը��ݵ��ӵ�ʧ��֪ͭ���ӵ����ʵ���Ӧ��0.1mol������Ũ����1.0mol/L������A��
�����Ѷȣ�һ��