��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��2NO2(����ɫ) N2O4(��ɫ)�Ŀ��淴Ӧ��,����״̬һ������ƽ��״̬����(����)��
N2O4(��ɫ)�Ŀ��淴Ӧ��,����״̬һ������ƽ��״̬����(����)��
A��N2O4��NO2�ķ�������Ϊ1��2
B��N2O4��NO2��Ũ�����
C��ƽ����ϵ����ɫ���ٸı�
D����λʱ������1 mol N2O4��ΪNO2��ͬʱ,��1 mol NO2��ΪN2O4
�ο��𰸣�C
�����������Ӧ�������ɫ���ٱ仯,˵��NO2Ũ�Ȳ���,��Ӧ�ﵽƽ�⡣
�����Ѷȣ�һ��
2������� ��14�֣���ͼ�Ǽ����л����ת����ϵ���밴Ҫ����գ�
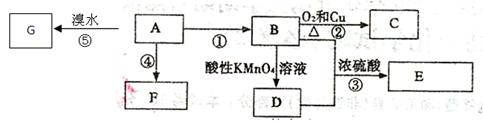
��֪��A������ʯ�͵���Ҫ�л�����ԭ�ϣ���ˮ���д������ã�75%��B������ҽ��������E�Ǿ��й���ζ���л��F��һ�ָ߾�����Ƴɶ��ְ�װ���ϡ�
��1��A�ķ���ʽΪ?��A�����Ը��������Һ���õ������ǣ�?��
��2��C������?��F�Ľṹ��ʽΪ?��
��3��D�����еĹ�����������?�������һ��ʵ������֤D���ʴ��ڸù����ŵķ�����?
?��
��4����д����Ӧ�ݵķ���ʽ��?��
��5������д��Ӧ���ͣ�A����F?��
��6�����й���A��F��������ȷ����?��
A��A�����������壬Ϊ�����F�������ǹ��壬Ϊ�����
B��A��F�Ļ�ѧ������ȫ��ͬ
C��ȡ��������A��F��ȫȼ�պ����ɵ�CO2��H2O�������ֱ����
D��ȡ�����ʵ�����A��F��ȫȼ�պ����ɵ�CO2��H2O�����ʵ����ֱ����
�ο��𰸣���1�� C2H4��?���������Һ��ɫ?��1+1�֣�
��2����ȩ��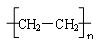 ?��1+2�֣�
?��1+2�֣�
��3���Ȼ���1�֣�?ȡ�������������Թ��еμ�ʯ����Һ������Һ�����֤���������д��ڡ�COOH��������Na2CO3��Һ��Mg������Cu��OH��2�ȣ���2�֣�
��4��CH2=CH2 + Br2 �� CH2Br-CH2Br?��2�֣�
��5���Ӿۣ�2�֣�?��6��AC?��2�֣�
���������A������ʯ�͵���Ҫ�л�����ԭ�ϣ���ˮ���д������ã����A����ϩ��75%��B������ҽ����������B���Ҵ�����ϩ�к���̼̼˫�����ܺ����շ����ӳɷ�Ӧ����G����G��CH2.BrCH2Br����ϩҲ�ܷ����Ӿ۷�Ӧ���ɸ߷��ӻ��������ϩ����F�Ǿ���ϩ����ϩ��ˮ�����ӳɷ�Ӧ�������Ҵ����Ҵ��к����ǻ����ܷ���������������ȩ���Ҵ�Ҳ������ǿ��������������ֱ�ӱ������������ᣬ��D�����ᣬ������Ҵ����Է���������Ӧ����������������E������������
�����Ѷȣ�һ��
3��ѡ���� ��ͼ���¶Ⱥ�ѹǿ��X+Y Z��ӦӰ���ʾ��ͼ������������ȷ����
Z��ӦӰ���ʾ��ͼ������������ȷ����
 ?
?
A��X��Y��ֻ��һ��Ϊ��̬��zΪ��̬
B��X��Y��Z��Ϊ��̬
C���������淴Ӧ������ӦΪ���ȷ�Ӧ
D��������Ӧ���淴Ӧ�ġ�H>0
�ο��𰸣�A
���������
ԭ�ⷽ��ʽ�д���ӦΪ��X+Y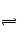 2Z
2Z
��ȷ�𰸣�A
A����ͼ����ѹ��Z������������٣�ƽ�������ƶ������������С��X��Y��ֻ��һ��Ϊ��̬��zΪ��̬��
B������ȷ��
C������ȷ����ͼ�����¶ȣ�Z���ӣ�ƽ�������ƶ��������H>0�����ȷ�Ӧ��DҲ����ȷ��
�����Ѷȣ�һ��
4��ѡ���� һ���¶��£����ݻ��̶�����������г���a mol NO2���������·�Ӧ��
2NO2(g) N2O4(g),�ﵽƽ�������������г���amol NO2���ﵽƽ�����ԭ��ƽ��Ƚ���ȷ����(����)
N2O4(g),�ﵽƽ�������������г���amol NO2���ﵽƽ�����ԭ��ƽ��Ƚ���ȷ����(����)
A��NO2��ת�������
B����ɫ��dz
C��ѹǿΪԭ��������
D��ƽ����Է���������С
�ο��𰸣�A
������������ڷ�Ӧ��������ﶼ��һ�֣���������������г���amol NO2���൱������ѹǿ��ƽ������Ӧ�����ƶ�������ѡ��A��ȷ������Ǵ���ģ���ѡA��
�����Ѷȣ�һ��
5��ѡ���� ������ʵ��������������ԭ�����͵���
A����ˮ��������ƽ��Br2+H2O HBr+HBrO����������������Һ����Һ��ɫ��dz
HBr+HBrO����������������Һ����Һ��ɫ��dz
B���ϳɰ���Ӧ��Ϊ��߰��IJ��ʣ�������Ӧ��ȡ�����¶ȵĴ�ʩ
C����ӦCO(g)+NO2(g) CO2(g)+NO(g)(����ӦΪ���ȷ�Ӧ)����ƽ��������¶���ϵ��ɫ����
CO2(g)+NO(g)(����ӦΪ���ȷ�Ӧ)����ƽ��������¶���ϵ��ɫ����
D������2HI(g) H2(g)+I2(g)����ƽ�����С���������ʹ��ϵ��ɫ����
H2(g)+I2(g)����ƽ�����С���������ʹ��ϵ��ɫ����
�ο��𰸣�D
���������A����ˮ�д�������ƽ��Br2+H2O HBr+HBrO��������AgNO3��Һʱ��Br�C��Ag+��Ӧ������AgBr������ƽ�������ƶ���Br2Ũ�ȼ�С����Һ��ɫ��dz��������������ԭ�����ͣ�B���ϳɰ���ӦΪ���ȷ�Ӧ�������¶�ƽ�������ƶ������IJ�����ߣ�������������ԭ�����ͣ�C�����ڷ�ӦCO(g)+NO2(g)
HBr+HBrO��������AgNO3��Һʱ��Br�C��Ag+��Ӧ������AgBr������ƽ�������ƶ���Br2Ũ�ȼ�С����Һ��ɫ��dz��������������ԭ�����ͣ�B���ϳɰ���ӦΪ���ȷ�Ӧ�������¶�ƽ�������ƶ������IJ�����ߣ�������������ԭ�����ͣ�C�����ڷ�ӦCO(g)+NO2(g) CO2(g)+NO(g)Ϊ���ȷ�Ӧ�����������¶ȣ�ƽ�������ƶ���NO2Ũ��������ϵ��ɫ���������������ԭ�����ͣ�D�����ڷ�Ӧ2HI(g)
CO2(g)+NO(g)Ϊ���ȷ�Ӧ�����������¶ȣ�ƽ�������ƶ���NO2Ũ��������ϵ��ɫ���������������ԭ�����ͣ�D�����ڷ�Ӧ2HI(g) H2(g)+I2(g)���������������ķ�Ӧ����С���������ƽ�ⲻ�ƶ�����ɫ�������������СʹI2Ũ����������ģ���������������ԭ�����͡�
H2(g)+I2(g)���������������ķ�Ӧ����С���������ƽ�ⲻ�ƶ�����ɫ�������������СʹI2Ũ����������ģ���������������ԭ�����͡�
�����Ѷȣ�һ��