��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �����ˮ�����Ϊ���������ε�ˮ��Ƿ��ε�ˮ�⣬�����ս���Ƿ�Ӧ���и����ʺ�ˮ�ֱ����������֣�����������������������������ϳ��µ����ʡ�����������Ϣ������˵������ȷ����(����)
A��K2O2��ˮ�������KOH��H2O2����
B��PCl3��ˮ�������HClO��PH3
C��NaClO��ˮ�����֮һ��HClO������
D��CaC2��ˮ�����֮һ��C2H2����
�ο��𰸣�B
���������A�й�����������K����O22�����ɵģ����Ը�����֪����Ϣ��֪��A��ȷ��B����ȷ����Ԫ�صķǽ�����ǿ��P�ģ�����������Ӧ����HCl��H3PO3��ͬ��������֪��ѡ��C��D����ȷ�ģ���ѡB��
�������������е��Ѷȵ����⣬����ѡ������⣬�ѶȽϴ�������ؿ���ѧ��������û���֪ʶ���ʵ�����������������������ѧ����֪ʶǨ�������ͷ�ɢ˼ά���������������ѧ����Ӧ��������
�����Ѷȣ�һ��
2��ѡ���� ��һ��Ũ�ȵ�FeCl3��Һ�У���������ˮ��ƽ�⣺Fe3+��3H2O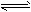 Fe(OH)3��3H+���ڴ���Һ�е��뱥�͵�FeCl3��Һ�������ĸ��仯��˵����ȷ
Fe(OH)3��3H+���ڴ���Һ�е��뱥�͵�FeCl3��Һ�������ĸ��仯��˵����ȷ
[? ]
A��ˮ��ƽ��������Ӧ�����ƶ�
B��ˮ��ƽ�����淴Ӧ�����ƶ�
C����Һ��H+Ũ������
D��Fe3+��ˮ��̶�����
�ο��𰸣�AC
���������
�����Ѷȣ�һ��
3��ѡ���� ������������ʵ���Ũ�ȵ�NaCl��NaF��Һ�У����������������?��?��
A��ǰ�߶�
B�����߶�
C��һ����
D�����ж�
�ο��𰸣�B
���������
��ȷ�𰸣�B
NaF��ǿ�������Σ�F����H2O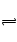 HF��OH�D ,�ٽ�ˮ���롣�������ɵ�OH�D�࣬��������������Ⱥ��߶ࡣ
HF��OH�D ,�ٽ�ˮ���롣�������ɵ�OH�D�࣬��������������Ⱥ��߶ࡣ
�����Ѷȣ���
4��ѡ���� ��֪KHSO3��Һ�������ԡ���0.1mol��L-1KHSO3��Һ�У����й�ϵ��ȷ����
A��c(K+)+ c(H+) ��c(HSO3-)+ c(OH-)+ c(SO32-)
B��c(HSO3-) + c(SO32-) = 0.1mol��L-1
C��c(SO32-) �� c(H2SO3)
D��c(K+) = c(H2SO3) + c(HSO3-) + c(SO32-)
�ο��𰸣�D
�����������0.1mol��L-1KHSO3��Һ�У�A����ݵ���غ㣺c(K+)+ c(H+)��c(HSO3-)+c(OH-)+2c(SO32-)����ԭ��ʽ��������B�����SԪ���غ㣺c(HSO3-)+ c(H2SO3) + c(SO32-) = 0.1mol��L-1����ԭ��ʽ��������C������HSO3-�����ԣ�˵���������ˮ�⣬��c(SO32-)��c(H2SO3)��ԭ��ϵ����D����������غ㣺c(K+) = c(H2SO3) + c(HSO3-) + c(SO32-)����ȷ��3��Һ������Ũ�ȵĹ�ϵ����ȷ���жϡ�
�����Ѷȣ�һ��
5������� ��ͼΪ��������25mL 0��1 mol��L-1 MOH��Һ����εμ�0��2 mol��L-1HA��Һ��������ҺpH�ı仯���ߡ�
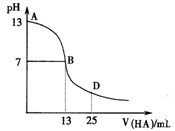
�ش��������⣺
��1����ͼ��ȷ��MOHΪ?����ǿ������������,
������?��
��2����ͼ��ȷ��HAΪ?����ǿ������������,
������?��
��3����D��ʱ����Һ��c��A����+c��HA��?2c��M+�������������������������
�ο��𰸣���1��ǿ��2�֣�������������ˮ�����ӻ�����Ϊ10-14��0��1 mol��L-1 MOH��Һ��pH=13��˵��Ϊǿ���3�֣�
��2������2�֣�����HAΪǿ������pH=7�Ǹպ���ȫ��Ӧ���������HA12��5mL����������13ml��˵�����ɵ�ǿ�������Ρ���3�֣�
��3��=��3�֣�
�����������
�����Ѷȣ�һ��