| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学必备知识点《盐类水解的原理》高频考点巩固(2017年模拟版)(十)
参考答案:C 本题解析:A中前后电荷不守恒;B中将10mL 0.1 mol/L Na2CO3溶液逐滴滴加到10 mL 0.1 mol/L盐酸中,反应是Na2CO3+2HCl==2NaCl+H2O+CO2↑,是NaCl和Na2CO3的混合物,故是c(Na+)>c(Cl-)>c(CO32-)>c(HCO3-)关系;C中根据电荷守恒是正确的;D中因为Ba(OH)2的物质的量是KAl(SO4)2的2倍,故OH-物质的量是Al3+的4倍,产物是AlO2-,故不正确。 本题难度:一般 2、填空题 (10分)工业制备氯化铜时,将浓盐酸用蒸气加热到80℃左右,慢慢加入粗CuO粉末(含杂质Fe2O3、FeO),充分搅拌使之溶解,得一强酸性的混合溶液,现欲从该混合溶液中制备纯净的CuCl2溶液[参考数据:pH≥9.6时,Fe2+完全水解成Fe(OH)2;pH≥6.4时,Cu2+完全水解成Cu(OH)2;pH≥3.7时,Fe3+完全水解成Fe(OH)3]。请回答以下问题: 参考答案:(1)不能 因Fe2+沉淀时的pH最大,Fe2+完全沉淀时的Cu2+、Fe3+早已沉淀 本题解析: 本题难度:困难 3、填空题 已知某溶液中只存在OH-、H+、Na+、CH3COO-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系: |
参考答案:(1)B ;
(2)D;
(3)CH3COOH和CH3COONa ;
(4)> ; =。
本题解析:
试题分析:(1) B中不符合电荷守恒
(2)当溶液中只有一种溶质是必须为醋酸钠,则醋酸钠溶液中各离子浓度大小顺序为c (Na+)>c(CH3COO-)>c (OH-)>c (H+),因为醋酸根离子是弱酸根,会水解。
(3)因为溶液为酸性,所以存在醋酸,酸性溶液中不可能是氢氧化钠,所以只能是醋酸钠;
(4) 因为醋酸是弱酸,弱电解质,不能完全电离,而溶液体积相等,当恰好中和时,c(CH3COOH)>c(NaOH);因为恰好呈中性,氢离子与氢氧根离子的物质的量浓度恰好相等,因为电荷守恒,所以c(Na+)=c(CH3COO-)
考点:考查离子。
本题难度:困难
4、选择题 下列有机反应中,有一种反应类型与其他三种反应类型不同的是( )
A.CH3COOH+CH3CH2OH
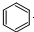 +Br2
+Br2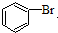 +HBr
+HBr参考答案:A.CH3COOH+CH3CH2OH浓H2SO4
本题解析:
本题难度:简单
5、填空题 (10分)泡沫灭火器的工作原理就是我们学习的盐类水解,它是彻底的双水解,
(1)灭火器有两个桶构成,一个是外面的钢桶,用来盛装 (硫酸铝、碳酸氢钠填药品的化学式)一个是里面看不到的塑料桶,用来盛装 。(同上)
(2)用离子方程式表示塑料桶盛放该试剂的原因 。
(3)用离子方程式表示其工作原理 。
(4)用碳酸氢钠而不用碳酸钠做灭火器的药品其原因是 。
(5)碳酸氢钠溶液中质子守恒的表达式是 。
参考答案:24、(1)NaHCO3与Al2(SO4)3 (2) Al3++3 H2O
本题解析:
本题难度:困难
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点大全《元素周期律.. | |