��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1�������� ���淴Ӧ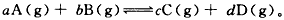 ȡamol A��b mol B����VL�����У�1 min���������A��Ũ��Ϊxmol/L����
ȡamol A��b mol B����VL�����У�1 min���������A��Ũ��Ϊxmol/L����
(1)��ʱB�����ʵ���Ũ��Ϊ���٣�
(2)��ʱC�����ʵ���Ũ��Ϊ���٣�
(3)v(A)Ϊ���٣�
�ο��𰸣�(1)bx/a mol/L
(2) (c/V-cx/a)mol/L
(3) (a/V- x) mol/(L��min)
���������
�����Ѷȣ�һ��
2��ѡ���� ��ͼ�DZ�ʾ��2X (g)��Y (g) ?Z (g)��R (g)?�SH<0 �����巴Ӧ���ʣ��ԣ���ʱ�䣨t���Ĺ�ϵ��t1ʱ��ʼ�ı������������ı�������������ߵ���
?Z (g)��R (g)?�SH<0 �����巴Ӧ���ʣ��ԣ���ʱ�䣨t���Ĺ�ϵ��t1ʱ��ʼ�ı������������ı�������������ߵ���

A������Z����
B���Ӵ�ѹǿ
C�������¶�
D��ʹ�ô���
�ο��𰸣�D
�����������ͼ���Կ�����t1ʱ�ı���������Ӧ��������ƽ�ⲻ�ƶ�������Z���ʣ�v��С��ƽ�����ƣ�A�����Ӵ�ѹǿ��v����ƽ�����ƣ�B���������¶ȣ�v����ƽ�����ƣ�C����ʹ�ô�������ͬ�ȳ̶ȵ��������淴Ӧ���ʣ�ƽ�ⲻ�ƶ���ѡD��
��������ѧƽ��ͼ���ǻ�ѧƽ���һ����Ҫ֪ʶ�㣬����߿��������飬�����ڱ���������Ӧѧ�����ͼ��
�����Ѷȣ�һ��
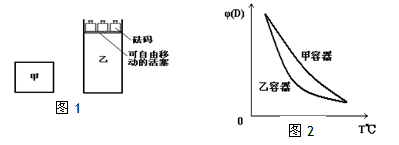
3��ѡ���� һ���¶��£��п��淴Ӧ��2A(g)��2B(g) C(g)��3D(g)����H��0���ֽ�2molA��2molB�������ΪV�ļ���������2molC��6molD������������ʹ�������ڷ�Ӧ��ʼǰ�����Ϊ2V(��ͼ1)��
C(g)��3D(g)����H��0���ֽ�2molA��2molB�������ΪV�ļ���������2molC��6molD������������ʹ�������ڷ�Ӧ��ʼǰ�����Ϊ2V(��ͼ1)��
�����������з�Ӧ��˵����ȷ����
A���������еķ�Ӧ�ȴﵽ��ѧƽ��״̬
B���������з�Ӧ����ƽ���ƽ����ϵ�и���ֵ�����ٷ������ͬ��Ũ��Ҳ��ͬ
C����������ƽ���������ͬ���¶ȣ�������������D������������¶ȱ仯��ͼ2��ʾ
D���ڼ��������ٳ���2?mol?A��2?mol?B��ƽ������c��C��������c��C����2��
�ο��𰸣�BD
���������A �������еķ�Ӧ�ȼ�����ʼ״̬�µ�4Ħ��A��4Ħ��B�ķ�Ӧ�����ݣ��Һ�ѹ�����ڸ÷�Ӧ���������������ķ�Ӧ�����Լ�����������ʼ���ո��ɷֵ�Ũ�Ⱦ���ȣ����淴Ӧ�ٶ��κ�ʱ�̾���ȣ��ʼ���������Ӧͬʱ�ﵽ��ѧƽ��״̬
B ��ȷ ��������֪�����������ﵽ��ƽ��״̬��ȫ��ͬ����ƽ����ϵ�и���ֵ�����ٷ������ͬ��Ũ��Ҳ��ͬ
C ���� ��������ƽ���������ͬ���¶�ʱ��ƽ������������������D������������¶ȱ仯�����Ҳ��ͬ
D ��ȷ ��������һ�����ȫ��ͬ������������ͬ���������������Ӧ����ʱƽ��״̬���Ӧ��ȫ��ͬ���ټ���Ѹ������еķ�Ӧ����W��������У������൱�ڸ���ѹ��ʹ���ݻ���Сһ�룬ƽ�ⲻ�ƶ�����ƽ�������и��ɷֵ�Ũ�ȶ�����ԭ����2������ƽ������c��C��������c��C����2��
�����Ѷȣ�һ��
4��ѡ���� һ���¶��£��ڼס��ҡ��������ĸ������ܱ�������Ͷ��SO2(g)��O2(g)������ʼ���ʵ�����SO2��ƽ��ת�������±���ʾ��
?
| ��
| ��
| ��
| ��
|
�ܱ��������/L
| 2
| 2
| 2
| 1
|
��ʼ���ʵ���
| n(SO2)/mol
| 0.4
| 0.8
| 0.8
| 0.4
|
n(O2)/mol
| 0.24
| 0.24
| 0.48
| 0.24
|
SO2��ƽ��ת����/%
| 80
| ��1
| ��2
| ��3
|
?
�����ж��У���ȷ����
A�����з�Ӧ��ƽ�ⳣ��С����
B�����¶��£������з�Ӧ��ƽ�ⳣ��K��Ϊ400
C��SO2��ƽ��ת���ʣ���1����2����3
D��������SO3�����ʵ���Ũ�ȣ������ף���
�ο��𰸣�B
���������A���¶�һ����ƽ�ⳣ�����䣬����B������ƽ�ⳣ��K= 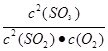 =
=  =400����ȷ��C���Һͱ��ж���������ʼ����ͬ���������������ʵ������������������ʵ��������Ԧ�1<��2�����Ͷ��ж��������������ʼŨ����ͬ��ƽ���Ч����������ת������ȣ�����D�����Ͷ�ƽ���Ч����������Ũ����ͬ�����ж��������������ʼŨ���Ǽ��ж��������������ʼŨ�ȵ�2����Ũ�ȼӱ���Ч������ѹǿ�����Ա�����������Ũ�ȴ��ڼ�����������Ũ�ȣ�����
=400����ȷ��C���Һͱ��ж���������ʼ����ͬ���������������ʵ������������������ʵ��������Ԧ�1<��2�����Ͷ��ж��������������ʼŨ����ͬ��ƽ���Ч����������ת������ȣ�����D�����Ͷ�ƽ���Ч����������Ũ����ͬ�����ж��������������ʼŨ���Ǽ��ж��������������ʼŨ�ȵ�2����Ũ�ȼӱ���Ч������ѹǿ�����Ա�����������Ũ�ȴ��ڼ�����������Ũ�ȣ�����
�����Ѷȣ�һ��
5��ѡ���� ��0.6molA��0.5molB����0.4L�ܱ������з���2A��g��+B��g��?mD��g��+E��g��������5min��ﵽ��ѧƽ�⣬��ʱ���DΪ0.2mol����֪5min����E��ʾ��ƽ����Ӧ����Ϊ0.1mol?L-1?min-1�����н�����ȷ���ǣ�������
A��A��B��ת���ʾ�Ϊ20%
B��mֵΪ1
C��5min����A��ʾ��ƽ����Ӧ����Ϊ0.1mol?L-1?min-1
D��ƽ��ʱ����������ʵ���Ϊ1mol
�ο��𰸣�v��D��=0.2mol0.4L5min=0.1mol?L-1?min-1����֪5min����E��ʾ��ƽ����Ӧ����Ϊ0.1mol?L-1?min-1��
��v��D����c��E��=0.1mol?L-1?min-1��0.1mol?L-1?min-1=1��1��
��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ���m=1����
2A��g��+B��g�� D��g��+E��g��
D��g��+E��g��
��ʼ��0.6mol 0.5mol 0 0
ת����0.4mol 0.4mol 0.2mol0.2mol
ƽ�⣺0.2mol 0.1mol 0.2mol 0.2mol
A��A��ת����Ϊ0.4mol0.6mol��100%=33.3%��B��ת����Ϊ0.4mol0.5mol��100%=80%����A����
B�������ϼ����֪��D��E�ķ�Ӧ������ͬ����m=1����B��ȷ��
C��v��A��=2v��D��=2��0.1mol?L-1?min-1=0.2mol?L-1?min-1����C����
D��ƽ��ʱ����������ʵ���Ϊ0.2mol+0.1mol+0.2mol+0.2mol=0.7mol����D����
��ѡB��
���������
�����Ѷȣ�һ��