微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (18分)工业上以黄铜矿(主要成分CuFeS2)为原料制备CuSO2・5H2O的主要流程如下:

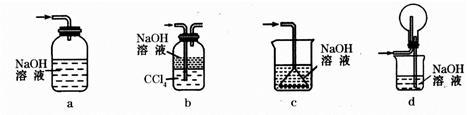
(1)下列装置可用于吸收气体X的是___________(填代号)。
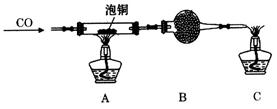
(2)某研究性学习小组用泡铜与CO反应来制取粗铜。
①装置B中的药品为_____________。?
②实验时,依次进行如下操作:组装仪器、__________________、加装药品、通入气体、_____________________、点燃酒精灯。
(3)熔渣Y的成分为Fe2O3和FeO,选用提供的试剂,设计实验验证熔渣中含有FeO。写出有关实验操作、现象与结论。?
提供的试剂:稀盐酸、稀硫酸、KSCN溶液、KMnO4溶液、NaOH溶液、氯水。
_______________________________________________________________________。
(4)向粗铜中加入硫酸和硝酸的混酸溶液制取硫酸铜时(杂质不参加反应),混酸中H2SO4与HNO3的最佳物质的量之比为___________________。
(5)用滴定法测定所得产品中CuSO4・5H2O的含量,称取a g样品配成100 mL溶液,取出20.00 mL,用c mol・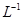 滴定剂EDTA(H2Y2-)标准溶液滴定至终点(滴定剂不与杂质反应),消耗滴定剂b mL。滴定反应如下:
滴定剂EDTA(H2Y2-)标准溶液滴定至终点(滴定剂不与杂质反应),消耗滴定剂b mL。滴定反应如下: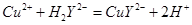 。则CuSO4・5H2O质量分数为__________。滴定管用蒸馏水洗涤后,直接注入标准溶液,则会导致测定结果偏_______。
。则CuSO4・5H2O质量分数为__________。滴定管用蒸馏水洗涤后,直接注入标准溶液,则会导致测定结果偏_______。
参考答案:(1)bd
(2)①碱石灰②检查装置气密性;收集CO检验纯度
(3)取少量熔渣,加过量稀硫酸溶解,然后向滤液中加少量KMnO4溶液,若溶液紫色退去,则说明熔渣中含有FeO
(4)3:2
(5) ;高
;高
本题解析:(1)气体X是SO2,可用NaOH溶液吸收,注意防止倒吸,故可选用bd;(2)①用泡铜制取粗铜是利用CO与Cu2O反应来得到Cu,同时生成CO2,故装置B干燥管内应放碱石灰;②实验时,依次进行的操作为:组装仪器、检查装置气密性、加装药品、通入气体、收集CO检验纯度、点燃酒精灯;(3)验证熔渣中含有FeO,可以利用亚铁离子的还原性,操作为:取少量熔渣,加过量稀硫酸溶解,然后向滤液中加少量KMnO4溶液,若溶液紫色退去,则说明熔渣中含有FeO;(4)铜不与稀硫酸反应,但可溶解在硝酸中,反应的离子方程式为3Cu+8H++2NO=3Cu2++2NO↑+4H2O,由此可知当硝酸与硫酸物质的量之比为2:3时,硝酸全部转化为NO,此时溶液中溶质为CuSO4,即混酸中H2SO4与HNO3的最佳物质的量之比为3:2;(5)根据所给反应可知n(Cu2+)=n(H2Y2-),所以CuSO4・5H2O的质量分数为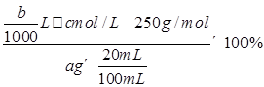 =
=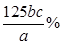 。
。
本题难度:一般
2、选择题 向只含有Fe3+、Cu2+、H+各0.1mol及a mol SO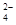 的某溶液中(只来源于水电离的离子不考虑)加入足量锌粉,搅拌使其充分反应,下列说法中正确的是(?)
的某溶液中(只来源于水电离的离子不考虑)加入足量锌粉,搅拌使其充分反应,下列说法中正确的是(?)
A.当消耗13克Zn时, 得到的还原产物为0.25mol
B.当溶液中不再产生气泡时,溶液中大量存在的阳离子只有Zn2+
C.反应中最多有两种单质生成
D.反应结束时,可得到0.25molZnSO4
参考答案:A
本题解析:三种阳离子的氧化性大小顺序是Fe3+、Cu2+、H+,所以首先还原的是Fe3+、然后是Cu2+,最后是H+。13g锌是0.2mol,失去0.4mol电子,所以根据电子的得失守恒可知,还原产物应该是0.1mol亚铁离子、0.1mo铜和0.05mol氢气,所以A正确,B不正确,含有亚铁离子;C不正确,锌足量还能生成单质铁,D不正确,应该是0.30mol硫酸锌,答案选A。
本题难度:一般
3、选择题 自然界中存在一种尖晶石,化学式为MgAl2O4,它晶莹剔透,非常美观,可以作为宝石。已知该尖晶石中混有一定量的Fe2O3。取该矿石粉末样品11.36 g,恰好能与200 mL一定浓度的盐酸反应,则该盐酸的浓度可能是( )
A.2.00 mol・L-1
B.2.80 mol・L-1
C.3.30 mol・L-1
D.3.50 mol・L-1
参考答案:B
本题解析:略
本题难度:简单
4、选择题 等质量、等溶质质量分数的稀盐酸和稀硫酸,分别与足量的铁、铝反应,按上述顺序得到氢气的质量比是()
A 1:1 ?B 1:3 ?C 98:73 ?D 73:49
参考答案:C
本题解析:足量的铁、铝说明酸完全反应,学生很容易参照例1而选A,忽略了酸中溶质的不同。等质量、等溶质质量分数的稀盐酸和稀硫酸,说明其中含有的溶质HCl和H2SO4质量是相等的,HCl和H2SO4又完全反应,所以生成氢气的质量比应等于HCl和H2SO4中所含氢元素的质量比。可设溶质HCl和H2SO4质量均为m,质量分数n,则得到氢气的质量比为:2×m×n÷36.5 :2×m×n÷98 ="?" 98 : 73。
本题难度:简单
5、简答题 用下面两种方法可以制得白色的Fe(OH)2沉淀.
方法一:用不含Fe3+的FeSO4溶液与用不含O2的蒸溜水配制的NaOH溶液反应制备.
(1)用硫酸亚铁晶体配制上述FeSO4溶液时还需加入______.
(2)除去蒸馏水中溶解的O2常采用______的方法.
(3)生成白色Fe(OH)2沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液.这样操作的理由是______.
方法二:在如图装置中,用NaOH溶液、铁屑、稀NaSO4等试剂制备.
(1)在试管I里加入的试剂是______.
(2)在试管Ⅱ里加入的试剂是______.
(3)这样生成的Fe(OH)2沉淀能较长时间保持白色,其理由是______.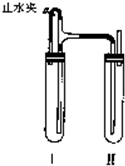
参考答案:方法一:(1)用硫酸亚铁晶体配制FeSO4溶液时要防止亚铁离子的水解和被氧气的氧化,所以要加入稀H2SO4来防止水解,加铁屑来防止被氧化,故答案为:稀H2SO4、铁屑;
(2)蒸馏水中的氧气可以通过煮沸的方法除去,故答案为:煮沸;
(3)Fe(OH)2遇到氧气会被氧气氧化成Fe(OH)3,用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,可以避免氢氧化亚铁生成后被氧气氧化,故答案为:避免生成的Fe(OH)2沉淀接触O2;
方法二:(1)铁与硫酸反应生成氢气,关闭止水夹,会使装置Ι中压强变大,使Ι中的药品进入Ⅱ中,与Ⅱ中的药品反应得到氢氧化亚铁,所以在试管I里加入试剂稀H2SO4、铁屑,获得硫酸亚铁溶液,故答案为:稀H2SO4、铁屑;
(2)试管I里加入试剂稀H2SO4、铁屑,获得硫酸亚铁溶液,并能产生氢气,当氢气使装置Ι中压强变大,使Ι中的药品硫酸亚铁进入Ⅱ中,与Ⅱ中的药品氢氧化钠反应得到氢氧化亚铁,故答案为:NaOH溶液;
(3)试管Ⅰ中反应生成的H2充满了试管I和试管Ⅱ,且外界空气不容易进入,这样获得的氢氧化亚铁可以不被氧气氧化而变质,故答案为:试管Ⅰ中反应生成的H2充满了试管I和试管Ⅱ,且外界空气不容易进入.
本题解析:
本题难度:一般