��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���д�ʩһ����ʹ��ѧ��Ӧ���ʼӿ����(����)
A������Ӧ�����
B������ѹǿ
C�������¶�
D��ʹ�ô���
�ο��𰸣�C
���������A����������Һ�巴Ӧ��������Ի�ѧ��Ӧ������Ӱ�죬����B������û������μӵķ�Ӧ������ѹǿ�Ի�ѧ��Ӧ������Ӱ�죬����C�������¶ȣ���ѧ��Ӧ����һ���ӿ죬��ȷ��D��ʹ������������ѧ��Ӧ���ʼӿ죬ʹ�ø���������ѧ��Ӧ���ʼ���������
�����Ѷȣ�һ��
2������� ��6�֣�(1)��ӦI2+2S2O32��=2I��+S4O62�������ھ����е⺬���ⶨ��ijͬѧ���ø÷�Ӧ̽��Ũ�ȶԷ�Ӧ���ʵ�Ӱ�졣ʵ��ʱ������1mL������Һ��ָʾ�������������㣬ֱ��ͨ����ɫʱ��ij����ж�Ũ���뷴Ӧ���ʵĹ�ϵ�������Լ���Ӧѡ�� (�����)��
��1mL 0.01 mol��L��1�ĵ�ˮ ��1mL 0.001 mol��L��1�ĵ�ˮ
��4mL 0.01 mol��L��1��Na2S2O3��Һ ��4mL 0.001 mol��L��1��Na2S2O3��Һ
(2)��ijͬѧѡȡ�٢۽���ʵ�飬�����ɫʱ��Ϊ4s�������(S2O32��)=
�ο��𰸣� (1)�ڢۢܣ�3�֣�����1�֣���1��1����1ȫ�ۣ�
(2)8.3��10��4mol��L��1��s��1��3�֣�
�����������1��������������Է�Ӧ���ʵ�Ӱ�졣���ݷ�Ӧ�ķ���ʽ��֪�����ѡ��٣����ڢ��У�Na2S2O3�Dz���ģ���ˮ�ǹ����ģ������Һ����ɫ����ȷ�Ĵ�ѡ�ڢۢܡ�
��2�����ݷ���ʽ��֪������Na2S2O3�����ʵ���Ũ����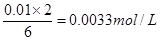 �����Ԧ�(S2O32��)��
�����Ԧ�(S2O32��)��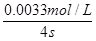 ��8.3��10��4mol��L��1��s��1��
��8.3��10��4mol��L��1��s��1��
�����Ѷȣ�һ��
3������� ��1����֪Na2S2O3+H2SO4�TNaSO4+S��+SO2+H2O����ͬѧͨ���ⶨ�÷�Ӧ����ʱ��Һ����ǵ�ʱ�䣬�о���������Ի�ѧ��Ӧ���ʵ�Ӱ�죮���ʵ���������ȡ��Һ�����Ϊ10mL����
| ʵ���� | ʵ���¶�/�� | c��Na2S2O3��/mol?L-1 | c��H2SO4��/mol?L-1
��
25
0.1
0.1
��
25
0.2
0.1
��
25
0.1
0.2
��
50
0.2
0.1
��
50
0.1
0.1
|
������������ʱ��̽���¶ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죬Ӧѡ��ʵ��______����ʵ���ţ���
��ͬʱѡ��ʵ��١�ʵ��ڡ�ʵ��ۣ��ⶨ���Һ����ǵ�ʱ�ʣ���̽��______�Ի�ѧ��Ӧ���ʵ�Ӱ�죮
��2��ijͬѧ�����ͼʵ������̽��Na2S2O3�Ļ�ѧ���ʣ�
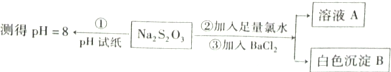
���������ʽ��ʾNa2S2O3��Һ���м��Ե�ԭ��______��ʵ��������в���ʱpH��ֽ����ɫӦ�ýӽ�______��
A����ɫB������ɫC����ɫD����ɫ
����������ʵ��ڡ��۵�Ŀ����Ϊ��̽��Na2S2O3ij�ֻ�ѧ���ʣ�����Ϊ��̽����Na2S2O3��______�ԣ�
�ο��𰸣���1��������������̽���¶ȶԻ�ѧ��Ӧ���ʵ�Ӱ��ʱ��Ҫ��Ũ�ȱ���һ�£��¶ȳ�ΪΨһ�������٢ݺ͢ڢ�������Ũ��һ�£���˿�ѡ�٢ݻ�ڢܣ�ʵ��١�ʵ��ں�ʵ��۵��¶���ͬ��Ũ�Ȳ�ͬ�����̽������Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죬
�ʴ�Ϊ���٢ݻ�ڢܣ��Ƚϸı䲻ͬ��Ӧ���Ũ�ȶԷ�Ӧ���ʵ�Ӱ�죻
��2��Na2S2O3����ǿ�������Σ���ˮ��Һ�п��Է���ˮ�⣬ˮ������ӷ���ʽΪ��S2O32-+H2O?HS2O3-+OH-��PH=8��Ӧ����ɫ����Ӧ����ɫΪ��ɫ����ɫ����BΪ���ᱵ��������ˮ��Ŀ���ǰ�S2O32-����Ϊ��������ӣ�������Na2S2O3�Ļ�ԭ�ԣ�
�ʴ�Ϊ��S2O32-+H2O?HS2O3-+OH-��D����ԭ��
���������
�����Ѷȣ�һ��
4������� ijͬѧͨ����ѧ��Ӧ2H2O2=2H2O+O2��̽�������Ի�ѧ��Ӧ���ʵ�Ӱ�죬��Ʋ�������±���ʾ��̽��ʵ�飺
| ʵ����� | ʵ������ | ʵ�����
ʵ��һ
ȡ5mL5%�Ĺ���������Һ���Թ��У���������ǵ�ľ��
���������ݲ�����ľ������ȼ
��������ֽ�������������Ƿ�Ӧ������
ʵ���
���������ܼӿ��������ķֽ�
|
��1������Ϊ��ʵ�������ʵ�����ӦΪ______ʵ������ӦΪ______
��2����ͬѧ���һ��֤�����������ڷ�Ӧ2H2O2=2H2O+O2����ֻ�䵱�������ֲ�����������������̽��ʵ�飺��һ�����ʵ������а��������γ�������Ŀ����______��?�ڶ������ʵ�����á�ʵ�������Ӧ���Թ��ڵ�ʣ�������ʵ�飮��������ʵ�������______������______����Ϊ______��
�ο��𰸣���1������ʵ����ۣ����������ܼӿ��������ķֽ⣬ʵ����е�ʵ�����Ӧ����������̣���ʱľ��Ѹ�ٸ�ȼ��
�ʴ�Ϊ��ȡ5mL5%�Ĺ���������Һ���Թ��У�����������̣���������ǵ�ľ�����д������ݲ�����ľ��Ѹ�ٸ�ȼ��
��2����������ֻ�䵱����������Ҫ֤�����������ڷ�Ӧǰ����������ֲ��䣻����Ҫ֤���������̵Ļ�ѧ���ʱ��ֲ��䣮
�ʴ�Ϊ���Ƚ϶��������ڹ�������ֽ�ǰ��������Ƿ����仯���㵹����Ӧ���Һ�壬��ʣ��Ĺ��������¼������������Һ���д������ݲ�����˵�������������ܼӿ��������ķֽ����ʣ�����ѧ����û�䣮
���������
�����Ѷȣ�һ��
5��ѡ���� ����Ƭ��ϡ���ᷴӦ��ȡ����ʱ�����д�ʩ��ʹ�����������ʼӴ���ǣ�������
A������ϡ���ᣬ����98%Ũ����
B�����������ˮ����ͭ
C�������¶�
D������������ˮ
�ο��𰸣�A����Ũ�������ǿ�����ԣ�������Ũ���ᷴӦ���ɶ��������ò�����������A����
B���μ�����CuSO4��Һ���û���Cu���γ�ԭ��أ������绯ѧ��Ӧ����Ӧ���ʼӿ죬��B��ȷ��
C��������ʹ��Ӧ���ʼ�������C����
D����ˮ���൱�ڽ�����ϡ�ͣ���Ӧ���ʼ�������D����
��ѡB��
���������
�����Ѷȣ�һ��