微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、推断题 下图是部分短周期元素的单质及其化合物(或其溶液)的转化关系,已知B、C、D、E是非金属单质,且在常温常压下都是气体;化合物G的焰色反应为黄色,化合物I和J通常状况下呈气态

请完成下列填空
(1)H的化学式_________、F的电子式_________。
(2)F和CO2的化学方程式__________________。写出G溶液中逐滴加入等物质的量的I溶液反应的离子方程式______________________。
(3)A与B在加热条件下反应的主要现象是__________________;检验H中阳离子的方法是___________________________。
参考答案:
(1)NH4Cl;
(2)2Na2O2+2CO2==2Na2CO3+O2;CO32-+H+=HCO3-
(3)剧烈反应,火焰为黄色,生成淡黄色的固体;取少量H样品放入试管,加入氢氧化钠溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,证明有铵根离子
本题解析:
本题难度:一般
2、推断题 在下列各变化中,E为常温下无色无味的液体,F为淡黄色粉末,G为常见的无色气体(反应条件均已省略)。

回答下列问题:
(1)写出H的电子式:_______________。
(2)若反应①在加热条件下进行,A为单质,C为无色有刺激性气味的气体,D为无色无味的气体,且C、D两种气体均能使澄清的石灰水变浑浊,则反应①的化学方程式是 ___________。
①实验需要检验出C、D、E三种气体产物,三种气体检验的先后顺序是 ___________(用化学式填空),在检验D气体前,需除去C气体,所用试剂是_____________ ,反应的离子方程式是_____________ 。
②已知:A(s)+O2(g) =AO2(g) △H=-393.5kJ・mol-1; 2A(s)+O2(g) =2AO(g) △H=-221.0kJ・mol-1,则AO的燃烧热的热化学方程式_________________________。
③AO2在自然界循环时可与碳酸钙反应,碳酸钙是一种难溶物质,它的Ksp=2.8×10-9。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10-4mol/L,则生成沉淀所需CaCl2溶液的最小浓度为___________。
(3)若反应①在溶液中进行,A是一种常见一元强碱,B是一种酸式盐,D是一种气体,且B遇盐酸产生能使品红溶液褪色的气体,在加热条件下,当A过量时,反应①的离子方程式是_______________ 。
(4)若反应①在溶液中进行,A是一种强酸,B是一种含有两种金属元素的盐,且B的水溶液显碱性,A、B均由短周期元素组成,当A过量时,C及D均易溶于水,则A过量时反应①的离子方程式是_________________ 。
参考答案:(1)NaOH
(2)C+2H2SO4(浓)=CO2↑+2SO2↑+2H2O
①H2O、SO2、CO2;酸性KMnO4溶液;2MnO4-+5SO2+H2O=2Mn2++5SO42-+4H+
②CO(g)+ 1/2 O2(g)=CO2(g);△H=-283.0kJ×mol-1?
③5.6×10-5mol/L)
(3)2OH-+NH4++HSO3-=NH3↑+2H2O+SO32-
(4)4H++AlO2-=Al3++2H2O
本题解析:
本题难度:一般
3、推断题 已知:A、B为短周期非金属单质且均为气体;甲、乙为短周期金属单质,乙在I的浓溶液中发生钝化;C、H、J的溶液均呈碱性.各物质间的转化关系如下(部分生成物未给出,且未注明反应条件)

(1)写出A的电子式__________、C分子的空间构型:_____________。
(2)写出反应②的化学方程式____________________________。
(3)反应④的化学方程式为______________________________。
(4)反应⑤的化学方程式是______________________________。
(5)反应⑥的离子方程式是______________________________。
参考答案:(1)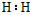 ;三角锥形
;三角锥形
(2)4NH3+5O2 4NO+6H2O
4NO+6H2O
(3)3NO2+H2O==2HNO3+NO
(4)2Na+2H2O==2NaOH+H2↑
(5)2Al+2H2O+2OH-==2AlO2-+3H2↑
本题解析:
本题难度:困难
4、填空题 (16分). 在某澄清、透明的黄色溶液中,可能含有NH4+、Fe3+、Ba2+、Al3+、SO42-、HCO3-、I-?Cl-离子。进行下述实验(所加试剂均过量)。
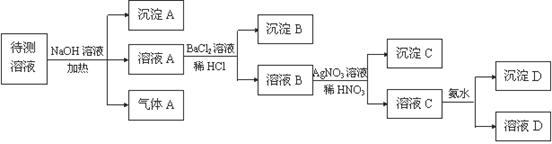
(1) 沉淀 A的化学式是?,气体A的化学式是?;
(2)待测液中一定存在?;一定不存在? _______?用离子方程式表示上述离子一定不存在的原因?。
(3)写出溶液C与过量氨水反应的离子方程式?。
(4)若气体A、沉淀A、沉淀D的物质的量各为1mol,则SO42-的物质的量为:? mol
参考答案:(1)Fe(OH)3? (1分)? NH3(1分)(2) (2分)
(2分)
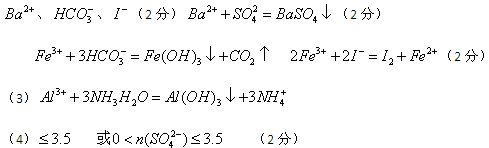
本题解析:溶液显黄色,所以一定含有铁离子。铁离子具有氧化性,能氧化碘离子生成单质碘。同时也能和HCO3-相互水解生成氢氧化铁和CO2,所以就一定不能含有HCO3-、I-。加入过量的氢氧化钠生成沉淀,所以该沉淀一定是氢氧化铁。气体应该是氨气,因此一定含有NH4+。溶液A能和盐酸酸化的氯化钡反应生成白色沉淀,所以该沉淀是硫酸钡,因此一定含有SO42-,则就一定没有Ba2+。溶液B中含有氯离子,生成沉淀C是氯化银,但由于前面用盐酸酸化,所以不能确定是否含有氯离子。溶液C能和过量的氨水反应生成沉淀,所以该沉淀只能是氢氧化铝,即原溶液中还含有Al3+。若气体A、沉淀A、沉淀D的物质的量各为1mol,则溶液中阳离子的电荷数是7mol,由于不能排除氯离子,所以SO42-的物质的量应该是小于等于3.5mol。
本题难度:一般
5、选择题 如右图所示,6个编号分别表示六种物质:Al、Fe2O3、NaOH溶液、氢碘酸、NH3、O2.凡是直线相连的两种物质均能发生化学反应(已知高温时氨气能还原Fe2O3).图中①表示的物质是( )
A.Al
B.NaOH溶液
C.氢碘酸
D.O2或Fe2O3
