��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��ӦC��s��+H2O��g��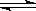 CO��g��+ H2��g����һ�ݻ��ɱ���ܱ������н��С����������ĸı���䷴Ӧ���ʼ�����Ӱ�����
CO��g��+ H2��g����һ�ݻ��ɱ���ܱ������н��С����������ĸı���䷴Ӧ���ʼ�����Ӱ�����
A�����ӹ���C����
B�������ʵ��Ĵ���
C������ѹǿ���䣬�����������ʹ�����ݻ�����
D�����������ݻ����䣬�����������ʹ��ϵѹǿ����
�ο��𰸣�AD
�����������
�����Ѷȣ���
2��ѡ���� һ���¶��£����淴Ӧ3X��g��+Y��g��?

?2Z��g���ﵽ�ȵı�־�ǣ�������
A��X��Y��Z��Ũ�����
B��X������������Z�������������
C��X��Y��Z�ķ��Ӹ�����Ϊ3��1��2
D����λʱ��������3nmolX��ͬʱ����nmolY
�ο��𰸣�A��ƽ��ʱ�����ʵ�Ũ���Ƿ���ȣ�ȡ���ڷ�Ӧ���Ũ�ȴ�С��ϵ�Լ���Ӧ�ij̶ȣ������ж��Ƿ�ﵽƽ��״̬����A����
B��X������������Z������������Ȳ���ƽ��״̬��ֻ�е�λʱ��������3nmolX��ͬʱ����2nmolZ����֤�����淴Ӧ������ȣ��ﵽƽ��״̬����B����
C��ƽ��ʱ�����ʵķ��Ӹ�������ȷ����ȡ���ڿ�ʼ��Ӧʱ�����ʵ����ʵ����Ķ����Լ���Ӧ��ת���̶ȣ������ж��Ƿ�ﵽƽ��״̬����C����
D����λʱ��������3nmolX��ͬʱ����nmolY��˵�����淴Ӧ������ȣ��ﵽƽ��״̬����D��ȷ��
��ѡD��
���������
�����Ѷȣ�һ��
3��ѡ���� ����ͼ��Ӧ˵����ȷ���ǣ�?��
A��ͼ1��ʾ���º�ѹ����������2HI  H2 + I2 ��H>0�ķ�Ӧ�ﵽƽ��������г���HI���ױ�ʾ����Ӧ���ʣ��ұ�ʾ�淴Ӧ����
H2 + I2 ��H>0�ķ�Ӧ�ﵽƽ��������г���HI���ױ�ʾ����Ӧ���ʣ��ұ�ʾ�淴Ӧ����
B��ͼ1��ʾ��������������2HI  H2 + I2 ��H>0�� ��Ӧ�ﵽƽ����������ȣ��ױ�ʾ����Ӧ���ʣ��ұ�ʾ�淴Ӧ����
H2 + I2 ��H>0�� ��Ӧ�ﵽƽ����������ȣ��ױ�ʾ����Ӧ���ʣ��ұ�ʾ�淴Ӧ����
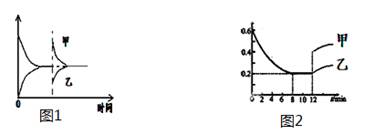
C��ͼ2��ʾ���������£�ѹ��2SO3(g) 2SO2(g)��O2(g) ��H>0ƽ�ⷴӦ��ϵ���ױ�ʾ��SO3���ʵ����ı仯���ұ�ʾ��SO3���ʵ���Ũ�ȵı仯
2SO2(g)��O2(g) ��H>0ƽ�ⷴӦ��ϵ���ױ�ʾ��SO3���ʵ����ı仯���ұ�ʾ��SO3���ʵ���Ũ�ȵı仯
D��ͼ2��ʾ���������£�����2SO3(g) 2SO2(g)��O2(g) ��H>0��Ӧƽ����ϵ���ױ�ʾ�����¶�SO3���ʵ����ı仯���ұ�ʾ����O2��SO3���ʵ����仯
2SO2(g)��O2(g) ��H>0��Ӧƽ����ϵ���ױ�ʾ�����¶�SO3���ʵ����ı仯���ұ�ʾ����O2��SO3���ʵ����仯
�ο��𰸣�A
������������º�ѹ����������2HI  H2 + I2 ?��H>0�ķ�Ӧ�ﵽƽ��������г���HI�����������������ʵ��������������ݻ���������HI�ĺ�����Ũ��������������Ӧ����������Ϊ�������Ũ���ڸı��һ˲�䣬�����������ݻ�������Ũ�ȼ�С�������淴Ӧ���ʽ��͡���˸�˵����ȷ��B. �����¶ȣ������Ƿ��ȷ�Ӧ�������ȷ�Ӧ����Ӧ���ʶ��ӿ졣����C�����������£�ѹ��2SO3(g)
H2 + I2 ?��H>0�ķ�Ӧ�ﵽƽ��������г���HI�����������������ʵ��������������ݻ���������HI�ĺ�����Ũ��������������Ӧ����������Ϊ�������Ũ���ڸı��һ˲�䣬�����������ݻ�������Ũ�ȼ�С�������淴Ӧ���ʽ��͡���˸�˵����ȷ��B. �����¶ȣ������Ƿ��ȷ�Ӧ�������ȷ�Ӧ����Ӧ���ʶ��ӿ졣����C�����������£�ѹ��2SO3(g) 2SO2(g)��O2(g)��Ӧ��������Ũ�ȶ����������������ϵ���������������Ũ������Ķ࣬����ƽ�������ƶ�������D.��Ӧ2SO3(g)
2SO2(g)��O2(g)��Ӧ��������Ũ�ȶ����������������ϵ���������������Ũ������Ķ࣬����ƽ�������ƶ�������D.��Ӧ2SO3(g) 2SO2(g)��O2(g) ������ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ��������Ӧ�����ƶ��������������ݻ����䣬SO3�����ʵ�������С����c(SO3)���͡�����O2����Ϊ�������Ũ����������ƽ�������ƶ�SO3���ʵ���������
2SO2(g)��O2(g) ������ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ��������Ӧ�����ƶ��������������ݻ����䣬SO3�����ʵ�������С����c(SO3)���͡�����O2����Ϊ�������Ũ����������ƽ�������ƶ�SO3���ʵ���������
�����Ѷȣ�һ��
4��ѡ���� ���淴Ӧ��2A��g��+3B��g��?3C��g��һ�������£�ʹһ������A��B��Ӧ�ﵽƽ��״̬ʱ������˵����ȷ���ǣ�������
A��ƽ�����������Ƿ�Ӧ�տ�ʼʱ��
B��ƽ�������и����ʵ�Ũ�ȱ�Ϊ2��3��3
C����λʱ������������a?mol?A������ͬʱҲ������1.5a?mol��C
D��ƽ�������и����ʵ�Ũ�����
�ο��𰸣�A��������ʼ��δ֪���Ҳ�֪ƽ�ⳣ����������ƽ�����������Ƿ�Ӧ�տ�ʼʱ��35��Ϊ�ж��Ƿ�ƽ������ݣ���A����
B��ƽ�������и����ʵ�Ũ�ȱ�Ϊ2��3��3���������ж��Ƿ�ﵽƽ��״̬������ʼ���ϱ��Լ���Ӧ��ת���̶��йأ���B����
C����λʱ������������amolA������ͬʱҲ������1.5amol��C��˵�����淴Ӧ������ȣ���C��ȷ��
D��ƽ�������и����ʵ�Ũ����Ȳ����ж��Ƿ�ﵽƽ��״̬������ʼ���ϱ��Լ���Ӧ��ת���̶��йأ���D����
��ѡC��
���������
�����Ѷȣ���
5������� �״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����
��1����ҵ��һ��������ַ����Ʊ��״���
��Ӧ��CO(g) + 2H2 (g)  CH3OH (g)?DH1
CH3OH (g)?DH1
��Ӧ��CO2(g)+ 3H2(g)? ?CH3OH (g)+H2O(g)?DH2
?CH3OH (g)+H2O(g)?DH2
�� �±����������Ƿ�Ӧ���ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ����K����
�¶�
| 250��
| 300��
| 350��
|
K
| 2.041
| 0.270
| 0.012
|
�ɱ��������ж�DH1_______________0���<������=����>������
�� ij�¶��£���2molCO��6molH2����2L�ܱ������г�ַ�Ӧ��4���Ӻ�Ӧ�ﵽƽ�⣬���CO�����ʵ���Ϊ0.4mol����CO�ķ�Ӧ����Ϊ________________����ʱ��ѹǿ�Ƿ�Ӧǰѹǿ��___________����
��2����Ӧ���ƽ�ⳣ������ʽΪ____________________��Ϊ�˼ӿ췴Ӧ��ķ�Ӧ���ʣ��������H2��ת���ʣ���ȡ�Ĵ�ʩ��_______________����д��ȷѡ�����ĸ����
a������CO2��Ũ��? b������H2��Ũ��
c������ѹǿ? d���������
��3����ҵ������CO��ˮ�����ķ�Ӧ�����ж���COת��Ϊ����CO2����д�й��Ȼ�ѧ��Ӧ����ʽ__________________________________���÷�Ӧ��830K�½���ʱ����ʼŨ�ȵ���ƽ���ʱ�������µĹ�ϵ��
CO�ij�ʼŨ��(mol/L)
| 2
| 4
| 1
| 3
|
H2�ij�ʼŨ��(mol/L)
| 3
| 2
| 3
| 3
|
ʱ�䣨min��
| 8
| 6
| 12
| n
|
?
��n Ϊ________min��
��4����������������Ա�¿�����һ�ּ״���������ǿ����ҺΪ�������Һ�������ֻ���ء��õ���м״�������Ӧ��һ��Ϊ______������缫��ӦʽΪ_________________��
��5���øõ������Դ���ö��Ե缫��ⱥ��NaCl��Һʱ��ÿ����0.2mol CH3OH�����������������������Ϊ?L��
�ο��𰸣���1����<(1��)��?�� 0.2mol/(L��min) (1��)��? 0.6(2��)��
��2��K= c(CH3OH ) ��c(H2O) / c(CO2) ��c3(H2) (1��)��? a��c(1��)��
��3��CO(g)+ H2O(g)  CO2(g)+H2(g)?DH = DH 1 - DH 2(2��)��? 4(2��)��
CO2(g)+H2(g)?DH = DH 1 - DH 2(2��)��? 4(2��)��
��4������1�֣���? CH3OH �C 6e- + 8OH-? = CO32- + 6H2O��2�֣���
��5��13.44(2��)��
��������������������¶����ߣ�ƽ�ⳣ��K��С�����Է�Ӧ���ȣ�
CO(g) + 2H2 (g)  CH3OH (g)
CH3OH (g)
��ʼ��mol����? 2? 6? 0
�仯����mol����1.6? 3.2? 1.6
ƽ������mol����0.4? 2.8? 1.6
ƽ��ʱ���������Ϊ0.4+2.8+1.6=4.8mol��Ϊԭ����4.8/8=0.6������ѹǿΪԭ����0.6������3���ɸ�˹���ɿ�֪��Ӧ��-�ɵ÷�ӦCO(g)+ H2O(g)  CO2(g)+H2(g)?DH = DH 1 - DH 2������
CO2(g)+H2(g)?DH = DH 1 - DH 2������
CO�ij�ʼŨ��(mol/L)
2
4
1
3
H2�ij�ʼŨ��(mol/L)
3
2
3
3
ʱ�䣨min��
8
6
12
n
?
H2�ij�ʼŨ����ͬ��CO��Ũ��Ϊ2��1ʱ������ʱ��Ϊ2��3����CO��Ũ��Ϊ2��3ʱ������ʱ��Ϊ2��1����n=4����4����? CH3OH �C 6e- + 8OH-? = CO32- + 6H2O����5��ÿ����0.2mol CH3OH��ת�Ƶĵ���Ϊ1.2mol�����ص�������ӦΪ2H++2e-=H2�����Բ���������Ϊ0.6mol������µ����Ϊ13.44L.
�����Ѷȣ�����