微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (6分)元素在周期表中的位置,反映了元素的原子结构和元素的性质。右图是元素周期表的一部分。
?
| ?
| ?
| ?
| ?
| ?
|
?
| C
| N
| O
| F
| ?
|
?
| Si
| P
| S
| Cl
| ?
|
?
| Ge
| As
| Se
| Br
| ?
|
?
| Sn
| Sb
| Te
| I
| ?
|
?
| Pb
| Bi
| Po
| At
| ?
|
?
(1)非金属性最强的元素是?,常用来做半导体材料的元素是?;?
(2)形成化合物种类最多的元素是?,写出该元素最高价氧化物的化学式?;
(3)根据元素周期律,请你预测(填“>”或“<”):酸性强弱H3AsO4?H3PO4,气态氢化物的稳定性AsH3?H2Se 。
参考答案:(1)F ,Si或Ge (2)C ,CO2 ?(3)<,<
本题解析:考查元素周期表的结构和元素周期律的应用。在周期表中非金属性最强的元素位于周期表的右上角,是氟元素。在金属和非金属的分界线附近的元素常用作半导体材料。有机物的种类最多,氧化物必须还有碳元素。同主族元素自上而下金属性逐渐增强,非金属性逐渐减弱。同周期元素自左向右金属性逐渐减弱,非金属性逐渐增强。
本题难度:一般
2、选择题 短周期元素W、X、Y和Z的原子序数依次增大。其中W的原子半径最小,X的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气分馏方法来生产Y的单质,且Y和Z可以形成化合物ZY2和ZY3。根据以上叙述,下列说法中正确的是
A.以上四种元素的原子半径大小为W<X<Y<Z
B.W、X、Y、Z原子的核外最外层电子数的总和为20
C.W与Y可形成既含极性共价键又含非极性共价键的化合物
D.由W与X组成的化合物的沸点总低于由W与Y组成的化合物的沸点
参考答案:C
本题解析:X的一种核素在考古时常用来鉴定一些文物的年代,用的是14C,采用的是断代法;工业上采用液态空气分馏方法来生产Y的单质,因此Y可能是氧气或氮气。又因为Y和Z可以形成化合物ZY2和ZY3,且短周期元素W、X、Y和Z的原子序数依次增大,所以Y是氧元素,Z是硫元素。W的原子半径最小,所以W是H。A、同周期元素从左到右元素的原子半径逐渐减小,同主族元素自上而下原子半径逐渐增大,所以四种元素的原子半径大小为W<Y<X<Z,故A错误;B、W、X、Y、Z原子的核外最外层电子数的总和为1+4+8+8=21,故B错误;C、W与Y可形成H2O2的化合物,既含极性共价键又含非极性共价键,故C正确;D、碳元素与氢元素可以形成多种烃类化合物,当相对分子质量较大时,形成的烃在常温下为液体或固体,沸点较高,可以高于氧元素与氢元素形成的化合物的沸点,D不正确,答案选C。
本题难度:一般
3、填空题 (9分)下表是元素周期表的一部分,按要求填空(填元素符号或化学式):
族
周期
| ⅠA
| ⅡA
| ⅢA
| ⅣA
| ⅤA
| ⅥA
| ⅦA
| 0
|
2
| ?
| ?
| ?
| ?
| ①
| ?
| ②
| ?
|
3
| ③
| ④
| ⑤
| ⑥
| ?
| ⑦
| ⑧
| ⑨
|
4
| ⑩
| (11)
| ?
| ?
| ?
| ?
| (12)
| ?
|
(1)写出下列元素的元素符号:①?②?(11)?
(2)在这些元素中,最活泼的金属元素是?,最活泼的非金属元素是?,最不活泼的元素是?。
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是?,碱性最强的是?,呈两性的氢氧化物是?。
参考答案:(1)① N?②? F? (11) Ca?(2)? K?, F?, Ar?。
(3)? HClO4?,? KOH?,? Al(OH)3?。
本题解析:略
本题难度:简单
4、选择题 47Ag有两种同位素,在自然界所占的原子百分比几乎相同,若Ag的近似相对原子质量为108,则这两种同位素的中子数为:
A.106和110
B.57和63
C.153和73
D.60和62
参考答案:D
本题解析:元素的相对原子质量是该元素各种同位素原子所占的一定百分比算出的平均值。设这两种同位素的中子数分别为x和y,则有(47+x)×50%+(47+y)×50%=108,解得x+y=122。所以答案是D。
本题难度:简单
5、选择题 短周期元素X、Y、Z、M、R在周期表中的相对位置如图所示。下列说法正确的是
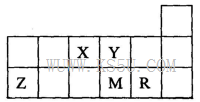
A.元素X和M的氧化物对应的水化物均为强酸
B.R的单质能与M的氢化物发生置换反应
C.气态氢化物的稳定性:M>Y
D.元素Y、Z形成的简单离子半径大小关系为:Z>Y
参考答案:B
本题解析:有元素在周期表中的位置可知:X:N;Y:O;Z:Al; M:S;R:Cl。N有多种氧化物,NO、NO2为不成盐氧化物,N2O3对应的水化物HNO2是弱酸,S的氧化物SO2对应的水化物H2SO3也为弱酸。错误。B.Cl2+H2S=2HCl+S.正确。C.元素的非金属性越强,其氢化物的稳定性就越强。由于非金属性O>S。所以气态氢化物的稳定性:H2O > H2S。错误。D.对于电子层结构相同的离子来说,元素的核电荷数越多,离子半径就越小。O2-、 Al3+的的核外电子排布均为2 8;但核电荷数Al3+ >O2-,所以离子半径:O2->Al3+。错误。
本题难度:简单