微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在中和热测定的实验中不需要用到的仪器是
[? ]
A.量筒
B.温度计
C.环形玻璃搅拌棒
D.天平
参考答案:D
本题解析:
本题难度:简单
2、选择题 为了测定酸碱反应的中和热,计算时至少需要的数据是:①酸的浓度和体积;② 碱的浓度和体积;③比热容;④反应后溶液的质量;⑤生成水的物质的量;⑥反应前后温度变化;⑦操作所需的时间
[? ]
A.①②③⑥
B.①③④⑤
C.③④⑤⑥
D.全部
参考答案:A
本题解析:
本题难度:一般
3、简答题 (1)已知20.0gNaOH稀溶液跟足量稀盐酸反应,放出28.68kJ热量,那么此反应数据表明:如果NaOH稀溶液跟稀盐酸中和生成18g水时,该反应放出热量______kJ,由此测得的中和热为______kJ/mol.
(2)已知断开1molH-H键、1mol?Br-Br键、1mol?H-Br键分别需要吸收的能量为436kJ、193kJ、366kJ.?计算H2和Br2反应生成1mol?HBr需______(填“吸收”或“放出”)能量______kJ.
参考答案:(1)NaOH+HCl=NaCl+H2O
? 40g?18g
?20g?xg
x=9g
设生成18g水放出热量为QkJ,有18:9=Q:28.68,
Q=57.36,
中和热为生成1mol水放出的热量,中和热为57.36kJ/mol,
故答案为:57.36;57.36;
(2)H2和Br2反应生成1mol?HBr,
则断裂化学键吸收的能量为:0.5mol×436kJ/mol+0.5mol×193kJ=314.5kJ,
形成1molH-Br键放出的能量为:366kJ,
314.5kJ<366kJ,
所以反应放热,放出的热量为:366kJ-314.5kJ=51.5kJ,
故答案为:放出;?51.5.
本题解析:
本题难度:一般
4、实验题 用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题
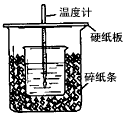
(1)从实验装置上看,图中尚缺少的一种玻璃用品是________________。
(2)烧杯间填满碎纸条的作用是________________。
(3)大烧杯上如不盖硬纸板,求得的中和热数值____________(填“偏大、偏小、无影响”)
(4)如果用60 ml 0.50 mol/L盐酸与50mL 0.55 mol/L Na OH溶液进行反应,与上述实验相比,所放出的热量_________(填“相等、不相等”),所求中和热___________(填“相等、不相等”), 简述理由
_____________________
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热___________的数值会 (填“偏大”、“偏小”、“无影响”)。
参考答案:(1)环形玻璃搅拌棒
(2)减少实验过程中的热量损失
(3)偏小
(4)不相等;相等;因为中和热是指酸跟碱发生中和反应生成1mol H2O所放出的热量,与酸碱的用量无关
(5)偏小
本题解析:
本题难度:一般
5、实验题 某化学兴趣小组要完成中和热的测定。
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃棒、0.5mol・?L-1?盐酸、0.55mol・L-1 NaOH溶液,尚缺少的实验玻璃用品是__________、____________。
(2)他们记录的实验数据如下:

已知:Q=Cm(t2?-t1),反应后溶液的比热容C为4.18KJ・℃-1・Kg-1,各物质的密度均为1g・cm-3。计算完成上表。△H=____________
(3)某研究小组将V1?mL?1.0?mol/L?HCl溶液和V2?mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2=50?mL)。
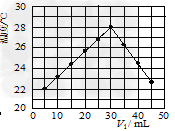
回答下列问题:研究小组做该实验时环境温度__________(填“高于”、“低于”或“等于”)22?℃,此反应所用NaOH溶液的浓度应为__________mol/L。
参考答案:(1)量筒? ;温度计
(2)-56.8KJ/mol?
(3 )低于?;1.5
本题解析:
本题难度:一般