微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 中国是最早使用天然气的国家.天然气的主要成分是( )
A.CO
B.H2
C.CH4
D.H2S
参考答案:C
本题解析:
本题难度:一般
2、填空题 铝是一种重要的金属,在生产、生活中具有许多重要的用途。眉山市电解铝厂位于三苏故里修文乡,现已经形成年产33万吨电解铝,配套年产15万吨阳级碳块的规模。该厂用铝土矿为原料制备铝的工艺流程如下

已知:
①铝土矿的主要成分是?Al2O3,此外还含有少量CuO、Fe2O3等杂质。?
②电解冶炼铝时用碳棒作阳极,用Na3AlF6作助熔剂,电解熔融的Al2O3。
回答下列问题:?
(1)写出铝土矿与?A?溶液反应的化学方程式?________________。
(2)滤渣?C的主要成分为___________;实验室过滤时使用的玻璃仪器有___________。
(3)生成过程中,除CaO、H2O可以循环使用外,还可以循环使用的物质有________?(填化学式)。
(4)写出过量CO2通入滤液C生成D的离子方程式?___________________。
(5)若生产54吨铝,放出平均摩尔质量为36g/mol的气体(经测定气体中不含O2),则消耗阳极______吨。
参考答案:(1)Al2O3+2NaOH=2NaAlO2+H2O
(2)CuO、Fe2O3;烧杯、漏斗、玻璃棒
(3)CaCO3、CO2、NaOH?
(4)CO2+AlO2-+2H2O?=?Al(OH)3↓+HCO3-
(5)24
本题解析:
本题难度:一般
3、填空题 某铜矿石含氧化铜、氧化亚铜、三氧化二铁和大量脉石(SiO2),现采用酸浸法从矿石中提取铜,其流程图如下
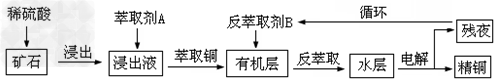
已知:?
①当矿石中三氧化二铁含量太低时,可用硫酸和硫酸铁的混合液浸出铜;
②反萃取后的水层是硫酸铜溶液,Cu2+浓度约为50g/L。
回答下列问题:
(1)矿石用稀硫酸浸出过程中氧化亚铜发生的反应为:Cu2O+2H+==Cu2++Cu+H2O;请写出该过程中发生的另一个氧化还原反应的离子方程式:______________________。
(2)写出用惰性电极电解水层的电解总反应方程式:_________________________。
(3)循环中反萃取剂B的主要成分是___________________。
(4)某铜矿石样品中,若仅含氧化亚铜、三氧化二铁和脉石三种物质。取该矿石样品200.0g,用100mL1.0mol/LH2SO4溶液浸取后,还需加入10mL?1.0mol/L?Fe2(SO4)3溶液才能使铜全部浸出,浸取液经充分电解后可得到?6.4gCu。求铜矿石样品中氧化亚铜和氧化铁的质量分数?
参考答案:(1)Cu+2Fe3+==2Fe2++?Cu2+
(2)2CuSO4?+?2H2O O2↑+?2Cu?+?2H2SO4
O2↑+?2Cu?+?2H2SO4
(3)H2SO4
(4)Cu2O:3.6%?;Fe2O3:3.2%
本题解析:
本题难度:一般
4、填空题 分析下面两个案例并回答有关问题。
(1)某城镇生产、生活的分布情况如下图所示,河流中W、X、Y、Z处某次水样抽测结果如下表所示。
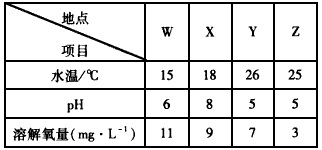
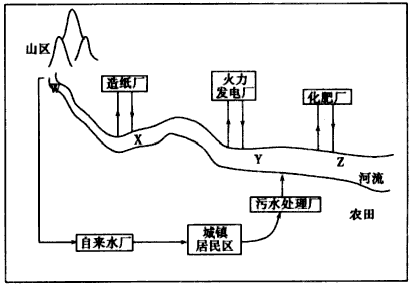
①导致X、Y处水样pH变化的原因可能是__________________,
②Z处鱼类大量减少,产生这种现象的原因可能是________________。
(2)某地区已探明蕴藏有丰富的赤铁矿(主要成分为Fe2O3,还含有SiO2等杂质)、煤矿、石灰石和黏土。拟在该地区建设大型炼铁厂。
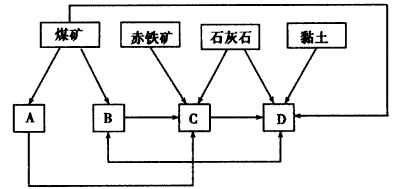
①随着铁矿的开发和炼铁厂的建立,需要在该地区相应建立焦化厂、发电厂、水泥厂等,形成有规模的工业体系。据此确定上图中相应工厂的名称A ______、B_________、C_________、D__________;
②以赤铁矿为原料,写出高炉炼铁中得到生铁和产生炉渣的化学方程式_______________________;
③从“三废”利用、环境保护等角度考虑,该地区和企业在生产中应采取的一些措施有(举出2种措施即可)_________________________。
参考答案:(1)①造纸厂排放的碱性污水使X处河水pH升高,火力发电厂净化烟气的酸性废水治理未达标就排放,造成Y处等的河水pH降低(或火力发电厂燃煤产生的SO2会导致酸雨,飘落后使Y处等的河水 pH降低)
②化肥厂、农田及生活污水使Z处河水富营养化,水温较高、适于藻类等水生植物生长,河水中溶解氧被大量消耗,导致鱼类死亡
(2)①发电厂;焦化厂;炼铁厂;水泥厂;②Fe2O3+3CO2 Fe+3CO2、CaCO3+SiO2
Fe+3CO2、CaCO3+SiO2 CaSiO3+CO2↑;
CaSiO3+CO2↑;
③用炼铁厂的炉渣(或CaSiO3)作为水泥厂的原料用发电厂的煤矸石和粉煤灰作为水泥厂的原料将石灰石煅烧成生石灰,用于吸收发电厂和焦化厂燃煤时产生的SO2,减少对空气的污染建立污水处理系统
本题解析:
本题难度:一般
5、填空题 高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下:
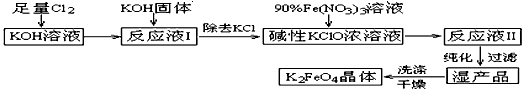
已知:① 2KOH + Cl2 → KCl + KClO + H2O(条件:温度较低)
② 6KOH + 3Cl2 → 5KCl + KClO3 + 3H2O(条件:温度较高)
③ 2Fe(NO3)3 + 2KClO + 10KOH → 2K2FeO4 + 6KNO3 + 3KCl + 5H2O
回答下列问题:
(1)该生产工艺应在__________(填“温度较高”或“温度较低”)情况下进行;
(2)写出工业上制取Cl2的化学方程式________________;
(3)K2FeO4具有强氧化性的原因___________________________;
(4)配制KOH溶液时,是在每100 mL水中溶解61.6 g KOH固体(该溶液的密度为1.47 g/mL),它的物质的量浓度为_________________;
(5)在“反应液I”中加KOH固体的目的是__________________:
A.与“反应液I”中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供反应物
D.使副产物KClO3转化为KClO
(6)从“反应液II”中分离出K2FeO4后,会有副产品___________(写化学式),它们都是重要的化工产品,具体说出其中一种物质的用途_______________________________。
参考答案:
(1)温度较低
(2)2NaCl + 2H2O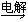 2NaOH + H2↑ + Cl2↑
2NaOH + H2↑ + Cl2↑
(3)Fe元素的化合价显+6价,易得电子
(4)10 mol/L
(5)AC
(6)KNO3、KCl;KNO3可用于化肥,炸药等
本题解析:
本题难度:一般