��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� �á�˫���š���������������ԭ��Ӧ�ĵ���ת�Ʒ�����Ŀ����ָ��������ʣ�
��1��CuO+H2?
Cu+H2O? ?��ԭ��______����������______��______��
��2��2Na+2H2O=2NaOH+H2��?��������______����ԭ����______��______��
�ο��𰸣���1��CuO+H2??��?.?Cu+H2O�У�HԪ�صĻ��ϼ����ߣ�H2Ϊ��ԭ����H2OΪ���������˫���š���ʾ����ת�Ʒ�����ĿΪ
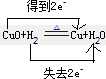
��
�ʴ�Ϊ��H2��H2O��

��
��2��2Na+2H2O=2NaOH+H2���У�HԪ�صĻ��ϼ۽��ͣ�H2OΪ��������H2Ϊ��ԭ�����˫���š���ʾ����ת�Ʒ�����ĿΪ
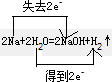
��
�ʴ�Ϊ��H2O��H2��

��
���������
�����Ѷȣ���
2��ѡ���� ���·�Ӧ�����ںϳɵ��ӡ��մɹ�ҵ���õĵ�������AlN��Al2O3+N2+3C
2AlN+3CO�������й�˵����ȷ���ǣ�������
A���������е�Ԫ�ػ��ϼ�Ϊ-3
B���÷�Ӧ�У�ÿ����NA��N��N������ת��Ϊ3mol
C���÷�Ӧ�У�Al2O3����������N2��C�ǻ�ԭ��
D���÷�Ӧ������CO�Ļ�ԭ��
�ο��𰸣�A��NԪ�صķǽ�����ǿ����Ԫ����+3�ۣ������������ϼ۵Ĵ�����Ϊ0��AlN��NΪ-3�ۣ���A��ȷ��
B�����ݷ�ӦAl2O3+N2+3C?����?.?2AlN+3CO����Ԫ�ػ��ϼ۽��ͣ�̼Ԫ�ػ��ϼ����ߣ�ÿ����NA��N��N������ת��Ϊ6mol����B����
C��Al2O3+N2+3C?����?.?2AlN+3CO�У�̼Ԫ�صĻ��ϼ���0���ߵ�+2�ۣ���Ԫ�صĻ��ϼ���0����Ϊ-3�ۣ��ڵ������ĺϳɷ�Ӧ�У�N2����������C�ǻ�ԭ������C����
D����Ԫ�صĻ��ϼ���0����Ϊ-3�ۣ�̼Ԫ�ػ��ϼ����ߣ�̼�Ƿ�Ӧ�Ļ�ԭ������D����
��ѡA��
���������
�����Ѷȣ���
3��ѡ���� ��Ȼ���д��ڵ�Ԫ�ش���Ի���̬���ڣ�����������������������Ҫ����ʣ����������������ȣ����룬�����ijԪ���ɻ���̬��Ϊ����̬�����Ԫ�أ�������
A��������
B���п��ܱ�������Ҳ�п��ܱ���ԭ
C������ԭ
D����Ԫ�ؼȲ�������Ҳ������ԭ
�ο��𰸣�A�����ܱ���ԭ����Fe+Cu2+=Fe2++Cu����A����
B��ijԪ���ڻ�ѧ��Ӧ��������̬��Ϊ����̬���緢��Fe+Cu2+=Fe2++Cu����ԭ���緢��Cl2+S2-=2Cl-+S������������B��ȷ��
C�����ܱ���������Cl2+S2-=2Cl-+S����C����
D��Ԫ���ڻ�ѧ��Ӧ��������̬��Ϊ����̬�����ϼ�һ�������仯����Ԫ��һ����������ԭ����D����
��ѡB��
���������
�����Ѷȣ���
4��ѡ���� ����ͭ��������ӻ�ͭ��ʼ����ͭ��ı��չ�������Ҫ��Ӧ֮һ�Ļ�ѧ����ʽΪ2CuFeS2+O2�T��+2FeS+SO2������˵������ȷ���ǣ�������
A������ʽ����ȱ����ӦΪ?Cu2S
B��O2ֻ��������
C��SO2?���������������ǻ�ԭ����
D������?1?mol?SO2���ɣ���Ӧ����?4?mol?����ת��
�ο��𰸣�A����ѧ��Ӧ��ѭ�����غ㶨�ɣ���Ԫ�������غ��֪����Ӧ�Ļ�ѧ����ʽΪ2CuFeS2+O2�TCu2S+2FeS+SO2������ʽ����ȱ����ӦΪCu2S����A��ȷ��
B����Ӧ��O2��OԪ�صĻ��ϼ�ֻ���ͣ����ڷ�Ӧ��ֻ�õ����ӣ�����Ϊ�����ԣ�Ϊ����������B��ȷ��
C���ɻ��ϼۿ�֪��CuFe-2S2��+4SO2��0O2��S-2O2��SO2���������������ǻ�ԭ�����C��ȷ��
D����CuFe-2S2��+4SO2��֪������1molSO2���ɣ���Ӧ����6mol?����ת�ƣ���D����
��ѡD��
���������
�����Ѷȣ�һ��
5��ѡ���� �����ڷ�Ӧ�пɱ��������ԡ���ԭ�ԡ����ԡ����Եȣ����淽��ʽ�л��ߵ����ʣ�����ͬһ��Ӧ��ͬʱ�����������ֻ������������ʵ��У�������
��8NH3+3Cl2=6NH4Cl+N2
��3FeO+10HNO3��ϡ��=3Fe��NO3��3+NO��+5H2O
��C+2H2SO4��Ũ��
CO2��+2SO2��+2H2O
��2Na2O2+2H2O=4NaOH+O2��
A���٢�
B���٢�
C���ڢ�
D���ڢ�
�ο��𰸣����������Ļ��ϼ۽��ͣ���������ֻ���������ԣ��ʲ�ѡ��
���������е�Ԫ�ز��ֻ��ϼ۽��ͣ����ֲ��䣬����������������Ժ����ԣ���ѡ��
������������Ԫ�ػ��ϼ۽��ͣ���������ֻ���������ԣ��ʲ�ѡ��
���й�����������Ԫ�ز��ֵõ��ӻ��ϼ۽��ͣ�����ʧ���ӻ��ϼ����ߣ����Թ������Ƽ������������л�ԭ�ԣ���ѡ��
��ѡD��
���������
�����Ѷȣ�һ��