微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 将4 mol SO3气体和4 molNO置于2L容器中,一定条件下发生如下可逆反应(不考虑NO2和N2O4之间的相互转化):2SO3(g) 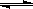 2SO2+O2、2NO+O2
2SO2+O2、2NO+O2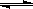 2NO2
2NO2
⑴当上述系统达到平衡时,O2和NO2的物质的量分别为n(O2)="0.1" mol、n(NO2)="3.6" mol,则此时SO3气体的物质的量为 。
⑵当上述系统达到平衡时,欲求其混合气体的平衡组成,则至少还需要知道两种气体的平衡浓度,但这两种气体不能同时是SO3和 ,或NO和 (填它们的分子式)。
⑶在其它条件不变的情况下,若改为起始时在1 L容器中充入2 molNO2和2 molSO2,则上述两反应达到平衡时,c(SO2)平= mol/L。
参考答案:⑴0.2 mol ⑵SO2、NO2 ⑶1.9
本题解析:(1)NO2的物质的量是3.6mol,则消耗氧气的物质的量是1.8mol,所以最初生成的氧气是1.9mol,则分解的三氧化硫是3.8mol,所以平衡时三氧化硫的物质的量是0.2mol。
(2)根据原子守恒可知,两种气体一定不能同时是三氧化硫和二氧化硫,以及NO和NO2。
(3)根据题意可知,此时平衡一定是等效的,所以平衡时SO2的浓度还是1.9mol/L。
本题难度:一般
2、选择题 能够充分说明在恒温下的密闭容器中,反应2SO2+O2=2SO3已达平衡状态的标志是
A.容器中SO2、O2、SO3的物质的量之比为2:1:2
B.SO2和SO3的物质的量浓度相等
C.单位时间内生成2molSO3时,即消耗1molO2
D.反应容器内压强不随时间变化而变化
参考答案:D
本题解析:略
本题难度:简单
3、选择题 在不同条件下分别测得反应2SO2+O2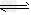 2SO3的化学反应速率,其中表示该反应进行的最快的是
2SO3的化学反应速率,其中表示该反应进行的最快的是
[? ]
A.v(SO2)=4?mol/(L・min)?
B.v(O2)=3?mol/(L・min)
C.v(SO2)=0.1?mol/(L・s)?
D.v(O2)=0.1?mol/(L・s)
参考答案:D
本题解析:
本题难度:简单
4、选择题 对可逆反应:A(g) + B(s)  ?C(s) + D(g);(正反应吸热)。下图所示为正逆反应速率(v)与时间(t)关系的示意图,如果在t1时刻改变以下条件:(?)
?C(s) + D(g);(正反应吸热)。下图所示为正逆反应速率(v)与时间(t)关系的示意图,如果在t1时刻改变以下条件:(?)
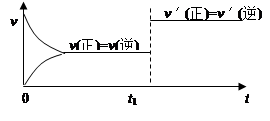
①加入A;②加入催化剂;③加压;④升温;⑤减少C,符合图示的条件是
A.②③
B.①②
C.③④
D.④⑤
参考答案:A
本题解析:由图像可知改变条件后反应速率增加但平衡不移动。加入A,速率加快,平衡向右移动;加入催化剂,速率加快,平衡不移动;B、C是固体,A、D是气体,加压速率加快,平衡不移动;升高温度,速率加快,平衡向右移动;C是固体,减少C,速率减小,平衡不移动。
点评:本题要同时考虑速率加快和平衡不移动,否则容易误认为⑤也正确。
本题难度:一般
5、填空题 目前工业上有一种方法是用CO2来生产燃料甲醇。
CO2(g)+3H2(g)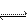 CH3OH(g)+H2O(g)?ΔH=-49.0kJ/mol,为探究反应原理,现进行如下实验:
CH3OH(g)+H2O(g)?ΔH=-49.0kJ/mol,为探究反应原理,现进行如下实验:
在体积为1 L的密闭容器中,充入1mol CO2和4 mol H2,一定条件下发生反应:测得CO2和CH3OH(g)的浓度随时间变化如图所示。

(1)从反应开始到平衡,氢气的平均反应速率v(H2)=?mol/(L・min)。
(2)该反应的平衡常数表达式为?。
(3)下列措施中能使n(CH3OH)/n(CO2)增大的是?。
A.升高温度
B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离
D.再充入1 mol CO2和4 mol H2
 mol CH3OH和1 mol H2O,为了使反应达到的化学平衡和上述一样,则起始还需加入H2的物质的量为?。
mol CH3OH和1 mol H2O,为了使反应达到的化学平衡和上述一样,则起始还需加入H2的物质的量为?。