��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��10�֣���֪����A��B��C��D�������ʾ�����Ԫ��X,�еĻ��п��ܺ���Ԫ��Y��Z����Ԫ��Y��X��Z��ԭ���������ε�������X��A��B��C��D���������ж�������������ϼۡ��������µ���A��ij�ֳ���һԪǿ����Һ��Ӧ���ɵõ�B��C���ܻ�����D���ȷֽ⣬���Ƶ�Ԫ��Y�ĵ��ʡ��Ը������������ش�
��1��д��A��B��C��D�Ļ�ѧʽ:��A_______B_______C_______D______��
��2��д���ۡ����е�������ѧ����ʽ��
�ۣ�?�� ?��
�ο��𰸣�Cl2? KCl? KClO? KClO3
����������������֪��XԪ�ؾ��ж��ּ�̬������4�֣����ɵ�XԪ��һ��Ϊ�ǽ���Ԫ�أ��ڷǽ���Ԫ�ص���������ij�ֳ���һԪǿ����Һ��Ӧ������ΪCL2,��XԪ��ΪCLԪ�ء�������D���ȷֽ⣬�ֺ�CLԪ�أ�����ΪKCLO3����B��C��ΪKCL��KCLO�е�һ�֣�����������A:CL2? B��CΪKCL��KCLO? D:KCLO3
��CL2+2NaOH=NaCL+NaCLO+H2O;��2KCLO3=====2KCL + 3O2��
�����Ѷȣ�һ��
2������� A��B��C��D��E��F���ֵ�ת����ϵ��ͼ������AΪӦ����㷺�Ľ�����������E���������ᷴӦ��������NaOH��Һ��Ӧ��X��Y����ͬһ���ڣ��Һ˵�������4��
����ת����ijЩ��Ӧ����δָ������ش��������⣺
��1��ָ��C�еĻ�ѧ�����ͣ�______��D�Ļ�ѧʽΪ______��Ԫ��X��Y��ԭ�Ӱ뾶��С˳����______����Ԫ�ط��ű�ʾ����
��2��E��NaOH��Һ��Ӧ�����ӷ���ʽΪ______��
��3����ӦA+H2O��C+D�Ļ�ѧ����ʽΪ______��
��4��F�ܴٽ�H2O�ĵ��룬��ԭ����______�������ӷ���ʽ��ʾ����
��5��250Cʱ����pH=1��������pH=12��NaOH��Һ�������1��9��ϣ����ʱ��Һ����仯���Բ��ƣ�����Ͼ��Ⱥ�������Һ��pH=______��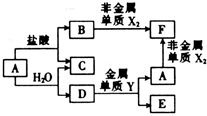
�ο��𰸣����������Ϣ������E���������ᷴӦ��������NaOH��Һ��Ӧ������֪EΪ��������AΪӦ����㷺�Ľ��������ܺ�ˮ��Ӧ����AӦΪ����BΪ�Ȼ�������CΪ������DΪFe3O4��YΪ����
��1���ǽ�������X2Ϊ������FΪ�Ȼ����������еĻ�ѧ���Ƿǽ���Ԫ��֮�����ɵĽ���Ϊ���ۼ�������Ԫ�����ڱ���ͬ����Ԫ��ԭ�Ӱ뾶���μ�С�ĵݱ���ɣ��뾶Al��Cl���ʴ�Ϊ�����ۼ���Fe3O4��Al��Cl��
��2���������������������ǿ�Ӧ�õ���Ӧ���κ�ˮ�����ӷ���ʽΪ��Al2O3+2OH-=2AlO2-+H2O���ʴ�Ϊ��Al2O3+2OH-=2AlO2-+H2O��
��3�����ڸ������ܺ�ˮ���������û���Ӧ������ʽΪ��Fe+4H2O��g��??����?.??Fe3O4+4H2���ʴ�Ϊ��Fe+4H2O��g��?����?.??Fe3O4+4H2��
��4���Ȼ����е�Fe3+��ˮ�⣬��ˮ����ζ�ˮ�ĵ�����ٽ����ã�ˮ�ⷽ��ʽΪ��3Fe3++3H2O?

?Fe��OH��3+3H+���ʴ�Ϊ��3Fe3++3H2O?

?Fe��OH��3+3H+��
��5����ǿ���ǿ�������ֱ�Ϊ1L��9L��ǿ���ǿ���Ϻ���Һ��[H+]=�����������ӵ����ʵ���-���������������������ʵ�����Һ�������=0.1mol/l��1L-0.01mol/l��9L10L=0.001mol/l��PH=3���ʴ�Ϊ��3��
���������
�����Ѷȣ�һ��
3������� ��15�֣�A��B��C��X����ѧ��ѧ�������ʣ����ɶ�����Ԫ����ɣ�ת����ϵ��ͼ��ʾ��������������ֲ�ͬ����ش�
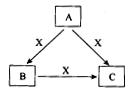
��1����A��B��C�о���ͬһ�ֳ����ǽ���Ԫ�أ���A��C��ˮ
��Һ��Ͽɵ�B�ij���
��A��B��C�к��е�ͬһ�ֳ����ǽ���Ԫ��Ϊ___________��
��д��A��C��ˮ��Һ������ɳ���B�Ļ�ѧ��Ӧ����ʽ
Ϊ?��
��2����AΪ��̬�ǽ������ʣ�A��XͬΪ��������Ԫ�أ����³�ѹ��CΪ��ɫ���壬B�����и�ԭ��������Ϊ8e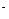 �ṹ��
�ṹ��
��B�ĵ���ʽΪ_____________��
��C��ˮ���ҷ�Ӧ���������ֳ����ᣬ��Ӧ�Ļ�ѧ����ʽΪ_____________ ��
��
��3����A��B��C����ɫ��Ӧ���ʻ�ɫ��ˮ��Һ��Ϊ���ԣ���C�ӵ������У�����ɫ��ζ������X������
��A�������еĻ�ѧ����_____________��
�ڽ�����Xͨ��100mL 3 mol��L? A��ˮ��Һ�У���������Һ��������Һ��ϣ�д�����ʱ��Ӧ�����ӷ���ʽ___________��
����Ȼ���д���B��C��H2O��һ�������ᾧ���ɵĹ��塣ȡһ�����ù�������ˮ���100mL��Һ����������н��������ӵ�Ũ��Ϊ0��5 mol��L����ȡ��ͬ�����Ĺ�����������أ�ʣ����������Ϊ__________ g��
�ο��𰸣���15�֡�ÿ��2�֣�
��1������?��2H2S+SO2=3S��+2H2O
��2����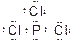 ?��PCl5+4H2O=H3PO4+5HC1��
?��PCl5+4H2O=H3PO4+5HC1��
��3�������Ӽ�?���ۼ�
�� 3HCO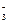 +Al3+=Al��OH��3��+3CO2����
+Al3+=Al��OH��3��+3CO2����
��2��65 g?��3�֣�
�����������
�����Ѷȣ�һ��
4������� B��D��EΪ��ѧ��ѧ�����ĵ��ʣ�����D��EΪ��������һ��������C��D���ܷ�����Ӧ��������ת����ϵ����ͼ��
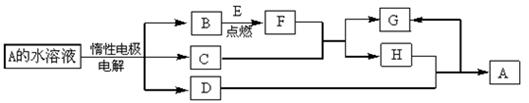
(1)B��ͬ�������������Ϊ��_____________��H�Ļ�ѧʽΪ��_____________��
(2)��֪1g E��������ȼ�շų�������ΪQ kJ����д����ʾEȼ���ȵ��Ȼ�ѧ����ʽ_____________��
(3)�ö��Ե缫���A ��Һ��������ӦʽΪ��_____________��
(4)����H��G�Ļ����Һ�к���G�������ӵ��Լ������ǣ�_____________��
a.��ˮ��KSCN��Һ? b.����������Һ? c. ����KMnO4��Һ
(5)�ö��Ե缫���һ��Ũ�ȵ�A��Һ��ͨ��һ��ʱ�����������Һ�м���8.0g A���������ǡ�ûָ������ǰ��Ũ�Ⱥ�pH�����������ת�Ƶ��ӵ����ʵ���Ϊ_____________mol, �ռ�����״���µ��������Ϊ_____________��
�ο��𰸣�(1)����? (2��)? Fe2��SO4��3?(2��)
(2)Fe��s����2/3O2(g)=1/3Fe3O4��s����H����56QkJ/mol? (2��)
(3)4OH����4e����2H2O ��O2��(2��)? (4)c? (2��)?
(5)0.2mol (2��)? 1.12L(2��)
�����������
�����Ѷȣ�һ��
5������� �� I��ij��ɫϡ��ҺX�У����ܺ����±����������е�ij���֣�
| ������ | CO32-��SiO32-��AlO2-��Cl-
������
Al3+��Cu2+��Mg2+��NH4+��Na+
|
��ȡ����Һ�����������м���ij�Լ�Y���������������ʵ�����n��������Լ�Y�����V���Ĺ�ϵ��ͼ��ʾ��
��1����Y�����ᣬ����Һ�к��еĽ�����������______��ab�η�����Ӧ�������ӷ���ʽΪ______��Oa���ϱ��вμӷ�Ӧ�����ӵ����ʵ���֮��Ϊ��______[Ҫ�������ӷ��ţ���n��Na+��]��
��2����Y��NaOH��Һ����bc�η�Ӧ�����ӷ���ʽΪ______�������������ӵ�ˮ�����أ�����H+��OH-Ӱ�죬����Һ��ֻ�����������ӣ������ǵ����Ӹ�����Ϊ______[����������ǰ���������ں���ǰ���ͼ��ں��˳������]��
�� II����Ϊ��IVA��Ԫ�أ����ĵ��ʺͻ�������ijЩ���ʵĻ�ѧ����������������֮������֪��Ԫ�ؾ����������ʣ���Sn4++Sn�T2Sn2+����2Sn2++O2+4H+�T2Sn4++2H2O����2H++SnO22-?Sn��OH��2?Sn2++2OH-���Իش�
��1�����������ᣬ����Ӧ�����Һ��ͨ���������йط�Ӧ������������Ӧ�仯����д���йط�Ӧ�Ļ�ѧ����ʽ��______��______��
��2������1������Һ���ɺ�����������ù��壬�仯����������FeCl3��Һ��Ӧ�ı仯�������õ��Ĺ��������ǣ�����ʽ��______��
��3��������SnCl2��Һ������ļ���Һ��Ӧ�ķ�����Sn��OH��2���ü���______��

�ο��𰸣���Һ��ɫ˵����Һ�в���ͭ���ӣ�
��1�����Y�����ᣬ����Һ�м����ᣬ�����ɳ�������a-b��ʱ�������������仯�������̼������ӷ�Ӧ�������壬����Һ�в���þ���ӡ������ӣ���b-c��ʱ�������������٣����ֳ��������ᷴӦ�����ֳ����������Ӧ��˵����Һ���й�������Ӻ�ƫ��������ӣ���������Ӻ�笠�������˫ˮ�⣬������Һ�к��е��������������ӣ�ͨ�����Ϸ���֪����Һ�к��е��������������ӣ�ab�η�����Ӧ��̼������Ӻ������ӷ�Ӧ���ɶ�����̼��ˮ�����ӷ���ʽΪ��CO32-+2H+=H2O+CO2��������ͼ��֪���������������ᷴӦ��Ҫ1V���ᣬƫ��������Ӻ�������Ӻ����ᷴӦ��Ҫ����4V���ᣬ�йط�Ӧ����ʽΪ��AlO2-+H++H2O=Al��OH��3����SiO32-+2H+=H2SiO3 ����Al��OH��3+3H+=Al3++3H2O�����ݷ���ʽ֪��SiO32-����H2SiO3��Ҫ����������AlO2-����Al��OH��3��Ҫ��������֮��(4-13)13=11��1������AlO2-+H++H2O=Al��OH��3����SiO32-+2H+=H2SiO3 ��֪����n��SiO32-����n��AlO2-��=4-132��13=11��2��
�ʴ�Ϊ��Na+��CO32-+2H+=H2O+CO2����n��SiO32-����n��AlO2-��=11��2��
��2����Y���������ƣ�����Һ�м�����������Һ�������ɳ�������a-b��ʱ�������������仯���������ƺ�笠����ӷ�Ӧ�������壻��b-c��ʱ�������������٣����ֳ������������Ʒ�Ӧ�����ֳ�������Ӧ��˵����Һ�����������Ӻ�þ���ӣ�����Һ�в�����������ӡ�̼������Ӻ�ƫ��������ӣ�������Һ�к��е��������������ӣ�
Y��NaOH��Һ����bc���������������������Ʒ�Ӧ����ƫ�����ƺ�ˮ�����ӷ���ʽΪ��Al��OH��3+OH-=AlO2-+2H2O��
��笠�������Ҫ�������Ƶ������2V�������������������Ʒ�Ӧ��Ҫ�������Ƶ������1V������������������Ҫ�������Ƶ������3V������������þ��Ҫ�������Ƶ������1V����n��Al3+����n��Mg2+����n��NH4+��=1��12��2=2��1��4����Һ��������������������֪��n��Al3+����n��Mg2+ ����n��NH4+����n��Cl- ��=2��1��4��12����N��Al3+����N��Mg2+ ����N��NH4+����N��Cl- ��=2��1��4��12��
�ʴ�Ϊ��Al��OH��3+OH-=AlO2-+2H2O��N��Al3+����N��Mg2+ ����N��NH4+����N��Cl- ��=2��1��4��12��
��II����1���������ᷴӦ���ɶ��Ȼ��������Ȼ��������������������Ȼ�������Ӧ����ʽΪ��Sn+2HCl=SnCl2+H2����SnCl2+Cl2=SnCl4��
�ʴ�Ϊ��Sn+2HCl=SnCl2+H2����SnCl2+Cl2=SnCl4
��2�����Ȼ�����Һ�������ù��������ڸ���������ݶ��ߵ�������֪�����Ȼ�����Һ���ɵõ��������������������õ��Ĺ�����SnO2���ʴ�Ϊ��SnO2��
��3�����������Ϣ֪��Sn��OH��2�������ԣ��ܺ�ǿ�Ӧ��������ȡ������ʱӦ��������������ΪNH3?H2O���ʴ�Ϊ��NH3?H2O��
���������
�����Ѷȣ���