微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 元素在周期表中的位置:
?族?
周期
| IA
| IIA
| IIIA
| IVA
| VA
| VIA
| VIIA
| 0
|
2
| ?
| ?
| ?
| E
| ?
| F
| ?
| ?
|
3
| A
| C
| D
| ?
| ?
| ?
| G
| R
|
4
| B
| ?
| ?
| ?
| ?
| ?
| H
| ?
|
(1)这9种元素中金属性最强的元素是______,化学性质最不活泼的是______(填元素符号,下同);
(2)D元素的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是___________;
(3)A、B、C三种元素按原子半径由大到小的顺序排列为___________;
(4)F元素氢化物的化学式是_________,该氢化物在常温下跟B发生反应的化学方程式是?,所得溶液的PH_______7;
(5)H元素跟A元素形成的化合物的化学式是_______,高温灼烧该化合物时,火焰呈现_______色;
(6)G元素和H元素两者核电荷数之差是_________
参考答案:(每空2分)(1)K?,Ar?(2)Al(OH)3+ OH -= AlO2-+2H2O? (3) K> Na> Mg
(4)H2O? 2K+2H2O=2KOH+H2↑ >? (5) NaBr?黄?(6) 18
本题解析:(1)同周期自左向右金属性逐渐减弱,同主族自上而下金属性逐渐增强,据此可知这9种元素中金属性最强的元素是B即K元素。稀有气体元素的化学性质最不活泼,所以是R,即Ar元素。
(2)D是Al,其最高价氧化物对应的水化物是氢氧化铝,属于两性氢氧化物,则与氢氧化钠反应的离子方程式是Al(OH)3+ OH -= AlO2-+2H2O。
(3)同周期自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐增大,则A、B、C三种元素按原子半径由大到小的顺序排列为K>Na>Mg。
(4)F元素是氧元素,则其氢化物的化学式是H2O。K是活泼的碱金属,极易和水反应,生产氢氧化钾和氢气,反应的化学方程式是2K+2H2O=2KOH+H2↑。所得氢氧化钾是强碱,溶液显碱性,pH大于7。
(5)H元素与A元素分别是Br和Na,二者形成的化合物的化学式是NaBr,焰色反应显黄色。
(6)G元素是氯元素和H元素两者核电荷数之差是35-17=18。
点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,侧重对学生基础知识的巩固和训练,有利于提高学生的逻辑推理能力和应试能力。本题主要是元素“位、构、性”三者关系的综合考查,比较全面考查学生有关元素推断知识和灵活运用知识的能力,考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。
本题难度:一般
2、选择题 a、b、c、d、e是同周期的五种元素,a和b的最高价氧化物的水化物显碱性,且将a、b相连浸入稀硫酸中时,a溶解而b表面有气泡产生;c和d的气态氢化物的还原性d>c,五种元素的原子,得失电子后所形成的简单离子中,e的离子半径最小,则它们的原子序数由小到大的顺序是(? )
A.a、b、e、d、c
B.e、d、a、b、c
C.b、a、e、d、c
D.a、b、d、c、e
参考答案:A
本题解析:题中a溶解而b表面有气泡产生,则原子序数a<b,且都能失去电子,通过c和d的气体氢化物的还原性比较,确定原子序数d>c,e的离子半径最小,则原子序数小于b,所以A对。
本题难度:一般
3、填空题 A、B、C、D四种元素的原子序数均小于18,其最高正价数依次为1,4,5,7,已知B的原子核外次外层电子数为2。A、C原子的核外次外层电子数为8。D元素的最高价氧化物对应的水化物是已知含氧酸中最强酸,则:
(1)A、B、C、D的名称分别是________、___?_____、___?___、__?______。
(2)A的离子结构示意图是_?__?____,C的原子结构示意图是___?_____。
参考答案:(1)钠、碳、磷、氯?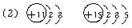
本题解析:D元素的最高价氧化物对应的水化物是已知含氧酸中最强酸,则D是氯元素。B的原子核外次外层电子数为2,且最高价是+4价,因此B是碳元素。A、C原子的核外次外层电子数为8,则根据A和C的最高价分别是+1、+5价,所以A是钠元素,C是磷元素。
点评:该题是高考中的常见题型,属于基础性试题的考查。试题基础性强,侧重对学生基础知识的巩固和训练,有利于提高学生的逻辑推理能力和应试能力。本题主要是元素“位、构、性”三者关系的综合考查,比较全面考查学生有关元素推断知识和灵活运用知识的能力。考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。
本题难度:一般
4、选择题 2011年3月11日,日本发生9.0级地震并引发海啸,福岛核电站反应堆发生爆炸产生核泄漏。 I是核裂变产物之一,可以通过测定大气或水中I的含量来检测核电站是否发生放射性物泄漏。下列有关I的叙述中错误的是
A.I与I的性质相同
B.I的原子序数为53
C.I 与I互为同位素
D.I的原子核内中子数多于核外电子数
参考答案:A
本题解析:I与I为同位素,物理性质不同,化学性质相似。I的原子序数为53,中子数为78,核外电子数为53,I的原子核内中子数多于核外电子数。
本题难度:一般
5、选择题 下列各组中,属于同位素的是(?)
A.H2、D2、T2
B.金刚石和足球烯C60
C.16O和18O
D.H2O和D2O
参考答案:C
本题解析:具有相同的质子数,不同中子数的同一种元素的不同核素互称为同位素。A中是单质分子,不是同位素。B中属于同一种元素形成的不同单质,是同素异形体。D代表水分子,所以正确的答案是C。
本题难度:一般