��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����ԭ�ӹ����˵����ȷ���ǣ�������
A����������ԭ�Ӳ�ȡsp3�ӻ���ʽ�ɼ��ķ����伸�ι��Ͷ�����������
B��CH4�����е�sp3�ӻ��������4��Hԭ�ӵ�1s�����Cԭ�ӵ�2p�������������γɵ�
C��sp3�ӻ��������ͬһ��ԭ�������������s�����p�����������γɵ�һ��������ͬ���¹��
D����AB3�͵Ĺ��ۻ����������ԭ��A������sp3�ӻ���ʽ�ɼ�
�ο��𰸣�C
���������
�����Ѷȣ�һ��
2������� ��ͼ��ʾΪѪ�쵰�ͼ��쵰�Ļ��Բ���--Ѫ���صĽṹʽ��
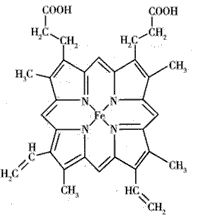
��ش��������⣺
(1)Ѫ�����к���C��H��O��N��Fe����Ԫ�أ�C��N��O����Ԫ�صĵ�һ��������С�����˳����___ д����̬Feԭ�ӵĺ�������Ų�ʽ___��
(2)Ѫ������Nԭ�ӵ��ӻ���ʽΪ___��������ķ������á��������Fe2+����λ����

(3)���Цġ��á�������ͬ�������壬�þ��徧���������е���ԭ����Ϊ___���ġ������־�������ԭ�ӵ���λ��֮��Ϊ____��

�ο��𰸣�(1)C< O <N ��[Ar]3d64s2
(2) sp2��sp3? ��
(3)4��4��3
���������
�����Ѷȣ�һ��
3��ѡ���� ��ϩ�Ʒ���һ�ּ�����ҩ���ṹ��ʽΪ

���������������
[? ]
A. ��ϩ�Ʒӷ�����̼ԭ�ӵ��ӻ���ʽ��sp2��sp3����
B. ��ϩ�Ʒӷ��������е�̼ԭ�Ӷ�������һ��ƽ����
C. ��ϩ�Ʒӷ��ӿ�ʹ��ˮ����������Һ��ɫ
D. 1mol��ϩ�Ʒӷ�����������һ����������ȫ��Ӧʱ����������6 molH2
�ο��𰸣�D
���������
�����Ѷȣ�һ��
4������� ԭ������С��36��X��Y��Z��W����Ԫ�أ�����X���γɻ�����������Ԫ�أ�Yԭ�ӻ�̬ʱ���������������ڲ��������2����Zԭ�ӻ�̬ʱ2pԭ�ӹ������3��δ�ɶԵĵ��ӣ�W��ԭ������Ϊ29��
�ش��������⣺
��1��Y2X2������Yԭ�ӹ�����ӻ�����Ϊ______��1mol?Y2X2���ЦҼ�����ĿΪ______��
��2��������ZX3�ķе�Ȼ�����YX4�ĸߣ�����Ҫԭ����______��
��3��Ԫ��Y��һ����������Ԫ��Z��һ�������ﻥΪ�ȵ����壬Ԫ��Z������������ķ���ʽ��______��
��4��Ԫ��W��һ���Ȼ��ᄃ��ľ����ṹ��ͼ��ʾ�����Ȼ���Ļ�ѧʽ��______��������Ũ���ᷢ����������ԭ��Ӧ�����������H2WCl3����Ӧ�Ļ�ѧ����ʽΪ______��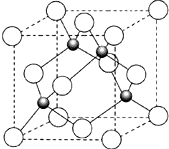
�ο��𰸣�ԭ������С��36��X��Y��Z��W����Ԫ�أ�����X���γɻ�������������Ԫ�أ���X��HԪ�أ�
Yԭ�ӻ�̬ʱ���������������ڲ��������2��������������������8�������ڲ������ֻ����2����Y��CԪ�أ�
Zԭ�ӻ�̬ʱ2pԭ�ӹ������3��δ�ɶԵĵ��ӣ���Z��NԪ�أ�W��ԭ������Ϊ29����W��CuԪ�أ�
��1��Y2X2����Ȳ������ʽΪC2H2��̼��ԭ��֮����ڦҼ���̼̼�����к���һ���Ҽ�������ÿ��̼ԭ�Ӻ���2���Ҽ�����ȡsp�ӻ���һ����Ȳ�����к���3���Ҽ�������1mol?Y2X2���ЦҼ�3mol��3��6.02��1023����
�ʴ�Ϊ��sp�ӻ���3mol��3��6.02��1023����
��2��Nԭ�ӵ縺�Խϴ�Cԭ�ӵ縺�Խ�С�������������д����������������в������������Ĵ��ڵ��°����ķе���ڼ��飬�ʴ�Ϊ��NH3���Ӵ��������
��3��CO2��N2O��ԭ�Ӹ�����ȡ��۵�������ȣ������ǵȵ����壬�ʴ�Ϊ��N2O��
��4�����þ�̯��֪���þ����к�ɫ�����=4����ɫ�����=18��8+12��6=4����ɫ��Ͱ�ɫ��ĸ���֮��=4��4=1��1�����Ը����ʵĻ�ѧʽ��CuCl��������Ũ���ᷢ����������ԭ��Ӧ�����������H2CuCl3������CuCl��H2CuCl3֪����Ԫ�ء�ͭԪ�صĻ��ϼ۲��䣬���Ը÷�Ӧ����������ԭ��Ӧ���ǻ��Ϸ�Ӧ�������䷴Ӧ����ʽΪCuCl+2HCl�TH2CuCl3����CuCl+2HCl�TH2[CuCl3]��
�ʴ�Ϊ��CuCl��CuCl+2HCl�TH2CuCl3����CuCl+2HCl�TH2[CuCl3]��
���������
�����Ѷȣ�һ��
5������� ����ѡһ������ѧ�����ʽṹ�����ʡ�
����ͭ�ĵ����Խ����������������ڵ�����ҵ��
��1���ý��������۽��ͽ���ͭ�ܵ����ԭ��_______________��
��2��д��ͭ�Ļ�̬ԭ�Ӻ�������Ų�ʽ_______________��
��3��ͭ��ij���Ȼ��ᄃ��ľ����ṹ��ͼ��ʾ�����Ȼ���Ļ�ѧʽΪ_______________��

��4��������ͭ��Һ�м��������ˮ��Ȼ����������Ҵ�����Һ����������ɫ��[Cu(NH3)4]SO4���塣��������Nԭ�ӵ��ӻ���ʽΪ____________?����������ɫ�����к��еĻ�ѧ������ͨ���ۼ��⣬����_________��___________��
�ο��𰸣���1������ͭ�����еĵ������ڵ糡�������¶����ƶ�������
��2��1s22s22p63s23p63d104s1
��3��CuCl
��4��sp3�����Ӽ���?��λ��
���������
�����Ѷȣ�һ��