微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在一定温度下,反应H2(g)+X2(g) 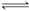 HX(g)的平衡常数为10。若将1.0 mol的HX(g)通入体积为1.0 L的密闭容器中,在该温度时HX(g)的最大分解率接近于( )
HX(g)的平衡常数为10。若将1.0 mol的HX(g)通入体积为1.0 L的密闭容器中,在该温度时HX(g)的最大分解率接近于( )
A.5%
B.17%
C.25%
D.33%
参考答案:B
本题解析:反应H2(g)+X2(g) 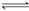 HX(g)中,HX(g)的最大分解率即达到平衡状态;
HX(g)中,HX(g)的最大分解率即达到平衡状态;
根据反应:HX(g) 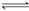 H2(g)+X2(g)
H2(g)+X2(g)
起始浓度? 1? 0? 0
变化浓度? 2x? x? x
平衡浓度 1-2x? x? x
由于反应H2(g)+X2(g)  HX(g)的平衡常数为10,则HX(g)
HX(g)的平衡常数为10,则HX(g)  H2(g)+X2(g)的平衡常数为
H2(g)+X2(g)的平衡常数为 ;所以
;所以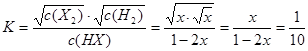 ;解得
;解得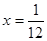 ;在该温度时HX(g)的最大分解率=
;在该温度时HX(g)的最大分解率=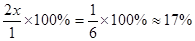
本题难度:一般
2、选择题 已知:A(s)+B(g) 2D(g) ΔH>0,该反应达到平衡后,下列条件的改变有利于平衡向正反应方向移动的是( )
2D(g) ΔH>0,该反应达到平衡后,下列条件的改变有利于平衡向正反应方向移动的是( )
A.升高温度和减小压强
B.降低温度和减小压强
C.降低温度和增大压强
D.升高温度和增大压强
参考答案:A
本题解析:该反应为正向气体分子数增多且反应吸热,因此低压高温有利于平衡正向移动。
本题难度:一般
3、选择题 将固体NH4I置于密闭容器中,在一定温度下发生下列反应:①NH4I(s)  ?NH3(g) + HI(g) ②2HI(g)
?NH3(g) + HI(g) ②2HI(g)  ?H2(g) + I2(g),当反应达到平衡时,c(H2)= 0.25mol/L,c(HI)= 2mol/L,则此温度下反应①的平衡常数为
?H2(g) + I2(g),当反应达到平衡时,c(H2)= 0.25mol/L,c(HI)= 2mol/L,则此温度下反应①的平衡常数为
A.5
B.6.25
C.20
D.25
参考答案:A
本题解析:平衡时c(HI)=2mol?L-1,HI分解生成的H2的浓度为0.25mol?L-1.
NH4I分解生成的HI的浓度为2mol?L-1+2×0.25mol?L-1=2.5mol?L-1,所以NH4I分解生成的NH3的浓度为2.5mol?L-1,
所以反应①的平衡常数k=c(NH3)?c(HI)=2.5mol?L-1×2mol?L-1=5mol2?L-2.
故选A.
本题难度:一般
4、选择题 在密闭容器中通入物质的量浓度均0.1mol・L-1的CH4与CO2,在一定条件下发生反应:
 ,测得CH4的平衡转化率与温度及压强的关系如图5,下列有关说法一定正确的是
,测得CH4的平衡转化率与温度及压强的关系如图5,下列有关说法一定正确的是

A.上述反应的△H>0
B.压强P1>P2>P3>P4
C.1100℃该反应的平衡常数为64mol2・L-1
D.压强为P4时,在Y点:v(正)<v(逆)
参考答案:A
本题解析:A、由图可知随温度升高CH4的平衡转化率增大,即温度升高平衡正向移动,故反应为吸热反应△H>0,正确;B、由方程式可知压强增大平衡逆向进行,CH4的平衡转化率减小,故P4>P3>P2>P1,错误;
C、? CO2 + CH4 2CO + 2H2
2CO + 2H2
始量? 0.1? 0.1? 0? 0
转化量? 0.08? 0.08? 0.16? 0.16
平衡量? 0.02? 0.02? 0.16? 0.16
平衡常数为k=0.162×0.162÷(0.02×0.02)=1.6384
错误;
D、该点处甲烷的转化率低,平衡应正向移动,v(正)>v(逆),错误。
本题难度:一般
5、计算题 在一定条件下,可逆反应A2(g)+B2(g)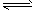 2C(g)在一个容积固定的密闭容器中达到平衡时,测得
2C(g)在一个容积固定的密闭容器中达到平衡时,测得
c(A2)=0.5mol・L-1, c(B2)=0.1mol・L-1,c(C)=1.6mol・L-1。若A2、B2、C的起始浓度分别为
amol・L-1、b mol・L-1、gmol・L-1请确定:
(1)a、g应满足的关系式为_________。
(2)若反应从正反应方向开始进行,当g=_________,a有最大值为_________。
(3)若反应从逆反应方向开始进行,当b=_________,a有最小值为_________。
(4)b的取值范围为________________。
参考答案:(1)a+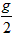 =1.3
=1.3
(2)0;1.3
(3)0;0.4
(4)0≤b≤0.9
本题解析:
本题难度:一般