微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 一定条件下,可逆反应2A(g) B(g)+3C(g),下列四项中处于平衡状态的是(?)
B(g)+3C(g),下列四项中处于平衡状态的是(?)
?
| 正反应速率
| 逆反应速率
|
A
| v(A)=2mol/(L・min)
| v(B)=2mol/(L・min)
|
B
| v(A)=2mol/(L・min)
| v(C)=2mol/(L・min)
|
C
| v(A)=1mol/(L・min)
| v(B)=2mol/(L・min)
|
D
| v(A)=1mol/(L・min)
| v(C)=1.5mol/(L・min)
|
?
参考答案:D
本题解析:可逆反应达到平衡状态时,正逆反应的反应速率相等,即用不同物质表示的化学反应速率之比应等于化学方程式中的化学计量数之比,只有D正确。
本题难度:一般
2、填空题 (12分)在一个2L的密闭容器中,投入反应物,发生反应2SO3(g) 2SO2(g)+O2(g)? ΔH>0,其中SO3的变化如下图所示:
2SO2(g)+O2(g)? ΔH>0,其中SO3的变化如下图所示:
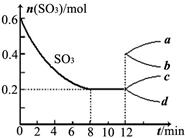
(1)写出该反应的平衡常数表达式并根据8min时到达平衡计算出结果?。
(2)用O2表示0到8min内该反应的平均速率v=?。
(3)能说明该反应已达到平衡状态的是?。
A.v(SO3)=2v(O2) ? B.容器内压强保持不变
C.v(SO2)逆=2v(O2)正?D.容器内密度保持不变
(4)在第12min时,容器压缩到1L,则SO3的变化曲线为?。
A.a? B.b? C.c? D.d
(5)若保持容积不变在第12min时,加入SO3(g),则平衡向?反应方向移动(填“正”或“逆”)。SO3的体积分数?(填“增大”或“减小”)。
参考答案:(1)K= = 0.4?(2)0.0125 mol/(L・min)
= 0.4?(2)0.0125 mol/(L・min)
(3)B、C?(4)C?(5)正?增大
本题解析:(1)K= ,8分钟时c(SO3)=0.1mol/L,则c(SO2)=0.2mol/L,c(O2)=0.1mol/L,所以K=0.4。
,8分钟时c(SO3)=0.1mol/L,则c(SO2)=0.2mol/L,c(O2)=0.1mol/L,所以K=0.4。
(2)v(O2)=
(3)反应前后压强不等,所以可以用压强不再变化判断反应达平衡,v(SO2)逆=2v(O2)正,正逆反应速率相等,可以判断反应达平衡,因此选BC。
(4)容器压缩的瞬间,SO3物质的量不变,随即平衡逆向移动,SO3的物质的量增大,所以c曲线符合。
(5)若保持容积不变在第12min时,加入SO3(g),相当于对体系加压,平衡正向移动,但SO3的体积分数增大。
点评:本题非常基础,只要掌握影响平衡移动的因素即可。
本题难度:一般
3、填空题 (8分)钾是―种活泼的金属,工业上通常用金属钠和氯化钾在高温下反应制取。该反应为:Na(l)+KCl(l)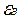 NaCl(l)+K(g)(正反应吸热)
NaCl(l)+K(g)(正反应吸热)
压强(kPa)
| 13.33
| 53.32
| 101.3
|
K的沸点(℃)
| 590
| 710
| 770
|
Ka的沸点(℃)
| 700
| 830
| 890
|
KCl的沸点(℃)
| ?
| ?
| 1437
|
NaCl的沸点(℃)
| ?
| ?
| 1465
|
该反应的平衡常数可表示为:K=c(K),各物质的沸点与压强的关系见上表。
(1)在常压下金属钾转变为气态从反应混合物中分离的最低温度约为?,而反应的最高温度应低于?。
(2)在制取钾的过程中,为了提高原料的转化率可以采取的措施是?。
(3)常压下,当反应温度升高到900℃时,该反应的平衡常数可表示为:K= ?。
?。
参考答案:(1)770℃? 890℃ (2)降低压强或移去钾蒸气?适当升高温度?(3)K=c(K)/c(Na)
本题解析:略
本题难度:一般
4、选择题 在某容积不变的密闭容器中放入一定量的NO2,发生反应2NO2(g)  N2O4(g);ΔH<0,在达到平衡后,若分别单独改变下列条件,重新达到平衡后,能使平衡混合气体平均相对分子质量减小的是? ( )
N2O4(g);ΔH<0,在达到平衡后,若分别单独改变下列条件,重新达到平衡后,能使平衡混合气体平均相对分子质量减小的是? ( )
A.通入N2
B.通入NO2
C.通入N2O4
D.降低温度
参考答案:A
本题解析:容器容积不变,通入氮气,平衡不移动。但由于氮气的相对分子质量小于NO2和N2O4的,所以混合气体平均相对分子质量减小;由于反应物和生成物都只有一种,因此不论再加入NO2还是N2O4,都相当于是增大压强,平衡向正反应方向移动,混合气体平均相对分子质量增大;正反应是放热反应,降低温度平衡向正反应方向移动,混合气体平均相对分子质量增大,答案选A。
本题难度:一般
5、选择题 下列有关化学反应速率的说法中,正确的是?
A.100 mL 2 mol/L的盐酸与锌反应时,加入适量的氯化钠溶液,生成氢气的速率不变
B.用铁片和稀硫酸反应制取氢气,改用铁片和浓硫酸可以加快产生氢气的速率
C.在做草酸与高锰酸钾的反应时,加入少量硫酸锰固体可加快溶液褪色速率
D.汽车尾气中的CO和NO可以缓慢反应生成N2和CO2,若升高温度,则吸热反应速率增大,放热反应速率减小
参考答案:C
本题解析:试题分析:氯化钠溶液和铁不反应,但溶液的体积增加,氢离子的浓度降低,反应速率降低,所以选项A不正确;常温下铁在浓硫酸中发生钝化,得不到氢气,B错误;C中硫酸锰起到催化剂的作用,可以加快反应速率,C正确;只要温度升高,反应速率都是增大的,D不正确,答案选C。
考点:考查外界条件对化学反应速率的影响
点评:该题是高考中的常见题型和重要考点,属于中等难度试题的考查。试题基础性强,侧重对学生基础知识的巩固和训练,主要是考查学生对化学反应速率概念以及外界条件对反应速率影响的熟悉了解程度,旨在考查学生灵活运用基础知识解决实际问题的能力。有利于培养学生的逻辑推理能力和发散思维能力。
本题难度:困难