微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列理解不正确的是( )。
A.化学平衡是一个动态平衡
B.化学平衡研究的对象主要是可逆反应
C.化学反应速率是研究化学反应进行的快慢问题,化学平衡是研究化学反应进行的限度问题
D.化学反应达到平衡时,正反应和逆反应速率相等,是对反应中不同物质而言
参考答案:D
本题解析:化学反应达到平衡时,对同种物质而言,其生成速率和消耗速率相等,D错。
本题难度:简单
2、实验题 以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3・6H2O)的工艺流程如下:
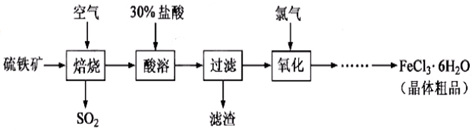
回答下列问题:
(1)在一定条件下,SO2转化为SO3的反应为2SO2(g)+O2(g) 2SO3(g) ,该反应的平衡常数表达式为K= ??;过量的SO2与NaOH溶液反应的化学方程式为?
2SO3(g) ,该反应的平衡常数表达式为K= ??;过量的SO2与NaOH溶液反应的化学方程式为?
(2)酸溶及后续过程中均需保持盐酸过量,其目的是?、??。
(3)通氯气氧化后时,发生的主要反应的离子方程式为??;该过程产生的尾气可用碱溶液吸收,尾气中污染空气的气体为 ?(写化学式)。
参考答案:(1)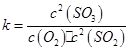 ? SO2+NaOH=NaHSO3;
? SO2+NaOH=NaHSO3;
(2)提高铁元素的浸出率?抑制Fe3+水解
(3)Cl2+2Fe2+=2Cl-+2Fe3+? Cl2? HCl
本题解析:(1)根据化学平衡常数概念写出平衡常数表达式;在一定条件下,SO2转化为SO3的反应为2SO2(g)+O2(g) 2SO3(g) ,该反应的平衡常数表达式为
2SO3(g) ,该反应的平衡常数表达式为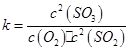 ;过量的SO2与NaOH溶液反应生成亚硫酸氢钠,化学方程式为SO2+NaOH=NaHSO3;(2)根据题给流程知,酸溶的目的是将氧化铁转化为氯化铁,盐酸可抑制铁离子水解,酸溶及后续过程中均需保持盐酸过量,其目的是提高铁元素的浸出率、抑制Fe3+水解。(3)通氯气氧化的目的是将亚铁离子氧化为铁离子,发生的主要反应的离子方程式为Cl2+2Fe2+=2Cl-+2Fe3+;该过程产生的尾气可用碱溶液吸收,尾气中污染空气的气体为Cl2、HCl。2)为原料制备氯化铁晶体(FeCl3・6H2O)的工艺流程为载体考查平衡常数表达式的书写、物质的分离和提纯。
;过量的SO2与NaOH溶液反应生成亚硫酸氢钠,化学方程式为SO2+NaOH=NaHSO3;(2)根据题给流程知,酸溶的目的是将氧化铁转化为氯化铁,盐酸可抑制铁离子水解,酸溶及后续过程中均需保持盐酸过量,其目的是提高铁元素的浸出率、抑制Fe3+水解。(3)通氯气氧化的目的是将亚铁离子氧化为铁离子,发生的主要反应的离子方程式为Cl2+2Fe2+=2Cl-+2Fe3+;该过程产生的尾气可用碱溶液吸收,尾气中污染空气的气体为Cl2、HCl。2)为原料制备氯化铁晶体(FeCl3・6H2O)的工艺流程为载体考查平衡常数表达式的书写、物质的分离和提纯。
本题难度:一般
3、选择题 在一定温度下的定容密闭容器中,表明反应:A(g)+2B(g)  ?C(g)+D(g)已达到平衡状态的是(? )
?C(g)+D(g)已达到平衡状态的是(? )
A. A、C、D的物质的量浓度相等?B. 混合气体的密度不再改变?
C. 气体的总物质的量不再改变? D. v(B) = 2v(C)
参考答案:C
本题解析:在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态。物质的浓度不再发生变化,但物质之间的浓度不一定相等或满足某种关系,A是错误的。混合气的密度是混合气的质量和容器容积的比值,再反应过程中质量和容积是不变的,所以密度始终是不变的,B不正确。反应是体积减小的可逆反应,因此当混合气的总物质的量不再发生变化时,可以说明反应达到平衡状态,C正确。在任何情况下速率之比都是相应的化学计量数之比,D不正确。答案选C。
本题难度:简单
4、选择题 相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:
N2(g)+3H2(g)  ?2NH3(g)+ 92.4 kJ。实验测得起始、平衡时的有关数据如下表:
?2NH3(g)+ 92.4 kJ。实验测得起始、平衡时的有关数据如下表:
容器编号
| 起始时各物质的物质的量/mol[]
| 平衡时反应中的能量变化
|
N2
| H2
| NH3
|
①
| 1
| 3
| 0
| 放出热量a kJ
|
②
| 2
| 3
| 0
| 放出热量b kJ
|
③
| 2
| 6
| 0
| 放出热量c kJ
|
下列叙述正确的是?
A.反应的平衡常数:③>①>②? B.达到平衡时氨气的体积分数:①>③
C.放出的热量(kJ):a<b<92.4? D.反应得到1mol NH3(l),放出热量46.2kJ
参考答案:C
本题解析:平衡常数只与温度有关系,所以三个容器中的平衡常数相同,A不正确。③相当于在①的基础上缩小容器的弱碱,平衡向正反应方向移动,所以达到平衡时氨气的体积分数是③>①,B不正确。反应是可逆反应,所以①②中不可能生成1mol氨气。②增大氢气的浓度,通过氮气的转化率,所以选项C正确。生成1mol氨气时放热46.2kJ,而不是液氨,D不正确。答案选C。
本题难度:一般
5、选择题 在一定温度下体积固定的容器中,可以充分说明可逆反应A(g)+3B(g) 3C(g)+2D(g),达到平衡状态的是
3C(g)+2D(g),达到平衡状态的是
A.混合气的平均相对分子质量不再改变?
B.反应器内A、B、C、D物质的量比为1:3:3:2
C.容器内密度不随时间变化而变化
D.生成 1mol A同时有3 mol C被消耗
参考答案:A
本题解析:A.混合气的平均相对分子质量等于气体的总质量除以总物质的量。根据质量守恒知,气体的总质量一直不变,而总物质的量只有达到平衡才会保持不变,所以混合气的平均相对分子质量不再改变能说明反应达到平衡状态。B,平衡时A、B、C、D物质的量之比不一定等于系数比,B错。C.气体的总质量一直保持不变,容器的容积也保持不变,所以容器内密度一直保持不变,C错。D.反应的任意时刻,生成 1mol A同时都会有3 mol C被消耗,D错。故选A
本题难度:一般