微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 下图所示为常见气体制备、分离、干燥和性质验证的部分仪器装置(加热设备及夹持固定装置均略去),请根据要求完成下列各题(仪器装置可任意选用,必要时可重复选择,a、b为活塞)。
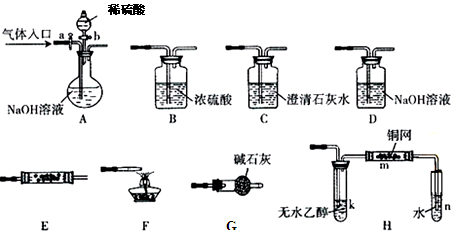
(1)若气体入口通入CO和CO2的混合气体,E内放置CuO,选择装置获得纯净干燥的CO,并验证其还原性及氧化产物,所选装置的连接顺序为 (填代号)。能验证CO氧化产物的现象是 。
(2)停止CO和CO2混合气体的通入,E内放置Na2O2,按A→E→D→B→H装置顺序制取纯净干燥的O2,并用O2氧化乙醇。此时,活塞a应 ,活塞b应 ,需要加热的仪器装置有 (填代号),m中反应的化学方程式为: 。
(3)若气体入口改通空气,分液漏斗内改加浓氨水,圆底烧瓶内改加NaOH固体,E内放置铂铑合金网,按A→G→E→D装置顺序制取干燥的氨气,并验证氨的某些性质。
①装置A中能产生氨气的原因有 。
②实验中观察到E内有红棕色气体出现,证明氨气具有 性。
参考答案:(1)ACBECF(2分)? AB之间的C装置中溶液保持澄清,EF之间的C装置中溶液变浑浊。(2分)(2)关闭(1分) 打开(1分) k和m(2分)? 2CH3CH2OH+O2 2CH3CHO+2H2O (2分)(3) ①氢氧化钠溶于水放出大量热,温度升高,使氨的溶解度降低而放出;氢氧化钠吸水,促使氨气放出;氢氧化钠电离出的OH-增大了氨水中的OH-浓度,使氨的电离平衡左移,促使氨气放出。(3分)②还原(1分)
2CH3CHO+2H2O (2分)(3) ①氢氧化钠溶于水放出大量热,温度升高,使氨的溶解度降低而放出;氢氧化钠吸水,促使氨气放出;氢氧化钠电离出的OH-增大了氨水中的OH-浓度,使氨的电离平衡左移,促使氨气放出。(3分)②还原(1分)
本题解析:(1)用A装置的NaOH来除CO中混有的CO2,(生成Na2CO3),用C装置检验有没有除尽CO2,B装置是干燥气体的,纯净的CO,通入E中,生成的CO2能使装置C有沉淀,多余的CO在装置F处尾气吸收。
(2)关闭装置A的活塞a,停止通入CO和CO2,打开活塞b,使稀硫酸和A中的碳酸钠反应,产生CO2,通入E,和Na2O2,产生O2,用D吸收O2混有的CO2,用B干燥O2中的H2O,纯净的O2在H中和乙醇发生催化氧化反应。加热k产生乙醇蒸汽,加热m ,是因为乙醇催化氧化需要催化剂铜和加热条件。
(3)这过程发生的反应为4NH3+5O2=4NO+6H2O(NH3表现还原性);2NO+O2=2NO2(红棕色)。
本题难度:一般
2、实验题 (15分)某过碳酸钠中含有少量过氧化钠,甲.乙两位同学各称取一定质量的该样品,并用如下图所示仪器测定样品的纯度。仪器的连接顺序,甲同学:⑤―⑧―③―⑦―④;乙同学:⑤―③―②。
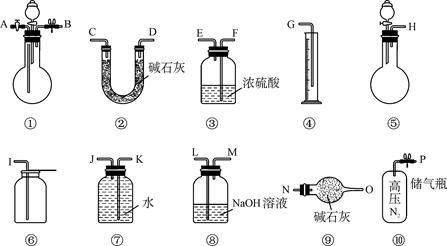
已知:过碳酸钠(Na2CO4).过氧化钠分别跟足量稀硫酸反应的化学方程式如下:
2Na2CO4+2H2SO4===2Na2SO4+2CO2↑+O2↑+2H2O;
2Na2O2+2H2SO4===2Na2SO4+O2↑+2H2O。
(1)甲同学想通过实验测得的数据是____________,他选用的装置________(填序号)是没有必要的。实验中甲同学测得气体体积为V L (20 ℃,1大气压),计算时他未将V L换算到标准状况,则他得到的Na2CO4的质量分数________(填“偏高”或“偏低”")。
(2)乙同学想通过实验测得的数据是________________。按他测得的数据计算出的实验结果有可能偏高,原因是________________;也有可能偏低,原因是 。
(3)为了测得准确的实验数据,请你将乙同学的实验设计进行改进,写出你所选用仪器的连接顺序(每种仪器最多使用一次,也可以不用):________________(填序号)。
参考答案:(1)生成的氧气的体积(2分) ③(2分) 偏低(2分)
(2)生成的二氧化碳的质量(2分) 空气中的水与二氧化碳进入②增重使结果偏大(2分) 产生的二氧化碳在装置⑤.③及导管中没有完全被②吸收使结果偏小(2分)
(3)⑩①③②⑨(3分)
本题解析:(1)根据甲的实验原理可知,甲是想通过测量排出的水的体积来计算生成的氧气体积,进而来计算样品的纯度的,所以将氧气干燥是多余的。若未将未将V L换算到标准状况,则其体积偏大。而根据方程式可以看出,在质量相等时过氧化钠生成的氧气要多。所以Na2CO4的质量分数偏小。
(2)由乙的实验原理可知,乙是通过测量生成的二氧化碳的质量来测定其纯度的。由于空气中含有水饱和二氧化碳,所以有可能使装置②的质量增加,导致结果偏大。如果反应中生成的二氧化碳没有被②完全吸收,也有可能使测定的结果偏低。
(3)要使结果更准确,就必须使反应中生成的二氧化碳完全被碱石灰吸收,而且还需要保证空气中的水和二氧化碳不参与反应,所以正确的顺序是⑩①③②⑨。
本题难度:一般
3、选择题 下图所示仪器可用于实验室制备少量无水FeCl3,仪器连接顺序正确的是( )

A.a-b-c-d-e-f-g-h
B.a-e-d-c-b-h-i-g
C.a-d-e-c-b-h-i-g
D.a-c-b-d-e-h-i-f
参考答案:B
本题解析:装置顺序为:制氯气、除杂(HCl、水蒸气)、反应制备、尾气处理,注意洗气瓶中导管为“长进短出”。
本题难度:一般
4、实验题 若配制500 mL 0.2 mol/L的稀硫酸:
(1)需要量取质量分数为98%的硫酸( 密度为1.84 g・mL-1)_____________mL。
密度为1.84 g・mL-1)_____________mL。
(2)下面是某学生的操作过程:
a.检查容量瓶是否漏水;b.用100 mL的量筒量取浓硫酸;
c.将浓硫酸倒入 另一个盛有适量蒸馏水的量筒中稀释,并冷却到室温;
另一个盛有适量蒸馏水的量筒中稀释,并冷却到室温;
d.用玻璃棒引流,将稀释后的硫酸倒入500 mL的容量瓶;
e.轻轻摇动容量瓶,使瓶内液体混合均匀,再向容量瓶中加水至离刻度线1 cm~2 cm;
f.用胶头滴管加水至凹液面底部与刻度线相切,摇匀;
g.在容量瓶上贴上标签待用。
按照通常的配制要求,指出其中缺少或操作的错误,并补充或改正(有几项填几项 ,若空格不够可以补加)。
,若空格不够可以补加)。
①________________________________________________________;
②________________________________________________________;
③________________________________________________________;
④________________________________________________________;
⑤________________________________________________________。
(3)任何实验都有误差,在你改正后的操作中,产生误差的原因还有_________________。(4)本实验最浪费时间的步骤是将稀释后的硫酸冷却到室温,为了节约时间,简便易行的加快稀硫酸冷却的方法是_______________________。
参考答案:(1)5.4
(2)①缺少洗涤烧杯和玻璃棒的操作
②量筒的规格错,应该用10 mL的量筒量取浓H2SO4(或用移液管、酸式滴定管量取浓H2SO4)
③不应该在量筒中稀释浓H2SO4,应用烧杯
④不应该用容量瓶保存溶液,应用细口瓶
(3)量筒的精确度不够高(或读数误差,溶质仍有少量残留在烧杯内、室温未必是20℃等)
(4)充分搅拌(给盛有稀H2SO4的烧杯敷冰块等)
本题解析:略
本题难度:简单
5、选择题 下列实验不能用水浴加热的是(?)
A.苯的硝化制硝基苯
B.乙酸乙酯的水解
C.用乙醇制乙醚
D.麦芽糖与银氨溶液的反应
参考答案:C
本题解析:略
本题难度:简单