微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列有关说法正确的是:(?)
A.由14N2和15N2组成的物质是混合物
B.在常温常压下,11.2L氧气所含的原子数目为NA
C.第三周期的元素从左往右非金属性逐渐增强
D.电解MgCl2饱和溶液,可制得金属镁
参考答案:C
本题解析:
正确答案:C
A.不正确,由14N2和15N2组成的物质是纯净物,它们同属氮气分子;
B.不正确,应在标准状况下,11.2L氧气所含的原子数目为NA
C.正确,从元素周期律可以得出结论,第三周期的元素从左往右非金属性逐渐增强
D.不正确,电解MgCl2饱和溶液,MgCl2+2H2O Mg(OH)2+H2↑+Cl2↑
Mg(OH)2+H2↑+Cl2↑
本题难度:一般
2、选择题 下列元素中基态原子的第一电离能最大的是(?)
A.O
B.B
C.C
D.N
参考答案:D
本题解析:气态电中性基态原子失去1个电子转化为气态基态正离子所需要的最低能量叫第一电离能。金属性越强,第一电离能越小,非金属性越强,第一电离能越大。但氮的第一电离能缺大于氧的,所以答案选D。
本题难度:一般
3、选择题 下列说法正确的是(?)
A.第ⅠA族金属单质的密度、熔沸点均随着核电荷数的增大而递增
B.金属锂在氧气中燃烧生成Li2O2
C.金属的还原性:Li>Na>K>Rb
D.氢化物的稳定性: HF > HCl > HBr > HI
参考答案:D
本题解析:第ⅠA族金属单质的密度随着核电荷数的增大而递增,但熔沸点随着核电荷数的增大而减小,A不正确;金属锂在氧气中燃烧生成Li2O,得不到Li2O2,B不正确;同主族自上而下,金属性逐渐增强,则金属的还原性:Li<Na<K<Rb,C不正确;非金属性越强,则氢化物的温度下越强,所以氢化物的稳定性:HF>HCl>HBr>HI,D正确,答案选D。
点评:该题主要是考查学生对元素周期律的熟悉了解程度,以及灵活运用元素周期律解决实际问题的能力。难度不大。该题的关键是熟练记住元素周期律的具体内容,然后结合题意灵活运用即可,有利于培养学生的逻辑思维能力。
本题难度:一般
4、选择题 下图是周期表中短周期的一部分,A、B、C三种元素的原子核外电子数等于B的质量数,B元素的原子核内质子数等于中子数,下列叙述不正确的是(?)

A.B为第三周期的元素? B.C为VA族元素
C.三种元素都为非金属元素? D.C是化学性质最活泼的非金属元素
参考答案:B
本题解析:如图所示,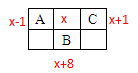 A、B、C三种元素的的核外电子数依次为x-1;x+8;x+1,依题意有:(x+1)+(x+8)+(x-1)=2(x+8),求得x=8,即A、B、C三种元素的的核外电子数依次为7;16;9,即A、B、C三种元素分别为N、S、F。C元素(F)为VIIA族的元素,故B错。
A、B、C三种元素的的核外电子数依次为x-1;x+8;x+1,依题意有:(x+1)+(x+8)+(x-1)=2(x+8),求得x=8,即A、B、C三种元素的的核外电子数依次为7;16;9,即A、B、C三种元素分别为N、S、F。C元素(F)为VIIA族的元素,故B错。
本题难度:简单
5、填空题 X、Y、Z和W代表原子序数依次增大的4种短周期元素,它们满足以下条件:
①元素周期表中,Z与Y相邻,Z与W也相邻;
②Y、Z和W 3种元素的原子最外层电子数之和为17。
请填空:
(1)Y、Z和W 3种元素是否位于同一周期(填“是”或“否”):_____________,理由是_______________________________________________________________。
(2)Y是____________,Z是____________,W是____________ 。
(3)X、Y、Z和W可组成一化合物,其原子个数之比为8∶2∶4∶1。写出该化合物的名称及化学式_________________________________________。
参考答案:(1)否?若三者处于同一周期,则最外层电子数之和不可能为17?(2)N? O? S?(3)硫酸铵 (NH4)2SO4
本题解析:因为Z与Y,Z与W相邻,所以Z与Y原子序数相差1,Z与W相邻,原子序数相差1。如果在同一周期,则3种元素Y、Z、W依次排布,设Z最外层电子数为a,则Y为a-1,Z为a+1,则3a=17,a不符合1―8正整数。只能是Y、Z一周期,W为下一周期,设Z最外层电子数为a,则W为a,Y为a-1,则3a-1=17,a=6,则Z为O,W为S,Y为N。化合物分子式为H8N2O4S,只能是铵盐,符合条件的只有硫酸铵。
本题难度:简单