��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��������ƽ�������ϣ��ֱ��������������ͬ���ձ�����ʢ��6mol/LHCl100mL��ʹ��ƽ�ﵽƽ�⣮�ֱ������ձ��м��벻����5g��þ��������Ҫʹ���ַ�Ӧ����ƽ�Ա���ƽ�⣬������þ����������֮��Ϊ��������
A��1��1
B��24��27
C��12��9
D��32��33
�ο��𰸣�n��HCl��=0.01L��6mol/L=0.06mol��þ����������������5g���ɷ�ӦMg+2HCl=MgCl2+H2����2Al+6HCl=2AlCl3+3H2����֪��������ȫ��Ӧ������������Ҫʹ���ַ�Ӧ����ƽ�Ա���ƽ�⣬Ӧ��֤������ƽ���������н�������������������������֮����ȣ�
��þ������Ϊx����������Ϊy��
��Mg+2HCl=MgCl2+H2����m
24 22
��������22x24��
2Al+6HCl=2AlCl3+3H2����m
5448
��������48y54��
��22x24=48y54��
x��y=32��33��
��ѡD��
���������
�����Ѷȣ�һ��
2��ѡ���� ʳ�Ρ����ǡ����ᡢ������͡���84����Һ�������ճ������о���ʹ�õ����ʣ������й�˵�����ʾ��ȷ����
A��ʳ���������ӵĺ�������Ų��ṹʾ��ͼΪ��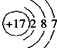
B������������ȥ�����۵�ԭ����ͬ
C����84����Һ������Ч�ɷ�NaClO�ĵ���ʽΪ��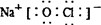
D���������������ʽ��ͬ
�ο��𰸣�C
���������A��ʳ��ΪNaCl����������ΪCl�C��Cl�C���������Ϊ18����������Ų�ʽ�ṹʾ��ͼΪ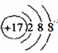 ������B������ȥ��ԭ������Ϊ����ˮ��ʹ��Һ�ʼ��ԣ������ڼ���������ˮ�⣬����������ˮ�ĸ�֬�����ƺ��ͣ���������ȥ������Ϊ���;��лӷ��ԣ������ܽ����ۣ���ͬ�ӷ������Դ���������ȥ�����۵�ԭ������ͬ������C����84����Һ������Ч�ɷ�ΪNaClO�������������Ӻʹ���������ӹ��ɣ�����ʽΪ��
������B������ȥ��ԭ������Ϊ����ˮ��ʹ��Һ�ʼ��ԣ������ڼ���������ˮ�⣬����������ˮ�ĸ�֬�����ƺ��ͣ���������ȥ������Ϊ���;��лӷ��ԣ������ܽ����ۣ���ͬ�ӷ������Դ���������ȥ�����۵�ԭ������ͬ������C����84����Һ������Ч�ɷ�ΪNaClO�������������Ӻʹ���������ӹ��ɣ�����ʽΪ��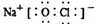 ����ȷ��D�����ǵķ���ʽΪC12H22O11�����ʽΪC12H22O11������ķ���ʽC2H4O2�����ʽΪCH2O�����ߵ����ʽ����ͬ������
����ȷ��D�����ǵķ���ʽΪC12H22O11�����ʽΪC12H22O11������ķ���ʽC2H4O2�����ʽΪCH2O�����ߵ����ʽ����ͬ������
�����Ѷȣ�һ��
3��ѡ���� ����˵���д�����ǣ�?��
A������������ԭ��Ӧ�����������Ǹ��ֽⷴӦ
B�����Ϸ�Ӧ��������������ԭ��Ӧ
C���û���Ӧһ����������ԭ��Ӧ
D���ֽⷴӦ������������ԭ��Ӧ
�ο��𰸣�B
������������ֽⷴӦһ������������ԭ��Ӧ��A��ȷ���е��ʲμӵĻ��Ϸ�Ӧ��������ԭ��Ӧ��B����ȷ��һ�ֵ��ʺ�һ�ֻ����ﷴӦ��������һ�ֵ��ʺͻ�����ķ�Ӧ���û���Ӧ�����C��ȷ��DҲ����ȷ�ģ��е������ɵķֽⷴӦҲ��������ԭ��Ӧ����ѡB��
������������Ԫ�ػ��ϼ������ķ�Ӧһ����������ԭ��Ӧ������ȷ����й�Ԫ�صĻ��ϼ����жϵĹؼ���������ԭ��Ӧ�����ֻ�����Ӧ���͵Ĺ�ϵ������ͼ������ı�ʾ
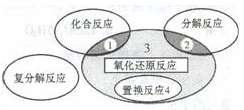 ��
��
�����Ѷȣ�һ��
4������� ����[CO(NH2)2]��һ�ַdz���Ҫ�ĸߵ�����,����Ȼ������H2S)Ϊԭ�Ϻϳ����ص���Ҫ��������ͼ��ʾ��ͼ��ijЩת������δ�г�����
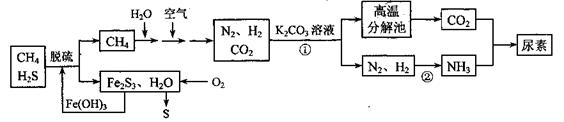
��ش��������⣺
��1����Ӧ�ٵ����ӷ���ʽ��______________
��2����Ȼ������������Fe2S3��H2O��02��Ӧ�Ļ�ѧ����ʽ��_______��
��3����Ӧ���Ƿ��ȷ�Ӧ���¶����ߣ��÷�Ӧ��ƽ�ⳣ��_______ (�� ����������С�� ���䡱)��H2NCOONH4(��������泥��Ǻϳ����ص��м��壬����̼ԭ�ӵ��ӻ����������_______�ӻ���
��4����������������������ɫ��ѧ���գ�������120t������������Ҫ?CH4___m3 (��״������
��5����ѧ�������о����ض���ȼ�ϵ�أ���ҺҲ�ܷ��磡�����ֵ��ֱ��ȥ�����з�ˮ�е����أ����ܲ���������ˮ���ܷ��硣����ȼ�ϵ�ؽṹ��ͼ��ʾ������ʱ�����ĵ缫��ӦʽΪ__________
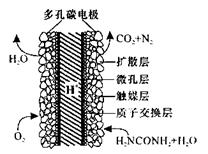
�ο��𰸣���14�֣�
��1��CO32-��CO2��H2O=2HCO3-��2�֣�
��2��2Fe2S3��6H2O��3O2=4Fe(OH)3��6S��2�֣�
��3����С��2�֣�? sp2��2�֣�?��4��4.48��104��3�֣�
��5��CO(NH2)2��H2O��6e��= N2����CO2����6H+��3�֣�
�����������1����Ӧ�ٷ���������̼��̼�����Һ��Ӧ����̼����أ������ӷ�ӦΪCO32-+CO2+H2O�T2HCO3-����2��Fe2S3��H2O��02��Ӧ��������������S���÷�ӦΪ2Fe2S3+6H2O+3O2�T4Fe��OH��3+6S����3����Ӧ��Ϊ�ϳɰ��ķ�Ӧ�����ȷ�Ӧ���¶����ߣ�ƽ�������ƶ�����ƽ�ⳣ��K��С��H2NCOONH4�е�Cԭ����û�й¶Ե��ӣ��ɼ���Ϊ3��Cԭ�Ӳ�ȡsp2�ӻ�����4����Cԭ���غ��֪��CH4��CO2��CO��NH2��2��������120t������������ҪCH4Ϊ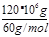 ��22.4L/mol��10-3m3=4.48��104m3����5������ȼ�ϵ���������ٸ�����ʧȥ�������ɵ�����������̼��������ӦΪCO��NH2��2+H2O-6e-�TN2��+CO2��+6H+��
��22.4L/mol��10-3m3=4.48��104m3����5������ȼ�ϵ���������ٸ�����ʧȥ�������ɵ�����������̼��������ӦΪCO��NH2��2+H2O-6e-�TN2��+CO2��+6H+��
�����Ѷȣ�һ��
5������� ��2�֣���ԭ�ӵ�������Ϊ23��������Ϊ12����ô���ĺ����������__________,��������__________��
�ο��𰸣�11? 11
�������������������=������+�����������������=������֪����������������Ϊ11.
�����Ѷȣ���