微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列原子半径最小 的是
A.F
B.P
C.O
D.Cl
2、填空题 根据已有内容的规律进行增补
(1)同族元素单质间的置换反应的化学方程式:
①2Na+2H2O=2NaOH+H2↑?②2HBr+Cl2=2HCl+Br2 ③2H2S+O2=2S+2H2O?④______
(2)已知
| 化学键 | Si-O | Si-Cl | H-Cl | Si-Si
键能/KJ?mol-1
460
360
431
176
|
回答下列问题:
①比较熔点SiCl4______SiO2(填“>”或“<”),
②工业制纯硅反应:SiCl4(g)+H2(g)=Si(s)+2HCl(g)△H=+118KJ?mol-1则H-H键能为______KJ?mol-1.
3、选择题 核磁共振(NMR)技术已广泛应用于复杂分子结构的测定和医学诊断等高科技领域。已知只有质子数或中子数为奇数的原子核有NMR现象。试判断下列哪组原子均可产生NMR现象
[? ]
A.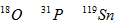
B.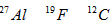
C.元素周期表中VA族所有元素的原子
D.元素周期表中第1周期所有元素的原子
4、简答题 下表是元素周期表的一部分.
族
周期 | I?A | II?A | III?A | IV?A | V?A | VI?A | VII?A
一
|
二
a
b
?d
e
三
f
g
h
j
|
(1)表中元素的单质中熔点最高的可能是______(填元素符号);写出a的氯化物的电子式______;e、f、h形成的简单离子的半径由大到小顺序依次为______(填离子符号).
(2)在一定条件下,j与d可形成一种化合物,常温下为淡黄色液体,则其晶体类型为______.该物质遇水强烈水解,生成两种产物,其中之一的分子构型为三角锥形,另一种物质具有漂白性,写出相关反应的化学方程式______.
(3)现有一种元素,其原子获得一个电子所释放出能量是上表中所列元素中最大的,该元素是表中______元素(填编号).
(4)在g的单质中添加f单质,形成物质k,则g、f、k中硬度最大的是______(填物质名称).
(5)若制得117号元素,按元素周期表中金属与非金属的分区,它应是一种______(选填“金属”“非金属”)元素,写出117号元素最外层电子排布式______.
(6)试用短周期元素,写出两种中心原子杂化轨道类型不同的AB3型分子的化学式______、______.
5、简答题 在下表所列的各元素组中,除一种元素外,其余都可以按某种共性归属一类.请选出各组中的例外元素,并将该组其他元素的可能归属按所给6种类型的编号填入表内.归属类型为:①主族元素;②过渡元素;③同周期元素;④同族元素;⑤金属元素;⑥非金属元素.
| 元?素 | 例外元素 | 其他元素所属类型
(1)S、N、Na、Mg
______
______
(2)Li、K、Ca、Cs
______
______
(3)Rb、B、I、Fe
______
______
|