微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 实验室需要0.5mol/L的硫酸500mL,若使用溶质的质量分数为98%(密度为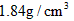 )的浓硫酸进行配制。求:
)的浓硫酸进行配制。求:
(1)该浓硫酸的物质的量浓度;
(2)需要浓硫酸的体积。
参考答案:(1)18.4mol/L
(2)13.6mL
本题解析:
本题难度:一般
2、简答题 某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路.课外活动小组为确认生产后的废液的组成,进行如下实验:
Ⅰ.取50mL废液稀释配成250mL溶液.
Ⅱ.从250mL稀释溶液取25mL加入足量的AgNO3溶液,生成不溶于硝酸的沉淀8.61g.
Ⅲ.另从250mL稀释溶液取25mL放入铜片充分反应,铜片质量减少了0.256g.
(1)操作I是配制物质的量浓度溶液,所用到的玻璃仪器除烧杯、玻璃棒外,还必须有______、______.(填仪器名称)
(2)下列操作可能使所配溶液浓度偏小的是______(填写序号).
①未洗涤烧杯和玻璃棒
②定容时俯视容量瓶的刻度线
③配溶液前容量瓶中有少量蒸馏水
④摇匀后,发现液面低于刻度线后继续加水至凹液面与刻度线相切
(3)操作Ⅱ中检验沉淀是否已经洗涤干净的操作是______.
(4)原废液中氯离子的物质的量浓度是______.
(5)原废液中三种阳离子浓度比值c(Fe3+):c(Fe2+):c(Cu2+)为______.
参考答案:(1)一定规格的容量瓶只能配制相应体积的溶液,容量瓶应选择250ml规格;用量筒量取废液体积,在烧杯中溶解(可用量筒量取水),用玻璃棒搅拌,冷却后转移到250mL容量瓶中,并用玻璃棒引流,洗涤并将洗涤液移入容量瓶中,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加至溶液凹面与刻度线水平相切,盖好瓶塞,摇匀.所以需要的仪器为:量筒、烧杯、玻璃棒、250ml容量瓶、胶头滴管,故答案为:量筒;250ml容量瓶、胶头滴管;
(2)①未洗涤烧杯和玻璃棒,转移到容量瓶中溶质的质量减小,所配溶液浓度偏低,故①正确;
②定容时俯视容量瓶的刻度线,使溶液的体积偏低,所配溶液浓度偏高,故②错误;
③定容时需要加入蒸馏水,配溶液前容量瓶中有少量蒸馏水无影响,故③错误;
④继续加水至凹液面与刻度线相切,使溶液的体积增大,所配溶液浓度偏低,故④正确;
故答案为:①④;
(3)沉淀洗涤就是把Cl-洗掉,可以检验洗涤液中是否含有Cl-,取少量最后一次洗出液,滴加AgNO3溶液,若无沉淀生成,则证明洗涤干净,故答案为:取少量最后一次洗出液,滴加AgNO3溶液,若无沉淀生成,则证明洗涤干净;
(4)n(Clˉ)=8.61g143.5g/mol=0.06mol,C=nV=()()0.06mol×100.05L=12mol/l,故答案为:12mol/l;
(5)反应的n(Fe 3+)=0.256g64g/mol×2=0.0008mol,剩余的n(Fe 3+)=0.02-0.0008=0.0192mol,根据铜与氯化铁反应的方程式可知,废液中n(Fe2+):n(Cu2+)=2:1.由离子电荷守恒得等式:
n(Clˉ)=3 n(Fe3+)+2n(Fe2+)+2n(Cu2+)
0.06=3×0.0192+2n(Fe2+)+2×0.0004
,可求出原废液中n(Fe2+)=0.0008mol,得c(Fe3+):c(Fe2+):c(Cu2+)=0.0192mol:0.0008mol:0.0004mol=49:2:1,故答案为:49:2:1;
本题解析:
本题难度:简单
3、选择题 实验室用浓硫酸配制1 mol・L-1的稀硫酸溶液250 mL,下列不需要的仪器是
[? ]
A.烧杯
B.漏斗
C.玻璃棒
D.容量瓶
参考答案:B
本题解析:
本题难度:简单
4、选择题 实验室需用480mL0.1mol・L-1的硫酸铜溶液,现选取500mL容量瓶进行配制,以下操作正确的是
[? ]
A.称取7.68g硫酸铜,加入480mL的水
B.称取12.0g胆矾,配成480mL溶液
C.称取8.0g硫酸铜,加入500mL水
D.称取12.5g 胆矾,配成500mL溶液
参考答案:D
本题解析:
本题难度:简单
5、实验题 实验室用密度为1.84g/cm3,溶质的质量分数为98%的硫酸,配制980mL物质的量浓度为0.1mol/L的硫酸。供选用的仪器有:
① 胶头滴管;② 烧瓶;③ 烧杯;④ 药匙;⑤ 量筒;⑥ 托盘天平。
请回答下列问题:
(1)配制稀硫酸时,上述仪器中不需要使用的有________(选填序号),还缺少的仪器有________(写仪器名称);
(2)经计算,配制上述稀硫酸需要用量筒量取所给浓硫酸的体积为________mL,量取浓硫酸时应选用
________(选填 ① 10mL、② 50mL 、③ 100mL)规格的量筒;
(3)下列操作使所配溶液的物质的量浓度偏高的是__________。
A、用量筒量取的浓H2SO4,慢慢地沿着玻璃棒注入盛有20mL蒸馏水的小烧杯,搅拌后,立即转移到容量瓶中,再按正确操作配制溶液。
B、往容量瓶转移溶液时,有少量液体溅出。
C、未洗涤稀释浓H2SO4的小烧杯
D、定容时俯视刻度线。
E、容量瓶未干燥即用来配制溶液。
F、定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线。
参考答案:(1)②④⑥;1000mL的容量瓶、玻璃棒
(2)5.4mL;10mL
(3)AD
本题解析:
本题难度:一般